Nuevos artículos
TIVDAK®, aprobado por la FDA: dirigido al factor tisular en el cáncer de cuello de útero
Último revisado: 02.07.2025

Todo el contenido de iLive se revisa médicamente o se verifica para asegurar la mayor precisión posible.
Tenemos pautas de abastecimiento estrictas y solo estamos vinculados a sitios de medios acreditados, instituciones de investigación académica y, siempre que sea posible, estudios con revisión médica. Tenga en cuenta que los números entre paréntesis ([1], [2], etc.) son enlaces a estos estudios en los que se puede hacer clic.
Si considera que alguno de nuestros contenidos es incorrecto, está desactualizado o es cuestionable, selecciónelo y presione Ctrl + Intro.
El 29 de abril de 2024, la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) otorgó la aprobación total a TIVDAK® (tisotumab vedotin) de Seagen Inc., un fármaco dirigido al factor tisular (FT), para el tratamiento de pacientes con cáncer de cuello uterino recurrente o metastásico que ha progresado durante o después de la quimioterapia. Esto representa un avance significativo en la terapia del cáncer de cuello uterino, que destaca el potencial de los conjugados anticuerpo-fármaco (ADC) en oncología.
Mecanismo de acción de TIVDAK
Tivdak es un ADC que se dirige al TF mediante la combinación del anticuerpo monoclonal anti-TF tisotumab de Genmab con la tecnología ADC de Seagen diseñada para dirigirse a los antígenos TF en las células cancerosas y administrar el componente citotóxico MMAE directamente a las células cancerosas.
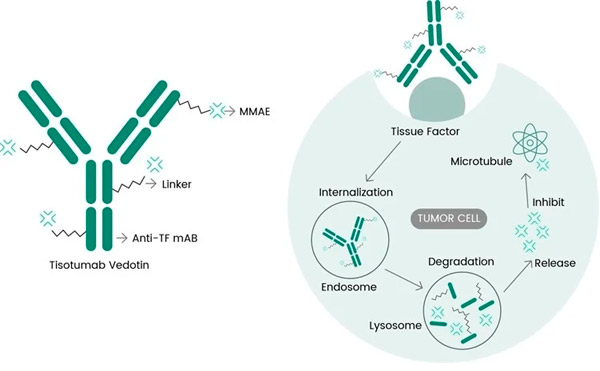
Mecanismo de acción molecular de tisotumab vedotin ( https://doi.org/10.3390/ijms23073559 )
TF: El objetivo perfecto para el desarrollo de ADC
Se sabe que el factor de transcripción (FT) participa en la señalización tumoral y la angiogénesis, y se sobreexpresa en la gran mayoría de pacientes con cáncer de cuello uterino y muchos otros tumores sólidos. Su capacidad de internalización rápida tras la unión a anticuerpos y su mínimo impacto en la coagulación sanguínea normal refuerzan aún más su idoneidad para la terapia dirigida contra el cáncer.
