Nuevos artículos
Identificada la proteína responsable de una enfermedad inflamatoria genética
Último revisado: 02.07.2025

Todo el contenido de iLive se revisa médicamente o se verifica para asegurar la mayor precisión posible.
Tenemos pautas de abastecimiento estrictas y solo estamos vinculados a sitios de medios acreditados, instituciones de investigación académica y, siempre que sea posible, estudios con revisión médica. Tenga en cuenta que los números entre paréntesis ([1], [2], etc.) son enlaces a estos estudios en los que se puede hacer clic.
Si considera que alguno de nuestros contenidos es incorrecto, está desactualizado o es cuestionable, selecciónelo y presione Ctrl + Intro.
Un equipo de investigadores, dirigido por el Dr. Hirotsugu Oda, del Clúster de Excelencia CECAD para la Investigación del Envejecimiento de la Universidad de Colonia, ha descubierto el papel de un complejo proteico en ciertas formas de desregulación inmunitaria. Este resultado podría impulsar el desarrollo de nuevos enfoques terapéuticos para reducir la autoinflación y restaurar el sistema inmunitario de pacientes con una disfunción genética de este complejo proteico.
El estudio, "La pérdida de función de SHARPIN humana bialélica induce autoinflamación e inmunodeficiencia", fue publicado en la revista Nature Immunology.
El complejo lineal de ensamblaje de ubiquitina (LUBAC), compuesto por las proteínas HOIP, HOIL-1 y SHARPIN, es reconocido desde hace tiempo por su papel crucial en el mantenimiento de la homeostasis inmunitaria. Estudios previos en ratones han demostrado las graves consecuencias de la pérdida de SHARPIN, que provoca dermatitis grave debido a la muerte excesiva de células cutáneas. Sin embargo, las consecuencias específicas de la deficiencia de SHARPIN para la salud humana siguen sin estar claras.
El equipo de investigación informó por primera vez de dos personas con deficiencia de SHARPIN que presentan síntomas de autoinflación e inmunodeficiencia, pero inesperadamente no muestran problemas dermatológicos como en los ratones.
Tras una investigación más exhaustiva, se descubrió que estos individuos presentaban una respuesta canónica de NF-κB alterada, una importante vía de respuesta inmunitaria. También presentaban una mayor susceptibilidad a la muerte celular inducida por miembros de la superfamilia del factor de necrosis tumoral (TNF). El tratamiento de un paciente con deficiencia de SHARPIN con terapia anti-TNF, que inhibe específicamente la muerte celular inducida por TNF, resultó en la resolución completa de la autoinflación a nivel celular y en la presentación clínica.
El estudio demuestra que la muerte celular excesiva e incontrolada desempeña un papel crucial en las enfermedades inflamatorias genéticas humanas. El equipo de Oda añadió la deficiencia de SHARPIN como un nuevo miembro de un grupo de enfermedades inflamatorias genéticas humanas que proponen denominar "errores innatos de muerte celular".
Protección contra la desregulación inmunitaria. El estudio se inició en el laboratorio del Dr. Dan Kastner, de los Institutos Nacionales de la Salud (NIH) de Estados Unidos. Allí, los científicos tuvieron la oportunidad de observar a un paciente con episodios inexplicables de fiebre, artritis, colitis e inmunodeficiencia, que comenzaron en la infancia.
Tras obtener el consentimiento informado, se realizó la secuenciación del exoma del paciente y sus familiares, y se descubrió que el paciente presentaba una variante genética devastadora en el gen SHARPIN que resultaba en niveles indetectables de la proteína SHARPIN. También se observó una mayor propensión a la muerte celular, tanto en cultivos celulares como en biopsias.
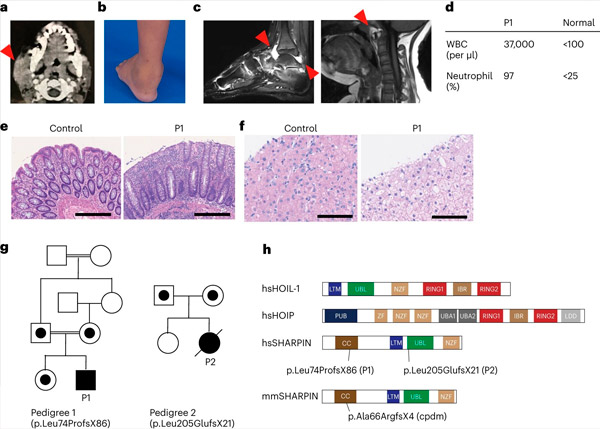
La deficiencia de SHARPIN en humanos causa autoinflamación y glucogenosis hepática. Fuente: Nature Immunology (2024). DOI: 10.1038/s41590-024-01817-w
El equipo también descubrió que el desarrollo de los centros germinales linfoides (microestructuras especializadas en las adenoides, cruciales para la maduración de las células B de nuestro sistema inmunitario y, por lo tanto, para la producción de anticuerpos) se redujo significativamente debido al aumento de la muerte de células B. Estos hallazgos explican la inmunodeficiencia de los pacientes y resaltan el importante papel de LUBAC en el mantenimiento de la homeostasis inmunitaria en humanos.
"Nuestro estudio destaca la importancia crucial de LUBAC en la protección contra la desregulación inmunitaria. Al dilucidar los mecanismos moleculares subyacentes a la deficiencia de LUBAC, allanamos el camino para nuevas estrategias terapéuticas destinadas a restablecer la homeostasis inmunitaria", afirmó Oda, autor principal del estudio.
Añadió: «Uno de los pacientes con deficiencia de SHARPIN llevaba años en silla de ruedas antes de que lo viéramos por primera vez. Tenía los tobillos inflamados y le dolía demasiado caminar. El diagnóstico genético nos permitió identificar la vía molecular correcta que subyace a sus afecciones».
Desde que el paciente comenzó a recibir terapia anti-TNF, ha estado asintomático durante casi siete años. «Como médico y científico, me complace tener la oportunidad de influir positivamente en la vida de un paciente a través de nuestra investigación», concluyó Oda.
