Nuevos artículos
La mutación del gen ARID1A hace que los tumores sean sensibles a la inmunoterapia
Último revisado: 02.07.2025

Todo el contenido de iLive se revisa médicamente o se verifica para asegurar la mayor precisión posible.
Tenemos pautas de abastecimiento estrictas y solo estamos vinculados a sitios de medios acreditados, instituciones de investigación académica y, siempre que sea posible, estudios con revisión médica. Tenga en cuenta que los números entre paréntesis ([1], [2], etc.) son enlaces a estos estudios en los que se puede hacer clic.
Si considera que alguno de nuestros contenidos es incorrecto, está desactualizado o es cuestionable, selecciónelo y presione Ctrl + Intro.
La inmunoterapia ha revolucionado el tratamiento del cáncer en los últimos años. En lugar de atacar directamente los tumores, la inmunoterapia dirige el sistema inmunitario del paciente para que los ataque con mayor eficacia. Esto es particularmente eficaz para algunos cánceres difíciles de tratar. Sin embargo, menos de la mitad de los pacientes con cáncer responden a las inmunoterapias actuales, lo que crea una necesidad urgente de identificar biomarcadores que puedan predecir qué pacientes tienen más probabilidades de beneficiarse del tratamiento.
Recientemente, los científicos han observado que los pacientes cuyos tumores tienen una mutación en el gen ARID1A tienen más probabilidades de responder positivamente al bloqueo del punto de control inmunitario, un tipo de inmunoterapia que funciona manteniendo activadas las células inmunes que combaten el cáncer.
Debido a que la mutación del gen ARID1A está presente en muchos tipos de cáncer, incluidos el de endometrio, ovario, colorrectal, gástrico, hepático y pancreático, los investigadores del Instituto Salk se preguntaron cómo podría contribuir a la sensibilidad del tratamiento y cómo los médicos podrían usar esta información para personalizar el tratamiento del cáncer para cada paciente.
Su nuevo estudio, publicado en la revista Cell, muestra que la mutación ARID1A hace que los tumores sean sensibles a la inmunoterapia al reclutar células inmunes que combaten el cáncer al tumor a través de una respuesta inmune similar a la antiviral.
Los investigadores sugieren que esta mutación y la respuesta inmunitaria antiviral podrían utilizarse como biomarcador para una mejor selección de pacientes para inmunoterapias específicas, como el bloqueo de puntos de control inmunitario. Estos hallazgos también fomentan el desarrollo de fármacos dirigidos a ARID1A y proteínas relacionadas para aumentar la sensibilidad de otros tumores a la inmunoterapia.
"Esto podría cambiar significativamente el resultado del tratamiento del cáncer para los pacientes", afirmó la profesora asociada Diana Hargreaves, autora principal del estudio. "Los pacientes con la mutación ARID1A ya poseen una respuesta inmunitaria, por lo que solo necesitamos potenciarla mediante el bloqueo de puntos de control inmunitario para ayudarlos a destruir sus tumores desde el interior".
Aunque se sabía que las personas con mutaciones en ARID1A respondían bien al bloqueo de puntos de control inmunitario, la conexión exacta entre ambos seguía sin estar clara. Para esclarecer el mecanismo, científicos del Instituto Salk utilizaron modelos murinos de melanoma y cáncer colorrectal con la mutación ARID1A y ARID1A funcional.
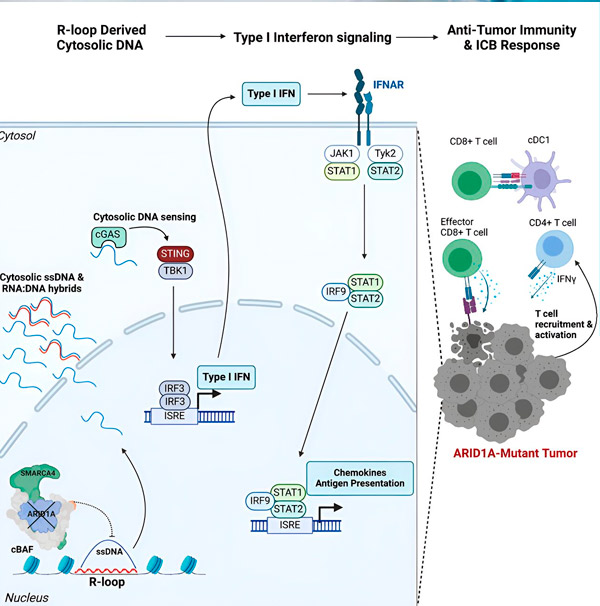
Fuente: Cell (2024). DOI: 10.1016/j.cell.2024.04.025
El equipo observó una respuesta inmunitaria robusta en todos los modelos con la mutación ARID1A, pero no en aquellos donde ARID1A era funcional, lo que respalda la idea de que la mutación ARID1A impulsa esta respuesta. Pero ¿cómo funciona esto a nivel molecular?
"Descubrimos que ARID1A desempeña un papel importante en el núcleo, manteniendo la correcta organización del ADN", afirma Matthew Maxwell, primer autor del estudio y estudiante de posgrado en el laboratorio de Hargreaves. "Sin ARID1A funcional, el ADN libre puede escindirse y liberarse al citosol, activando así una respuesta inmunitaria antiviral deseable que puede potenciarse mediante el bloqueo de puntos de control inmunitario".
El gen ARID1A codifica una proteína que ayuda a regular la forma de nuestro ADN y a mantener la estabilidad del genoma. Cuando ARID1A muta, desencadena una cadena de eventos similar a la de Rube Goldberg en las células cancerosas.
En primer lugar, la falta de ARID1A funcional provoca la liberación de ADN al citosol. El ADN citosólico activa entonces un sistema de alarma antiviral, la vía cGAS-STING, ya que nuestras células están adaptadas para marcar cualquier ADN en el citosol como extraño para protegerse contra infecciones virales. Finalmente, la vía cGAS-STING activa el sistema inmunitario para reclutar linfocitos T hacia el tumor y activarlos en linfocitos T especializados en la eliminación del cáncer.
En cada paso, dependiendo del anterior, esta cadena de eventos (mutación ARID1A, escape de ADN, alarma cGAS-STING, reclutamiento de linfocitos T) conduce a un aumento en el número de linfocitos T que combaten el cáncer en el tumor. El bloqueo de puntos de control inmunitario puede utilizarse entonces para asegurar que estos linfocitos T permanezcan activados, lo que aumenta su capacidad para combatir el cáncer.
«Nuestros hallazgos proporcionan un nuevo mecanismo molecular mediante el cual una mutación de ARID1A podría contribuir a una respuesta inmunitaria antitumoral», afirma Hargreaves. «Lo emocionante de estos hallazgos es su potencial translacional. Podemos utilizar las mutaciones de ARID1A para seleccionar pacientes para el bloqueo de puntos de control inmunitario, y ahora observamos un mecanismo mediante el cual los fármacos que inhiben ARID1A o su complejo proteico podrían utilizarse para mejorar aún más la inmunoterapia en otros pacientes».
Al describir el mecanismo por el cual el bloqueo de puntos de control inmunitario es más eficaz en cánceres con mutación en ARID1A, los investigadores justifican la priorización de esta inmunoterapia en pacientes con una mutación en ARID1A. Estos hallazgos representan un paso importante hacia la personalización del tratamiento del cáncer e inspiran el desarrollo de nuevas terapias dirigidas a ARID1A y su complejo proteico.
En el futuro, el equipo del Instituto Salk espera que sus hallazgos mejoren los resultados del tratamiento para pacientes con diversos tipos de cáncer asociados con mutaciones ARID1A y tiene la intención de explorar esta traducción clínica en colaboración con la Universidad de California en San Diego.
