Nuevos artículos
Oxígeno para las células: un simple implante ayudó a reducir los niveles de azúcar sin medicamentos fuertes
Último revisado: 18.08.2025

Todo el contenido de iLive se revisa médicamente o se verifica para asegurar la mayor precisión posible.
Tenemos pautas de abastecimiento estrictas y solo estamos vinculados a sitios de medios acreditados, instituciones de investigación académica y, siempre que sea posible, estudios con revisión médica. Tenga en cuenta que los números entre paréntesis ([1], [2], etc.) son enlaces a estos estudios en los que se puede hacer clic.
Si considera que alguno de nuestros contenidos es incorrecto, está desactualizado o es cuestionable, selecciónelo y presione Ctrl + Intro.
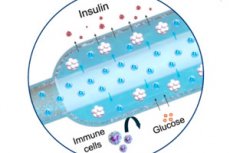
Un nuevo implante de oxígeno para el tratamiento de la diabetes tipo 1 se describió en Nature Communications: un generador electroquímico de oxígeno (iEOG) compacto que suministra O₂ continuamente a una macrocápsula con células secretoras de insulina. Este sistema permite la compactación de islotes aislados (hasta 60 000 IEQ/ml) y mantiene su viabilidad y secreción incluso en condiciones de baja concentración de oxígeno. En ratas con diabetes, el dispositivo implantado subcutáneamente mantuvo niveles normales de azúcar en sangre hasta tres meses, sin inmunosupresión. Las ratas de control, sin oxígeno, permanecieron hiperglucémicas.
Fondo
- El principal problema técnico es el oxígeno. En cuanto "ocultamos" las células tras la membrana y colocamos el dispositivo bajo la piel (de extracción cómoda y sencilla), les falta oxígeno: la difusión a través de la membrana y la zona poco vascularizada no satisface las necesidades de los voraces islotes. De ahí la muerte prematura, el bajo rendimiento y la necesidad de reducir considerablemente la siembra; de lo contrario, la cápsula se vuelve enorme.
- ¿Por qué es tan difícil físicamente? El oxígeno atraviesa los tejidos solo distancias muy cortas, y las células encapsuladas carecen de vasos propios; durante los primeros meses, viven únicamente gracias a la difusión pasiva. Cualquier engrosamiento de los materiales o compactación celular lleva rápidamente el centro de la cápsula a la hipoxia.
- ¿Qué has probado antes?
- Se fabricaron macrodispositivos rellenables con oxígeno (por ejemplo, βAir): contienen un depósito interno que se repone de oxígeno diariamente; se realizaron ensayos preclínicos y clínicos iniciales. Funciona, pero requiere mucho trabajo para el paciente.
- Se probaron donantes químicos de O₂ y materiales "transportadores" (compuestos perfluorocarbonados): son útiles, pero su efecto es breve y difícil de controlar. También surgieron estructuras de aire para acelerar la administración de O₂ en el espesor del gel.
- Se han mejorado las cápsulas y los lugares de implantación (membranas delgadas, prevascularización), pero sin una fuente externa de O₂ todavía se encuentran con los límites de densidad celular.
- ¿Qué vacío del rompecabezas llena el nuevo trabajo? Los autores de Nature Communications muestran un suministro continuo de oxígeno desde un minigenerador dentro del sistema de macroencapsulación: el dispositivo extrae agua de los tejidos y libera O₂ electroquímicamente, que se distribuye uniformemente a lo largo de la cápsula con células. La idea es dotar a la cápsula de su propio compresor de acuario para que pueda almacenar más células y mantenerlas vivas y en funcionamiento, incluso en una zona subcutánea poco oxigenada.
¿Por qué es esto necesario?
El trasplante de islotes o células beta es una de las vías más prometedoras para una "cura funcional" de la diabetes tipo 1. Sin embargo, existen dos obstáculos importantes:
- Inmunidad: generalmente requiere inmunosupresores de por vida;
- Falta de oxígeno: las cápsulas que protegen el sistema inmunitario aíslan simultáneamente las células de los vasos sanguíneos, y las células beta, voraces de O₂, se asfixian rápidamente. El nuevo trabajo aborda la segunda barrera: proporciona a la cápsula su propia fuente de oxígeno controlada.
Cómo funciona el implante
- Dos partes. En una caja de titanio se encuentra un minigenerador de oxígeno (iEOG), que extrae agua del líquido intersticial y libera O₂ mediante electrólisis. Junto a él, se encuentra una delgada cápsula lineal con células (similar a una salchicha larga), a través de la cual pasa un tubo permeable al gas: el oxígeno se absorbe uniformemente a lo largo de toda la cápsula. Entre las células y los tejidos hay una membrana semipermeable (electrospín + alginato): la glucosa y la insulina pasan a través de ella, pero las células inmunitarias no.
- Dimensiones: La segunda versión de iEOG tiene 13 mm de diámetro y 3,1 mm de grosor, con un peso aproximado de 2 g. Al combinarse con una cápsula, este sistema se puede insertar y extraer a través de una pequeña incisión, lo cual es importante para la seguridad.
- Productividad. El generador produce entre 1,9 y 2,3 cm³ de O₂/h y mantiene el flujo especificado durante meses e incluso años (en pruebas a largo plazo en solución salina, hasta 2,5 años). Tras la implantación en ratas, este nivel se mantuvo. Se calcula que dicho flujo cubre las necesidades de cientos de miles de islotes equivalentes, el orden de magnitud que necesita una persona.
Lo que mostraron los experimentos
- In vitro: Al 1% de O₂ (hipoxia severa), la oxigenación mantuvo la viabilidad y la secreción en agregados de INS-1 y en islotes humanos agrupados en una capa muy densa (60.000 IEQ/mL).
- In vivo (ratas). Tras la implantación subcutánea en un modelo de diabetes alogénica, el sistema iEOG normalizó la glucemia hasta por 3 meses sin inmunosupresión; los dispositivos sin oxígeno no tuvieron efecto. La histología alrededor del generador no mostró reacciones adversas significativas.
¿Por qué es esto importante para la clínica?
- Un paso hacia dimensiones realistas. Para administrar a un adulto una dosis de 300 a 770 mil IEQ, la cápsula debe estar compacta, ya que esto siempre ha estado limitado por el oxígeno. El suministro controlado de O₂ elimina el límite de densidad y permite que el dispositivo sea lo suficientemente compacto para una implantación real.
- Además de la comodidad. Anteriormente, probamos donantes químicos de oxígeno (peróxidos), que no funcionan a largo plazo y son incontrolables, así como depósitos de O₂ con recarga diaria a través de la piel, que resultan engorrosos e incómodos. En este caso, el oxígeno se suministra de forma constante y en dosis medidas, sin inyecciones.
Detalles técnicos que impresionan
- La fuente de agua es el tejido. iEOG absorbe el vapor del fluido intersticial a través de una “ventana” porosa, y luego se utiliza un ensamblaje clásico de membrana-electrodo (MEA) y un voltaje de 1,4–1,8 V para separar el agua en H₂ y O₂; los gases se eliminan a través de diferentes canales.
- Durabilidad. Tres dispositivos en solución salina funcionaron con corriente continua durante 11 meses, 2 años y 2,5 años sin degradación por el flujo de oxígeno; tras la implantación en ratas inmunodeficientes e inmunocompetentes, se mantuvo su rendimiento.
Limitaciones y "qué sigue"
Esto todavía es preclínico: ratas, alta densidad en la cápsula, suministro de oxígeno... todo está muy bien, pero aún quedan pruebas claves por delante:
- escalado a dosis humanas y plazos;
- fiabilidad y suministro de energía a los electroquímicos en el cuerpo humano durante años (la arquitectura de suministro de energía no se detalla en el artículo);
- minimización de la fibrosis alrededor de las cápsulas y estabilidad de la difusión;
- Pruebas en células madre beta y en modelos más parecidos a los humanos. Los autores comparan abiertamente su solución con enfoques previos y la presentan como una plataforma para cápsulas clínicamente traducibles.
Conclusión
Para que las células beta trasplantadas puedan vivir y funcionar sin inmunosupresores, necesitan respirar. El equipo de Cornell y sus colaboradores demostró que un minigenerador de oxígeno integrado en una cápsula lineal puede suministrar O₂ a las células durante el tiempo suficiente y de forma uniforme para que soporten una alta densidad y reduzcan el azúcar incluso en una zona subcutánea. El desarrollo clínico aún está lejos, pero la lógica de ingeniería es simple y atractiva: dar aire a las células donde falta.
