Nuevos artículos
Los científicos crean un compuesto "camaleónico" para tratar el cáncer cerebral resistente a los medicamentos
Último revisado: 14.06.2024

Todo el contenido de iLive se revisa médicamente o se verifica para asegurar la mayor precisión posible.
Tenemos pautas de abastecimiento estrictas y solo estamos vinculados a sitios de medios acreditados, instituciones de investigación académica y, siempre que sea posible, estudios con revisión médica. Tenga en cuenta que los números entre paréntesis ([1], [2], etc.) son enlaces a estos estudios en los que se puede hacer clic.
Si considera que alguno de nuestros contenidos es incorrecto, está desactualizado o es cuestionable, selecciónelo y presione Ctrl + Intro.
Un nuevo estudio dirigido por investigadores de la Universidad de Yale describe cómo un nuevo compuesto químico ataca los tumores cerebrales resistentes a los medicamentos sin dañar el tejido sano circundante.
Esta investigación, publicada en el Journal of the American Chemical Society, es un paso importante en el desarrollo de los llamados "compuestos camaleónicos" que podrían usarse para combatir una serie de tipos peligrosos de cáncer.
Los gliomas se desarrollan en aproximadamente 6,6 por 100.000 personas cada año y en 2,94 por 100.000 personas menores de 14 años. Con la excepción de las metástasis de otros cánceres que alcanzan el sistema nervioso central, los gliomas representan el 26% de los casos. Todos los tumores cerebrales (tumores cerebrales primarios) y el 81% de todos los tumores cerebrales malignos.
Durante décadas, los pacientes con glioblastoma han sido tratados con un medicamento llamado temozolomida. Sin embargo, la mayoría de los pacientes desarrollan resistencia a la temozolomida al cabo de un año. La tasa de supervivencia a cinco años para pacientes con glioblastoma es inferior al 5 %.
En 2022, el químico Seth Herzon de la Universidad de Yale y el oncólogo radioterapeuta Dr. Ranjit Bindra desarrollaron una nueva estrategia para tratar los glioblastomas de forma más eficaz. Crearon una clase de moléculas anticancerígenas llamadas compuestos camaleónicos que explotan un defecto en una proteína reparadora del ADN conocida como O6-metilguanina ADN metiltransferasa (MGMT).
Muchas células cancerosas, incluidos los glioblastomas, carecen de proteína MGMT. Nuevos compuestos camaleónicos están diseñados para dañar el ADN de las células tumorales que carecen de MGMT.
Los compuestos camaleónicos inician el daño del ADN al depositar lesiones primarias en el ADN, que con el tiempo se convierten en lesiones secundarias altamente tóxicas conocidas como enlaces cruzados entre cadenas. MGMT protege el ADN de los tejidos sanos reparando el daño primario antes de que pueda convertirse en enlaces cruzados mortales entre cadenas.
Para su nuevo estudio, los coautores Herzon y Bindra se centraron en su camaleón insignia, el KL-50.
“Utilizamos una combinación de estudios de química sintética y biología molecular para dilucidar las bases moleculares de nuestras observaciones anteriores, así como la cinética química que proporciona la selectividad única de estos compuestos”, dijo Herzon, profesor de química Milton Harris. En la Universidad de Yale. "Demostramos que KL-50 es único porque forma enlaces cruzados entre cadenas de ADN sólo en tumores con un defecto de reparación del ADN. Protege el tejido sano".
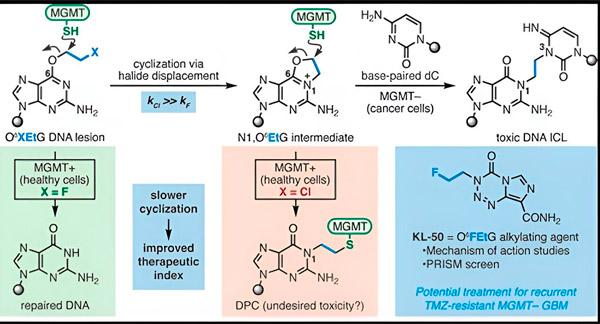
Fuente: Revista de la Sociedad Química Estadounidense (2024). DOI: 10.1021/jacs.3c06483
Esta es una diferencia significativa, enfatizaron los investigadores. Se han desarrollado otros compuestos anticancerígenos para desencadenar enlaces cruzados entre cadenas, pero no son selectivos para las células tumorales, lo que limita su utilidad.
El secreto del éxito del KL-50 reside en su duración de acción, señalaron los investigadores. KL-50 forma enlaces cruzados entre cadenas más lentamente que otros enlaces cruzados. Este retraso da a las células sanas tiempo suficiente para utilizar MGMT y evitar la formación de enlaces cruzados.
"Este perfil único demuestra su potencial para el tratamiento del glioblastoma resistente a los medicamentos, un área de gran necesidad clínica no cubierta", dijo Bindra, profesora Harvey y Kate Cushing de Radiología Terapéutica en la Facultad de Medicina de Yale. Bindra también es directora científica del Centro de Tumores Cerebrales de la Familia Chenevert en el Hospital Smilo.
Herzon y Bindra dijeron que su estudio destaca la importancia de considerar las tasas de modificación química del ADN y la reparación bioquímica del ADN. Creen que pueden utilizar esta estrategia para desarrollar tratamientos para otros cánceres que contienen defectos de reparación del ADN asociados a tumores específicos.
