Médico experto del artículo.
Nuevos artículos
Adenovirus respiratorios
Último revisado: 04.07.2025

Todo el contenido de iLive se revisa médicamente o se verifica para asegurar la mayor precisión posible.
Tenemos pautas de abastecimiento estrictas y solo estamos vinculados a sitios de medios acreditados, instituciones de investigación académica y, siempre que sea posible, estudios con revisión médica. Tenga en cuenta que los números entre paréntesis ([1], [2], etc.) son enlaces a estos estudios en los que se puede hacer clic.
Si considera que alguno de nuestros contenidos es incorrecto, está desactualizado o es cuestionable, selecciónelo y presione Ctrl + Intro.
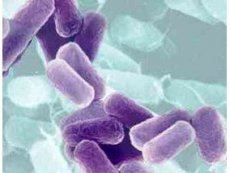
Los primeros representantes de la familia de los adenovirus fueron aislados en 1953 por W. Rowe (et al.) de las amígdalas y adenoides de niños, de ahí su nombre. La familia Adenoviridae se divide en dos géneros: Mastadenovirus (adenovirus de mamíferos) que incluye adenovirus de humanos (41 serovariantes), monos (24 serovariantes), así como de bovinos, caballos, ovejas, cerdos, perros, ratones y anfibios; y Aviadenovirus (adenovirus de aves) (9 serovariantes).
Los adenovirus carecen de supercápside. El virión tiene forma de icosaedro, un tipo de simetría cúbica, con un diámetro de 70-90 nm. La cápside consta de 252 capsómeros con un diámetro de 7-9 nm. Grupos de 9 capsómeros forman 20 caras equiláteras (180 capsómeros), y en sus esquinas hay 12 vértices que constan de 6 capsómeros (72 capsómeros). Dado que cada uno de los 180 capsómeros es adyacente a otros seis, se denomina hexón. A su vez, un hexón consta de tres subunidades con mm 120 kD. Cada uno de los 12 capsómeros de vértice es adyacente a cinco, por lo que se denomina pentón. Doce capsómeros de vértice del icosaedro llevan protuberancias filamentosas (fibras) de 8-30 nm de largo, que terminan en una cabeza de 4 nm de diámetro. El núcleo del virión contiene desoxirribonucleoproteína que consiste en una molécula de ADN genómico de doble cadena (20-25 MD), con una proteína terminal (55 kD) unida covalentemente a los extremos 5' de ambas cadenas, y dos proteínas principales: VII (18 kD) y V (48 kD). La desoxirribonucleoproteína es una estructura de 12 bucles, cuyos ápices se dirigen hacia las bases de las cápsides apicales, por lo que el núcleo del virión tiene una sección transversal en forma de flor. La proteína V se encuentra en la superficie externa. Además, las proteínas VI y X se encuentran en el núcleo. El genoma del adenovirus está representado por ADN lineal de doble cadena con mm 19-24 MD. Las cadenas de ADN están flanqueadas por repeticiones terminales invertidas, que permiten la formación de moléculas de anillo. Una proteína terminal hidrofóbica, que es necesaria para el inicio de la replicación del ADN, está unida covalentemente a los extremos 5' de ambas cadenas. El número de genes en una molécula de ADN no se ha determinado con precisión. En los adenovirus humanos, las proteínas representan entre el 86 % y el 88 % de la masa del virión. Su número total probablemente supere los 30, y su densidad varía de 5 a 120 kD. Las proteínas se designan con números romanos, de los cuales se han caracterizado del II al XIII. Actualmente, se han identificado en el genoma del adenovirus cuatro regiones de transcripción temprana (E1, E2, E3 y E4) y al menos cinco regiones de transcripción tardía (LI, L2, L3, L4 y L5).
Los productos de E1 inhiben el transporte de ARNm celular al citoplasma y su traducción. La región E2 codifica la síntesis de una proteína de unión al ADN que desempeña un papel importante en la replicación del ADN viral, la expresión génica temprana, el control del empalme y el ensamblaje del virión. Una de las proteínas tardías protege a los adenovirus del interferón. Los principales productos codificados por los genes tardíos incluyen proteínas que forman hexones, pentones, el núcleo del virión y una proteína no estructural que realiza tres funciones: a) participa en la formación de trímeros de hexones; b) transporta estos trímeros al núcleo; c) participa en la formación de viriones de adenovirus maduros. Se han identificado al menos 7 antígenos en el virión. El antígeno A (hexón) es específico del grupo y común a todos los adenovirus humanos. Según el antígeno B (base del pentón), todos los adenovirus humanos se dividen en tres subgrupos. El antígeno C (hilos, fibras) es específico del tipo. Según este antígeno, todos los adenovirus humanos se dividen en 41 serovariantes. Todos los adenovirus humanos, excepto las serovariantes 12, 18 y 31, presentan actividad hemaglutinante, mediada por un pentón (capsómero apical). En 1960, L. Rosen propuso la RTGA para identificar las serovariantes de adenovirus.
El ciclo de vida de los adenovirus durante la infección productiva consta de las siguientes etapas:
- adsorción en receptores específicos de la membrana celular utilizando la cabeza de fibra;
- penetración en la célula mediante el mecanismo de endocitosis mediada por receptores, acompañada de un "desnudo" parcial en el citoplasma;
- desproteinización final del genoma en la membrana nuclear y su penetración en el núcleo;
- síntesis de ARNm tempranos utilizando la ARN polimerasa celular;
- síntesis de proteínas específicas del virus temprano;
- replicación del ADN viral genómico;
- síntesis de ARNm tardíos;
- síntesis de proteínas virales tardías;
- morfogénesis de los viriones y su salida de la célula.
Los procesos de transcripción y replicación ocurren en el núcleo, el proceso de traducción, en el citoplasma, desde donde las proteínas son transportadas al núcleo. La morfogénesis de los viriones también ocurre en el núcleo y es multietapa: primero, los polipéptidos se ensamblan en estructuras multiméricas (fibras y hexones), luego se forman las cápsides, los viriones inmaduros y, finalmente, los viriones maduros. En los núcleos de las células infectadas, los viriones a menudo forman cúmulos cristalinos. En las últimas etapas de la infección, no solo los viriones maduros, sino también las cápsides inmaduras (sin ADN) se acumulan en los núcleos. La liberación de los viriones recién sintetizados va acompañada de la destrucción de las células. No todos ellos abandonan la célula en la que se sintetizan hasta un millón de nuevos viriones. Los viriones restantes interrumpen las funciones del núcleo y causan la degeneración celular.
Además de la forma productiva de infección, los adenovirus pueden causar una infección abortiva, en la que la reproducción viral se ve gravemente afectada en una etapa temprana o posterior. Además, algunas serovariantes de adenovirus humanos son capaces de inducir tumores malignos cuando se inoculan en diversos roedores. Según sus propiedades oncogénicas, los adenovirus se dividen en altamente oncogénicos, débilmente oncogénicos y no oncogénicos. Las capacidades oncogénicas están inversamente relacionadas con el contenido de pares GC en el ADN del adenovirus. El principal evento que conduce a la transformación celular (incluso en sus cultivos) es la integración del ADN viral en el cromosoma de la célula huésped. Los mecanismos moleculares de la acción oncogénica de los adenovirus siguen sin estar claros.
Los adenovirus no tienen propiedades oncogénicas en relación con los humanos.
Los adenovirus no se reproducen en embriones de pollo, pero se reproducen bien en cultivos de células primarias tripsinizadas y trasplantadas de diversos orígenes, provocando un efecto citopático característico (redondeo de las células y formación de racimos similares a uvas, degeneración en punta fina).
En comparación con otros virus humanos, los adenovirus son algo más estables en el ambiente externo, no se destruyen con disolventes grasos (no hay lípidos), no mueren a una temperatura de 50 °C y a un pH de 5,0-9,0; se conservan bien en estado congelado.
Características epidemiológicas. La fuente de infección es únicamente una persona enferma, incluyendo su forma latente. La infección se produce por gotitas en el aire, contacto doméstico, a través del agua de piscinas y por vía fecal-oral. El virus también puede penetrar los intestinos a través de la sangre. Las enfermedades de las vías respiratorias superiores y oculares son causadas por las serovariantes 1-8, 11, 19 y 21. Las serovariantes 1, 2, 3, 12, 18, 31, 40 y 41 causan gastroenteritis en niños de 6 meses a 2 años y adenitis mesentérica. Las serovariantes 1, 2, 5 y 6 se detectan con frecuencia en formas latentes de infección.
No existen datos sobre la capacidad de los adenovirus animales para causar enfermedades en humanos y, a la inversa, de los adenovirus humanos en animales. Los adenovirus causan enfermedades esporádicas y brotes epidémicos locales. El brote más grande en nuestro país afectó a 6.000 personas.
Síntomas de la infección por adenovirus
El período de incubación es de 6 a 9 días. El virus se multiplica en las células epiteliales de las vías respiratorias superiores y la mucosa ocular. Puede penetrar los pulmones, afectar los bronquios y los alvéolos, y causar neumonía grave. Una propiedad biológica característica de los adenovirus es su tropismo hacia el tejido linfoide.
Las enfermedades adenovirales se caracterizan por una inflamación febril y catarral de la mucosa de las vías respiratorias y los ojos, acompañada de un aumento del tejido linfoide submucoso y de los ganglios linfáticos regionales. Con mayor frecuencia, se presentan en forma de amigdalitis, faringitis, bronquitis, neumonía atípica, síndrome pseudogripal y fiebre faringoconjuntival. En algunos casos, la conjuntivitis acompaña a la enfermedad adenoviral, mientras que en otros es su síntoma principal.
Así, las enfermedades adenovirales se caracterizan por el predominio de síndromes respiratorio, conjuntival o intestinal. Al mismo tiempo, el virus puede causar una infección latente (asintomática) o crónica con persistencia prolongada en los tejidos de las amígdalas y adenoides.
La inmunidad postinfección es duradera y estable, pero específica para cada tipo de virus; no existe inmunidad cruzada. La inmunidad se basa en anticuerpos neutralizantes del virus y células de memoria inmunitaria.
Diagnóstico de laboratorio de la infección por adenovirus
- Detección de antígenos virales en células afectadas mediante métodos de inmunofluorescencia o IFM.
- Aislamiento del virus. El material de estudio son secreciones nasofaríngeas y conjuntivales, sangre y heces (el virus puede aislarse no solo al inicio de la enfermedad, sino también entre el séptimo y el decimocuarto día). Para aislar el virus, se utilizan cultivos celulares primarios tripsinizados (incluidos los diploides) de embriones humanos, sensibles a todos los serotipos de adenovirus. Los virus se detectan por su efecto citopático y mediante el antígeno de unión al complemento (CBA), ya que todos comparten un antígeno de unión al complemento. La identificación se realiza mediante antígenos específicos de cada tipo utilizando RTGA y RN en el cultivo celular.
- Detección del aumento del título de anticuerpos en sueros de pacientes pareados mediante el RSC. La determinación del aumento del título de anticuerpos específicos de tipo se realiza con cepas serológicas de adenovirus estándar en RTGA o RN en cultivo celular.


 [
[