Médico experto del artículo.
Nuevos artículos
Amiloidosis hepática
Último revisado: 29.06.2025

Todo el contenido de iLive se revisa médicamente o se verifica para asegurar la mayor precisión posible.
Tenemos pautas de abastecimiento estrictas y solo estamos vinculados a sitios de medios acreditados, instituciones de investigación académica y, siempre que sea posible, estudios con revisión médica. Tenga en cuenta que los números entre paréntesis ([1], [2], etc.) son enlaces a estos estudios en los que se puede hacer clic.
Si considera que alguno de nuestros contenidos es incorrecto, está desactualizado o es cuestionable, selecciónelo y presione Ctrl + Intro.
La amiloidosis suele ser una patología sistémica y general caracterizada por la acumulación de amiloide (una glucoproteína específica) en los tejidos y la consiguiente alteración de la función orgánica normal. La amiloidosis hepática es mucho menos frecuente que la renal y la esplénica [ 1 ], pero casi siempre acompaña a un daño sistémico en el organismo. Ninguna de las técnicas de imagen existentes puede demostrar específicamente la presencia de amiloide. Incluso cuando se sospecha clínica y radiológicamente, el diagnóstico de amiloidosis depende de una biopsia de tejido para confirmar la presencia de depósitos de amiloide. [ 3 ] El tratamiento es complejo, integral e incluye medidas inmunosupresoras y sintomáticas. En casos graves, puede ser necesario un trasplante de hígado.
Epidemiología
El éxito del tratamiento depende directamente del diagnóstico oportuno de la enfermedad, que provoca la formación de un complejo proteína-polisacárido (amiloide) en diversos órganos y el hígado. Como demuestra la práctica, la amiloidosis es difícil de presumir o sospechar, aunque es posible identificarla y confirmarla. De hecho, en más del 80% de los casos no diagnosticados, la enfermedad está clínicamente enmascarada por una patología hepática. El método diagnóstico más eficaz es la biopsia.
La amiloidosis hepática es un problema menos frecuente en comparación con la amiloidosis renal. Asimismo, todos los casos de lesiones hepáticas se acompañan de lesiones en otros órganos. Con mayor frecuencia, la patología afecta predominantemente las partes estructurales de la tríada hepática, lo que determina la mínima e inespecificidad de la sintomatología. El cuadro clínico y morfológico de la deficiencia hepatocelular y la hipertensión portal se manifiesta en forma difusa e intralobulillar.
La biopsia hepática está justificada cuando existe hepatomegalia sin síntomas hepáticos previos y en ausencia de síndrome nefrótico.
La afectación hepática difusa se observa en aproximadamente el 25% de los casos y en el 75% de los pacientes solo se ven afectados los tractos portales.
La amiloidosis primaria afecta al hígado en el 90% de los casos, mientras que la amiloidosis secundaria afecta al hígado sólo en el 47% de los casos.
La afectación hepática aislada es extremadamente rara. Los riñones (aproximadamente el 93 % de los casos), el bazo (72 %), el corazón (57 %), el páncreas (36 %), las glándulas suprarrenales (29 %), los intestinos y los pulmones (21 % cada uno) suelen verse afectados simultáneamente.
Las mujeres contraen la enfermedad con casi el doble de frecuencia que los hombres. La esperanza de vida promedio de los pacientes con amiloidosis es de 52 a 64 años.
Causas amiloidosis hepática
La amiloidosis se produce mediante la formación y acumulación de un complejo polisacárido-proteína (amiloide) en el tejido hepático. El problema de la aparición de la lesión primaria no se ha estudiado lo suficiente hasta la fecha. En cuanto a la patología secundaria, su aparición suele asociarse con las siguientes enfermedades:
- Procesos infecciosos crónicos (tuberculosis, sífilis, actinomicosis);
- Procesos inflamatorios purulentos (endocarditis microbiana, osteomielitis, enfermedad bronquiectásica, etc.);
- Enfermedades malignas (leucemia, cáncer visceral, linfogranulomatosis).
La forma reactiva de la amiloidosis se presenta en pacientes con aterosclerosis concomitante, enfermedades reumatológicas (enfermedad de Bechterew, artritis reumatoide), psoriasis, procesos inflamatorios crónicos y multisistémicos (incluida la sarcoidosis). Los principales factores de riesgo son: predisposición hereditaria, trastornos de la inmunidad celular e hiperglobulinemia.
Patogenesia
Existen diversas hipótesis sobre el origen de la amiloidosis hepática. La mayoría de los especialistas se adhieren a la teoría de la disproteinosis, la naturaleza inmunológica y mutacional de la enfermedad, así como la génesis celular local. Esta teoría incluye cambios en las reacciones que operan a nivel celular (formación de precursores fibrilares de amiloide por un complejo de macrófagos), aunque el amiloide se forma y se acumula fuera de las estructuras celulares.
La versión de la disproteinosis se basa en que el amiloide es producto de un metabolismo proteico inadecuado. El vínculo patogénico fundamental del problema reside en la disproteinemia y la hiperfibrinogenemia, que conducen a la acumulación de fracciones gruesas de proteínas y paraproteínas dispersas en el plasma.
Según la versión inmunológica, la formación de amiloide se debe a una reacción antígeno-anticuerpo, en la que los productos de degradación tisular o las proteínas extrañas actúan como antígenos. La acumulación de amiloide se encuentra principalmente en la zona de formación de anticuerpos y la presencia excesiva de antígenos.
La versión más plausible para los científicos es la teoría de la mutación, que tiene en cuenta diversos factores mutagénicos que pueden provocar anomalías en la síntesis de proteínas.
El amiloide es una hipoproteína compleja compuesta por proteínas globulares y fibrilares combinadas con polisacáridos. Las acumulaciones de amiloide afectan la íntima y la adventicia de la red vascular, el estroma de los órganos parenquimatosos, la estructura glandular, etc. Las acumulaciones de amiloide no causan daño funcional. Pequeñas acumulaciones no causan trastornos funcionales, pero con una presencia intensa de amiloide, el hígado aumenta de volumen, altera la apariencia del órgano y provoca una disfunción.
La amiloidosis hepática se caracteriza por el depósito de fibrillas amiloides en el espacio de Dysse, que suele comenzar en la región periportal, aunque a veces es centrolobulillar y también puede depositarse en la vasculatura hepática. [ 4 ], [ 5 ] En casos graves, el depósito de amiloide provoca atrofia por presión de los hepatocitos, lo que impide el paso de la bilis, resultando en colestasis, o puede bloquear los sinusoides, resultando en hipertensión portal. [ 6 ], [ 7 ], [ 8 ]
Síntomas amiloidosis hepática
El cuadro clínico de la amiloidosis hepática es diverso, depende de la intensidad de la acumulación de amiloide, de sus características bioquímicas, de la duración del proceso patológico, del grado de daño a los órganos y de la violación de su estado funcional.
En la fase latente de la amiloidosis, cuando las acumulaciones de amiloide en el hígado solo pueden detectarse mediante examen microscópico, los primeros signos de la enfermedad son inexistentes. Con el desarrollo posterior y el creciente déficit funcional del órgano, la sintomatología progresa.
El hígado se engrosa y agranda gradualmente. La palpación permite palpar bordes del órgano alterados, pero lisos e indoloros. En raras ocasiones, la patología se acompaña de dolor en la zona subcostal derecha, dispepsia, esplenomegalia, coloración amarillenta de la piel, las mucosas y las escleróticas, y síndrome hemorrágico.
Los síntomas más característicos de la amiloidosis hepática: [ 9 ], [ 10 ]
- La acumulación de amiloide en el hígado causa hepatomegalia en el 33-92% de los pacientes;
- ictericia leve
- Hipertensión portal;
- Colestasis moderada a grave.
Dado que la amiloidosis rara vez afecta solo a un órgano, suele presentarse sintomatología adicional:
- Cuando hay daño renal se desarrolla síndrome nefrótico e hipertensión arterial con posterior insuficiencia renal, edema, a veces trombosis de la vena renal, leucocituria, hematuria, hipoproteinemia, azotemia, etc.
- Cuando se afecta el corazón, se desarrolla un estado similar a la miocardiopatía restrictiva (alteraciones del ritmo, cardiomegalia, aumento del déficit cardíaco, debilidad y disnea, edema, con menor frecuencia, acumulación de líquido en la cavidad abdominal y pleural, pericarditis);
- Si se afecta el tracto digestivo, pueden aparecer macroglosia, debilidad y peristaltismo esofágico, náuseas y ardor de estómago, estreñimiento o diarrea, etc.
- Cuando el páncreas se ve afectado, se presentan los síntomas de pancreatitis crónica;
- Si está afectado el mecanismo musculoesquelético se desarrollan poliartritis simétrica, síndrome del túnel carpiano, miopatías y si está afectado el sistema nervioso se encuentran polineuropatías, parálisis, presión arterial baja ortostática, aumento de la sudoración, demencia.
Si la reacción patológica se extiende a la piel, aparecen numerosas placas cerosas en la cara, el cuello y los pliegues cutáneos. Es posible que se presente un cuadro de neurodermatitis, fiebre escamosa roja y esclerodermia.
La combinación de múltiples lesiones amiloides y la variedad de sintomatología hacen que la identificación de la amiloidosis hepática sea mucho más difícil y requiera un diagnóstico exhaustivo y exhaustivo.
Formas
Según la clasificación de la OMS se distinguen cinco tipos de amiloidosis:
- AL (primaria);
- AA (secundaria);
- ATTR (sistémica hereditaria y senil);
- Aβ2M (en pacientes en hemodiálisis);
- AIAPP (en pacientes con diabetes mellitus insulinodependiente);
- AB (para la enfermedad de Alzheimer);
- AANF (amiloidosis auricular senil).
Existe una amiloidosis local del hígado, pero más a menudo se trata de una lesión sistémica, en la que el proceso patológico también involucra los riñones, el corazón, el bazo, el sistema nervioso, así como otros órganos y tejidos.
Complicaciones y consecuencias
La amiloidosis sistémica conduce gradualmente al desarrollo de procesos patológicos agudos que, a su vez, pueden causar la muerte. Entre las complicaciones más comunes y potencialmente mortales se encuentran las siguientes:
- Patologías infecciosas (bacterianas, virales) frecuentes, incluidas neumonías, pielonefritis, glomerulonefritis;
- Insuficiencia hepática y renal crónica;
- Insuficiencia cardíaca crónica (puede preceder al infarto de miocardio);
- Accidentes cerebrovasculares hemorrágicos.
La trombosis venosa se produce como resultado de la acumulación y el depósito de proteínas en las paredes venosas. La luz de los vasos afectados se estrecha y se produce insuficiencia orgánica. Con el tiempo, en el contexto de una hiperproteinemia prolongada, el vaso puede obstruirse por completo. Cualquier complicación puede tener un desenlace desfavorable: la muerte.
Diagnostico amiloidosis hepática
Si se sospecha amiloidosis hepática, se realizan medidas diagnósticas tras consultas obligatorias con gastroenterólogos, terapeutas, reumatólogos, cardiólogos, dermatólogos, neurólogos y urólogos. Es importante evaluar exhaustivamente la anamnesis y las manifestaciones clínicas, y realizar un diagnóstico completo de laboratorio e instrumental.
Las pruebas incluyen necesariamente análisis de orina y sangre. En la amiloidosis hepática, se suele encontrar una combinación de leucocituria con proteinuria y cilindruria, e hipoproteinemia, con hiperlipidemia, anemia, hiponatremia e hipocalcemia, y disminución del recuento plaquetario. Se detectan paraproteínas en la electroforesis de orina y suero.
Los diagnósticos instrumentales incluyen:
- EKG, Eco;
- Ecografía abdominal;
- Radiografías del estómago, esófago;
- Irrigografía, rayos X con bario;
- Endoscopia.
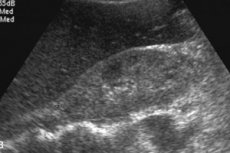
Los hallazgos radiológicos de la amiloidosis hepática incluyen hepatomegalia inespecífica, aumento de la ecogenicidad en la ecografía o de la densidad en la tomografía computarizada (TC) y aumento de la intensidad de la señal T1 en la resonancia magnética (RM). [ 12 ] La gammagrafía con indicadores relacionados con el Tc-99m muestra una captación heterogénea, pero es inespecífica. [ 13 ], [ 14 ] Se ha demostrado que el GC aumenta la rigidez hepática medida por elastografía; [ 15 ], [ 16 ], [ 17 ] pero hay pocos informes de casos. La elastografía por resonancia magnética (ERM) es actualmente el método no invasivo más preciso para detectar y estadificar la fibrosis hepática, [ 18 ], [ 19 ] La ERM es útil para detectar la progresión, la respuesta al tratamiento y predecir la descompensación hepática en pacientes con fibrosis hepática. [ 20 ]
La amiloidosis hepática mediante ecografía es difícil de detectar: se detecta un agrandamiento del órgano, siendo la hepatomegalia más específica superior a 15 cm. Bajo control ecográfico, se realiza una biopsia, que se convierte en un indicador determinante para el diagnóstico. Con una aguja especial, se extrae una pequeña muestra de tejido hepático, se tiñe con un tinte especial y se examina al microscopio, lo que permite visualizar directamente los depósitos de amiloide.
El diagnóstico definitivo se realiza únicamente tras la detección de fibrillas amiloides en el tejido hepático y otros órganos. El tipo de amiloidosis genéticamente determinado se determina mediante un minucioso examen genético-médico del árbol genealógico.
Diagnóstico diferencial
Se debe sospechar amiloidosis en todos los pacientes con una combinación de proteinuria renal, miocardiopatía restrictiva, neuropatía autonómica o periférica y hepatomelia, incluso en ausencia de paraproteína monoclonal. Verificar el tipo de amiloidosis es fundamental, ya que el tratamiento de lesiones de diferentes etiologías es muy diverso.
El diagnóstico histológico implica la tinción con rojo Congo seguida de un examen microscópico con luz polarizada. Se recomienda biopsiar varias muestras de tejido simultáneamente. Si la tinción es positiva, se realiza un análisis inmunohistoquímico con anticuerpos monoclonales contra proteínas precursoras para identificar el tipo de amiloide.
El análisis de ADN se realiza para diferenciar entre la amiloidosis primaria y diferentes variantes de la amiloidosis genética. Las fibrillas de amiloide pueden aislarse de muestras de biopsia y secuestrarse en aminoácidos individuales.
Estudios adicionales para determinar la discrasia de células plasmáticas:
- Electroforesis de proteínas séricas de sangre y orina;
- Inmunoensayo para cadenas ligeras libres;
- Inmunofijación (inmunotransferencia) de proteínas séricas;
- Aspiración de médula ósea y trepanobiopsia.
El diagnóstico de la amiloidosis hepática es un proceso largo y laborioso, que requiere una mayor atención de los especialistas y un equipamiento de calidad en las clínicas y los laboratorios.
¿A quién contactar?
Tratamiento amiloidosis hepática
Las medidas de tratamiento están dirigidas a reducir la concentración de proteínas amiloides preexistentes en la sangre (eliminando la causa de la amiloidosis) y apoyar la función hepática adecuada.
La amiloidosis secundaria requiere bloquear el proceso inflamatorio (en patologías infecciosas crónicas y autoinmunes). En las enfermedades autoinmunes, se recomienda el uso de citostáticos. Para eliminar los procesos infecciosos crónicos, la zona inflamatoria suele extirparse quirúrgicamente. Con frecuencia, este enfoque puede detener la progresión de la amiloidosis y mejorar la función hepática.
La amiloidosis primaria requiere el uso de medicamentos quimiopreventivos y, a veces, trasplante de médula ósea.
Las pautas actuales recomiendan la combinación de ciclofosfamida, bortezomib, dexametasona (CyBorD) y daratumumab como terapia de primera línea en pacientes con diagnóstico reciente de AL.
El bortezomib es un inhibidor del proteasoma. Los proteasomas participan en la reducción de la proteotoxicidad y la regulación de las proteínas que controlan la progresión celular y la apoptosis. Las células plasmáticas que generan amiloide son particularmente sensibles a la inhibición del proteasoma, ya que dependen de este para reducir los efectos tóxicos de las cadenas ligeras y prevenir la apoptosis.
Daratumumumab es un anticuerpo monoclonal (mAb) que se une a CD38, una glucoproteína transmembrana expresada en la superficie de las células plasmáticas, induciendo apoptosis. Es el único fármaco específicamente aprobado para el tratamiento de la amiloidosis AL cuando se utiliza con CyBorD. La eficacia de CyBorD-daratumumumab es muy alta, con un 78 % de pacientes que lograron una respuesta hematológica significativa (definida como una respuesta completa o una respuesta parcial muy buena). La mediana de supervivencia en el pequeño grupo de pacientes que recibieron CyBorD (n = 15) fue de 655 días, en comparación con los 178 días de los pacientes que recibieron otro tratamiento basado en melfalán-dexametasona (n = 10). 4
Sin embargo, estas terapias tienen numerosos efectos secundarios, incluida la cardiotoxicidad, que lleva a la necesidad de reducir la dosis o suspender el tratamiento y al uso de otras estrategias terapéuticas menos efectivas pero más tolerables.
Isatuximab, un anticuerpo monoclonal contra CD38 similar a daratumumab, se está estudiando para el tratamiento de la discrasia de células plasmáticas subyacente a la AL.
Tres anticuerpos monoclonales, birtamimab, CAEL-101 y AT-03, se están estudiando para la eliminación de fibrillas amiloides de órganos enfermos. Los resultados de estos estudios ofrecerán evidencia directa de la hipótesis de que la eliminación de las fibrillas de deposición de cadenas ligeras de los órganos mejora la función orgánica. [ 21 ]
Para apoyar la función hepática, se recetan medicamentos a base de ácido ursodesoxicólico (por ejemplo, Ursosan). El ácido ursodesoxicólico ayuda a estabilizar las membranas celulares, reduce el efecto adverso de los ácidos grasos tóxicos en la estasis biliar provocada por los depósitos de amiloide y ayuda a restablecer el flujo biliar normal.
Además, se realiza terapia sintomática y apoyo al funcionamiento de otras estructuras vitales como el sistema nervioso, corazón, riñones, etc. La terapia de soporte para pacientes con amiloidosis hepática incluye diversos aspectos clínicos, entre ellos el tratamiento de la insuficiencia cardíaca, arritmias, trastornos de la conducción, tromboembolismo y la presencia concomitante de estenosis aórtica.
Otros tratamientos dependen del tipo de amiloidosis y de las partes del cuerpo afectadas. Los tratamientos pueden incluir: [ 22 ]
- Medicamentos que alivian los síntomas, como analgésicos, medicamentos para las náuseas o medicamentos que reducen la hinchazón (diuréticos);
- Medicamentos para reducir el amiloide;
- Diálisis renal;
- Trasplante de hígado.
El hígado produce el 95% de TTR (transtiretina, una proteína involucrada en el transporte de tiroxina (T4) y proteína de unión al retinol. La transtiretina se sintetiza principalmente en el hígado y es rica en cadenas beta que tienden a agregarse en fibrillas amiloides insolubles) medida en suero. Por lo tanto, el trasplante de hígado se ha sugerido históricamente (desde 1990) como terapia de primera línea para eliminar la fuente principal de TTR amiloidogénica en pacientes con la forma familiar (ATTRv), mientras que no está indicado en la forma ATTR-wt. El trasplante de hígado de pacientes jóvenes en las primeras etapas de la enfermedad se asocia con una alta tasa de supervivencia a 20 años. El trasplante de hígado parece ser más efectivo en algunas mutaciones y menos efectivo en otras, como V122I (asociada con miocardiopatía). El trasplante combinado de hígado y corazón también es posible en pacientes jóvenes con ATTRv y miocardiopatía, y los datos de la literatura sobre un pequeño grupo de pacientes sugieren que esta combinación tiene un mejor pronóstico que el trasplante de corazón solo.
Los pacientes con amiloidosis hepática tienen contraindicado el uso de glucósidos cardíacos y antagonistas del calcio como diltiazem o verapamilo, ya que pueden acumularse en el amiloide. Los inhibidores de la ECA y los betabloqueantes se utilizan con precaución.
En caso de hipotensión ortostática, se prescriben mineralocorticoides o glucocorticosteroides, teniendo en cuenta que pueden causar descompensación de la insuficiencia cardíaca. El alfa-adrenomimético midodrina (Gutron) también se utiliza con precaución.
Los anticonvulsivos y antidepresivos son apropiados en las neuropatías.
En algunos casos de amiloidosis hepática, los médicos deben considerar el trasplante del órgano.
Prevención
Debido a la falta de información sobre la patogénesis de la amiloidosis hepática, los especialistas no pueden desarrollar una prevención específica. Por lo tanto, los principales esfuerzos se centran en la detección y el tratamiento oportunos de cualquier patología crónica que pueda desencadenar el desarrollo del trastorno. Si existen casos de amiloidosis de cualquier localización en la familia, se recomienda realizar visitas médicas sistemáticas para exámenes en el dispensario.
En general, las medidas preventivas se reducen a la eliminación oportuna de las enfermedades infecciosas, especialmente aquellas que tienden a cronificarse. Se trata de prevenir el desarrollo de tuberculosis, infecciones pulmonares, etc. Es importante la detección oportuna y el tratamiento adecuado de las infecciones estreptocócicas, que pueden causar formas crónicas de procesos inflamatorios autoinmunes. Nos referimos a la escarlatina, la amigdalitis estreptocócica, etc.
Si el paciente ya tiene una enfermedad autoinmune, entonces debe consultar sistemáticamente con un médico, observar la actividad de la patología, aplicar los medicamentos necesarios según lo prescrito por el médico, ajustar las dosis según las indicaciones.
Pronóstico
El pronóstico para los pacientes con amiloidosis hepática es desfavorable. La enfermedad progresa de forma lenta pero continua, lo que finalmente causa disfunción de los órganos afectados y un desenlace fatal, en particular debido a insuficiencia orgánica.
Los pacientes con patología sistémica fallecen principalmente como consecuencia del desarrollo de insuficiencia renal crónica, aunque en algunos casos la hemodiálisis o la diálisis peritoneal ambulatoria continua mejoran el pronóstico. La tasa de supervivencia de los pacientes en hemodiálisis, independientemente de su tipo, es comparable a la de las personas con otras patologías sistémicas y diabetes mellitus.
La principal causa de muerte durante la hemodiálisis es el desarrollo de complicaciones del sistema cardiovascular.
El trasplante de hígado se ha considerado durante mucho tiempo uno de los principales métodos de tratamiento de la enfermedad, y las tasas de supervivencia más optimistas se observan en pacientes menores de 50 años (siempre que el proceso patológico sea de corta duración y el índice de masa corporal sea normal). Los pacientes con amiloidosis hepática combinada con neuropatía periférica tienen un pronóstico algo peor.

