Médico experto del artículo.
Nuevos artículos
Aspectos genéticos y metabólicos de la patogénesis de la artrosis
Último revisado: 08.07.2025

Todo el contenido de iLive se revisa médicamente o se verifica para asegurar la mayor precisión posible.
Tenemos pautas de abastecimiento estrictas y solo estamos vinculados a sitios de medios acreditados, instituciones de investigación académica y, siempre que sea posible, estudios con revisión médica. Tenga en cuenta que los números entre paréntesis ([1], [2], etc.) son enlaces a estos estudios en los que se puede hacer clic.
Si considera que alguno de nuestros contenidos es incorrecto, está desactualizado o es cuestionable, selecciónelo y presione Ctrl + Intro.
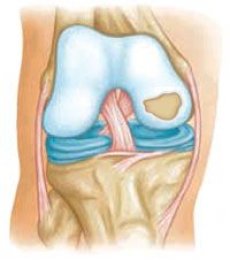
El papel de los factores mecánicos en la patogénesis de la osteoartritis es innegable, pero existen pruebas convincentes de que algunas formas de osteoartritis se heredan según las leyes de Mendel. Las osteoartropatías hereditarias se pueden dividir en:
- osteoartritis generalizada primaria (PGAO),
- artropatías asociadas a cristales,
- osteoartritis prematura debida a osteocondrodisplasia hereditaria.
En 1803, W. Heberden describió "nódulos ligeramente densos, del tamaño de un guisante pequeño" en la superficie dorsal de las articulaciones interfalángicas distales de las manos. Este síntoma, según el autor, distingue la osteoartritis de otras enfermedades articulares, como la gota. J. Hayagarth (1805) amplió la descripción clínica de los nódulos de Heberden, señalando su frecuente asociación con la artrosis en otras localizaciones. Posteriormente, Bouchard describió nódulos similares en la superficie dorsal de las articulaciones interfalángicas proximales de las manos. Utilizando los términos "nódulos de Heberden y de Bouchard", W. Osier distinguió entre "artritis hipertrófica" y "artritis deformante" (1909). En 1953, RM Stecher y H. Hersh descubrieron la prevalencia de los nódulos de Heberden en familiares y concluyeron que se heredan de forma autosómica dominante. Estudios posteriores al descubrimiento de RM Stecher y H. Hersh revelaron una asociación entre los nódulos de Heberden y Bouchard y lesiones degenerativas en otras articulaciones. Con base en datos de exámenes clínicos y la tipificación del HLA, JS Lawrence (1977) y JS Lawrence et al. (1983) sugirieron la presencia de herencia poligénica en lugar de un defecto genético único.
El espectro fenotípico de la osteoartritis hereditaria varía ampliamente, desde formas leves que se manifiestan clínicamente solo al final de la edad adulta hasta formas muy graves que se manifiestan en la infancia. Tradicionalmente, todas estas formas se han clasificado como osteoartritis secundaria. Actualmente, se sabe que algunos de estos fenotipos son causados por mutaciones en genes que codifican macromoléculas de la matriz extracelular (MEC) del cartílago articular, que alteran la integridad de la matriz cartilaginosa y la regulación de la proliferación de condrocitos y la expresión génica. Estas enfermedades hereditarias representan un subgrupo específico de osteoartritis, distinto de la osteoartritis secundaria.
Diferencias entre artrosis hereditaria y secundaria (según Williams CJ y Jiménez SA, 1999)
Osteoartritis hereditaria |
Artrosis secundaria |
|
Etiología |
Mutación de genes expresados en el cartílago articular |
Diversas enfermedades hereditarias y adquiridas |
Patogenesia |
Daño a los componentes estructurales o funcionales del cartílago articular |
Manifestaciones secundarias de la enfermedad, que no siempre afecta sólo al cartílago articular. |
Tratamiento |
La terapia genética podría ser posible para corregir el defecto genético |
Tratamiento de la enfermedad subyacente |
La condrodisplasia/osteocondrodisplasia es un grupo de enfermedades clínicamente heterogéneas que se caracterizan por anomalías en el crecimiento y desarrollo del cartílago articular y la placa de crecimiento. Algunas EC/OCD conducen al desarrollo temprano de osteoartritis, que se caracteriza clínicamente por una evolución grave. Entre ellas, se pueden distinguir las siguientes enfermedades:
- displasia espondiloepifisaria (SED),
- Síndrome de Stickler,
- displasia de Knista,
- displasia epifisaria múltiple (MED),
- condrodisplasia metafisaria (MCD),
- Algunas displasias otoespondilometaepifisarias (OSMED).
Displasias hereditarias caracterizadas por osteoartritis de aparición temprana (según Williams CJ y Jiménez SA, 1999)
Enfermedad |
Lugar |
Tipo de herencia |
Gen mutado |
Tipo de mutación |
OA temprana con SED de inicio tardío (OAR)* |
12q13.1-q13.2 |
INFIERNO |
COLUMNA 2A, |
Sustitución, inserción y eliminación de bases |
Síndrome de Stickler (STL1) |
12q13.1-q13.2 |
INFIERNO |
COL2A1 |
Sustitución de la base, inserción |
Síndrome de Stickler (STL2) |
6р21.3 |
INFIERNO |
REAJUSTE SALARIAL |
Inserción, eliminación |
Síndrome de Stickler |
1p21 |
INFIERNO |
REAJUSTE SALARIAL |
Reemplazo de la base |
Síndrome de Wagner |
12q13.1-q13.2 |
INFIERNO |
COUA, |
Reemplazo de la base |
OSMED |
6р21.3 |
Arkansas |
REAJUSTE SALARIAL |
Reemplazo de la base |
Síndrome de Marshall |
1p21 |
INFIERNO |
REAJUSTE SALARIAL |
Insertar |
Displasia de Knista |
12q13.1-q13.2 |
INFIERNO |
REAJUSTE SALARIAL |
Inserción, eliminación |
M3fl(EDM1) |
19р13.1 |
INFIERNO |
COMP |
Reemplazo de la base |
MED (EDM 2) |
1р32.2-рЗЗ |
INFIERNO |
REAJUSTE SALARIAL |
Insertar |
MCDS |
6q21-q22.3 |
INFIERNO |
REAJUSTE SALARIAL |
Sustitución y eliminación de bases |
MCDJ Jansen |
Zр21.2-р21.3 |
INFIERNO |
PTHR, |
Reemplazo de la base |
*Los símbolos del locus se dan entre paréntesis; AD - autosómico dominante; AR - autosómico recesivo.
Displasia espondiloepifisaria
Las displasias espondiloepifisarias (SED) incluyen un grupo heterogéneo de enfermedades con herencia autosómica dominante, caracterizadas por un desarrollo anormal del esqueleto axial y cambios graves en las epífisis de los huesos tubulares largos, que a menudo causan enanismo. La SED suele presentar una evolución clínica grave, acompañada de acortamiento del cuerpo y, en menor medida, de las extremidades.
En las formas de SED que se manifiestan a una edad más avanzada, el fenotipo suele presentar pocos cambios y puede no manifestarse clínicamente hasta la adolescencia, cuando se desarrolla osteoartrosis grave. La deformidad de la columna lumbar puede manifestarse como estrechamiento de los discos intervertebrales, platispondilia y cifoescoliosis leve. También se detectan anomalías de las epífisis en las articulaciones periféricas y cambios degenerativos tempranos en ellas. El signo más constante de daño articular periférico es el aplanamiento de las superficies articulares de las articulaciones del tobillo y la rodilla, así como el aplanamiento del surco intercondíleo del fémur. Las anomalías de la cabeza y el cuello del fémur se detectan a menudo con el desarrollo de osteoartrosis de la articulación de la cadera, que se manifiesta en la adolescencia.
Dado que el colágeno tipo II es el componente principal de la matriz extracelular (MEC) del cartílago hialino, se ha sugerido que el gen que lo codifica, COL1A, es la causa del SED. La primera descripción de una relación genética entre el fenotipo de la osteoartritis temprana asociada al SED de inicio tardío y el gen del procolágeno tipo II, COL 2 A, data de 1989 y 1990. El primer informe de una mutación en COL 2 A en familiares con osteoartritis temprana asociada al SED de inicio tardío se refería a la sustitución de bases Arg519>Cys. Hasta la fecha, se han identificado cuatro familias más con mutaciones similares. En miembros de otra familia con OA temprana y SED leve, se encontró la sustitución de bases Arg75>Cys, aunque el fenotipo de SED en los miembros de esta familia no es similar al fenotipo de la familia con una sustitución de arginina por cisteína en la posición 519. También se encontraron otras mutaciones COL 2 A-Gly976>Ser y Gly493>Ser en miembros de familias con SED. J. Spranger et al. (1994) utilizaron el término «colagenopatía tipo 11» para describir enfermedades hereditarias del tejido cartilaginoso con una mutación primaria en el gen del procolágeno tipo II, COL1A.
Forma clásica del síndrome de Stickler
Fue descrito por primera vez en 1965 por GB Stickler y colegas, quienes lo llamaron artrooftalmopatía hereditaria. El síndrome descrito por GB Stickler se caracterizaba por discapacidad visual y enfermedad articular degenerativa grave, que generalmente se desarrolla en la tercera o cuarta década de la vida. Es un trastorno autosómico dominante con una incidencia de aproximadamente 1 en 10.000 nacidos vivos. La presentación clínica incluye miopía, sordera progresiva, paladar hendido, hipoplasia de la mandíbula (anomalía de Pierre-Robin) e hipoplasia de las epífisis. En el período neonatal, las radiografías de pacientes con síndrome de Stickler revelan epífisis agrandadas, principalmente el fémur proximal y la tibia distal. Durante el crecimiento, se desarrolla displasia epifisaria, que se manifiesta por osificación irregular de las epífisis y cambios degenerativos posteriores.
Dado que COL 2 A se expresa en el cartílago articular y el vítreo ocular, la aparición del síndrome de Stickler se asoció con la patología de este gen. Sin embargo, un estudio de varias familias con síndrome de Stickler reveló que no todas presentan una enfermedad asociada con COL 2 A. Esta forma de la enfermedad se denomina síndrome de Stickler tipo I (símbolo del locus STL1).
El espectro de manifestaciones clínicas del síndrome de Stickler varía ampliamente, y hasta la fecha se han identificado varios fenotipos. Entre ellos se encuentra el síndrome de Wagner, que se caracteriza por un predominio de daño en el globo ocular. La artrosis en el síndrome de Wagner prácticamente nunca se desarrolla, aunque se ha identificado una mutación del gen COL 2A (sustitución de bases Gly67>Asp) en algunos pacientes. Aún no se ha aclarado por qué dicha mutación en COL compromete únicamente la función del cuerpo vítreo y no afecta al cartílago hialino.
Otra forma del síndrome de Stickler es la denominada variante holandesa; se caracteriza por todas las manifestaciones clásicas del síndrome, excepto la discapacidad visual. HG Brunner et al. (1994) demostraron que el fenotipo holandés del síndrome de Stickler está asociado a una mutación en el gen COL,,A 2: la mutación dominante es una deleción de 54 pares de bases seguida de una deleción de exón. M. Sirko-Osadsa et al. (1998) informaron de otra familia, no relacionada con la descrita por los autores anteriores, con un fenotipo similar y una mutación en el gen COL,,A 2 (deleción de 27 pares de bases), lo que confirma los datos de HG Brunner et al. (1994). Esta variante se denomina síndrome de Stickler tipo II (símbolo del locus STL1).
Recientemente, se identificó un tercer locus del síndrome de Stickler en miembros de una familia con patología vítrea y retiniana que difiere significativamente en su fenotipo de los cambios observados en la variante "clásica" del síndrome. Se encontró una mutación en el gen COL2A| (sustitución de bases Gly97>Val) en miembros de esta familia. Por supuesto, se necesitan nuevas descripciones de casos de este fenotipo y genotipo del síndrome de Stickler para confirmar los hallazgos de AJ Richards et al.
La conexión nosológica entre el síndrome de Marshall y la versión clásica del síndrome de Stickler se ha debatido durante mucho tiempo. Actualmente, el síndrome de Marshall se clasifica como un fenotipo independiente, principalmente debido a la deformación más pronunciada del esqueleto facial, aunque el daño a las articulaciones periféricas es similar al del síndrome de Stickler tipo I. En el síndrome de Marshall, la osteoartritis de las articulaciones de la rodilla y la columna lumbosacra comienza después de los 30 años. La causa del síndrome es una mutación en el gen del colágeno tipo IX COL n A1.
 [ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ]
[ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ]
OSMED
Este fenotipo se describió en una familia holandesa en la que se observaron cambios degenerativos articulares similares a la osteoartrosis en la adolescencia, afectando principalmente las articulaciones de la cadera, la rodilla, el codo y el hombro. También se observaron rasgos faciales peculiares, aumento de la lordosis lumbar, agrandamiento de las articulaciones interfalángicas y pérdida auditiva, pero no se detectaron anomalías visuales (Vikkula M. et al., 1995). Los investigadores encontraron una mutación en el gen que codifica la cadena α2del colágeno tipo II COL₃A₂.
Displasia de Knista
Se caracteriza por acortamiento del tronco y las extremidades, aplanamiento de la cara y el puente nasal, exoftalmos y anomalías articulares graves. En pacientes con síndrome de Kniest, las articulaciones, generalmente grandes desde el nacimiento, continúan agrandándose durante la infancia y la adolescencia temprana. También suelen presentar miopía, pérdida auditiva, paladar hendido y pie zambo; la mayoría de los pacientes desarrollan cambios degenerativos graves de forma temprana, especialmente pronunciados en las articulaciones de la rodilla y la cadera. Las radiografías de columna revelan aplanamiento y elongación significativa de los cuerpos vertebrales, así como platispondilia. Los huesos tubulares largos presentan una deformación similar a una mancuerna, y la osificación de las epífisis es lenta. En las articulaciones de las manos, las epífisis se aplanan y los espacios articulares se estrechan. El cartílago articular es blando y su elasticidad está reducida; histológicamente, se encuentran grandes quistes en él (síndrome del "queso suizo"). El síndrome de Kniest es causado por una mutación en el gen del procolágeno tipo II COb2A1.
 [ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ]
[ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ]
Displasia epifisaria múltiple (MED)
Un grupo heterogéneo de enfermedades que se caracteriza por el desarrollo anormal de las placas de crecimiento de los huesos tubulares largos, así como por osteoartrosis grave temprana (que se manifiesta en la infancia) que afecta tanto a las articulaciones axiales como periféricas (con mayor frecuencia a las articulaciones de la rodilla, la cadera, el hombro y la mano). Clínicamente, la MED se manifiesta con dolor y rigidez articular, así como alteraciones en la marcha. Los pacientes con MED también presentan cambios mínimos en la columna vertebral (diversos grados de aplanamiento de los cuerpos vertebrales); en ocasiones, la columna vertebral permanece intacta. La baja estatura de los pacientes también es característica, aunque rara vez se desarrolla enanismo. El órgano visual no se ve afectado. La MED incluye diversas variantes, por ejemplo, los fenotipos Fairbanks y Ribbing.
Las displasias de membranas (MED) se heredan de forma autosómica dominante con diversos grados de penetrancia. Dado que la característica distintiva de las MED es una anomalía de la placa de crecimiento epifisaria, se ha sugerido que estas displasias se deben a un defecto en los genes que codifican macromoléculas del cartílago de la placa de crecimiento. Se ha descubierto que al menos tres loci están asociados con el fenotipo MED. Estudios de E.J. Weaver et al. (1993) y J.T. Hecht et al. (1992) excluyeron los genes de los tipos de colágeno II y VI, la proteína del núcleo de los proteoglicanos y la proteína conectiva del cartílago de la lista de responsables de las MED. J.T. Hecht et al. (1993) y R. Oehelmann et al. (1994) encontraron una relación entre la MED, así como el síndrome de pseudoacondroplasia clínicamente relacionado, y la región pericentromérica del cromosoma 19. Estudios posteriores identificaron una mutación en el gen que codifica la proteína de la matriz oligomérica del cartílago (OMMP) en tres pacientes con MED (símbolo del locus EDM1). Dado que las tres mutaciones se produjeron en la región génica que codifica el dominio de unión al calcio de la OMMP, es probable que la función de unión al calcio de esta proteína sea esencial para el desarrollo normal del cartílago de la placa de crecimiento.
MD Briggs et al. (1994) informaron sobre una familia holandesa con un fenotipo MED asociado a una región del cromosoma 1 que contiene uno de los genes de colágeno tipo IX, COL1A1 (símbolo del locus EDM 2). Cabe destacar que la mutación encontrada constituyó la primera evidencia de la función del colágeno tipo IX, localizado en la superficie de las fibrillas de colágeno II, en el mantenimiento de la integridad del cartílago hialino. M. Deere et al. (1995) demostraron que el fenotipo Fairbanks no estaba genéticamente asociado ni con el locus EDM ni con el EDM2, lo que confirma la heterogeneidad del MED.
Condrodisplasia metafisaria (MCD)
Un grupo heterogéneo (se han descrito más de 150 tipos) de enfermedades hereditarias del cartílago hialino, que clínicamente se manifiestan como osteoartrosis temprana. Las MHD se caracterizan por cambios en las metáfisis óseas. Clínicamente, se manifiestan como baja estatura, extremidades acortadas, tibias arqueadas y marcha de pato. Los pacientes con MHD también muestran signos de daño en otros sistemas (por ejemplo, el inmunitario y el digestivo). Se observa desorganización del cartílago de la placa de crecimiento, que histológicamente se manifiesta como grupos de condrocitos proliferados e hipertrofiados rodeados de septos engrosados y matriz desorganizada, así como la penetración de cartílago no calcificado en el hueso subcondral.
Los síndromes de Jansen, Schmid y McKusick son los MHD más estudiados. Presentan características similares a las anomalías esqueléticas, pero difieren en su gravedad (síndrome de Jansen, síndrome de McKusick y síndrome de Schmid). El más común es el síndrome de Schmid (símbolo del locus MCDS), que se hereda de forma autosómica dominante. Radiológicamente, el síndrome se manifiesta por coxa vara, acortamiento y curvatura de los huesos tubulares y deformación en copa de las metáfisis (más pronunciada en la porción proximal del fémur que en la distal). Los cambios más pronunciados se observan en las placas de crecimiento de los huesos tubulares largos.
Se han descrito al menos 17 tipos diferentes de mutaciones en el gen del colágeno X en pacientes con síndrome de Schmid. El colágeno X se expresa en los condrocitos hipertrofiados de las placas de crecimiento y podría estar involucrado en los procesos de osificación. Por lo tanto, una mutación en el gen del colágeno X, COb2A1, es la causa más probable del síndrome de Schmid.
Los niños con síndrome de Jansen tienen hipercalcemia, niveles elevados de fosfato urinario y niveles disminuidos de hormona paratiroidea (PTH) y péptido relacionado con PT. La anomalía de este último es probablemente responsable del desarrollo del síndrome de Jansen. En 1994, AS Karaplis y coautores publicaron los resultados de un estudio original. Después de la interrupción del gen que codifica el péptido relacionado con PT en células madre embrionarias de ratón, los ratones con una deficiencia en este alelo murieron inmediatamente después del nacimiento. Se encontró que tenían una anomalía en el desarrollo del hueso subcondral, crecimiento deficiente del cartílago y disminución de la proliferación de condrocitos. En 1995, E. Schipani y coautores informaron una mutación heterocigótica en el gen del receptor de PTH en un paciente con síndrome de Jansen. La mutación consistió en una sustitución de bases Gys223>Arg, que condujo a la acumulación de AMPc; Esto significa que el aminoácido histidina en la posición 223 juega un papel crucial en la transmisión de señales. Más tarde, E. Schipani et al. (1996) informaron sobre otros tres pacientes con síndrome de Jansen, dos de los cuales tenían una mutación similar y el tercero tenía una sustitución TrА10>Рrо.
Osteoartritis generalizada primaria
La forma hereditaria más común de osteoartritis es la osteoartritis generalizada primaria (PGOA), que fue descrita por primera vez como una nosología separada por JH Kellgren y R. Moore en 1952. Clínicamente, la osteoartritis generalizada primaria se caracteriza por la aparición de nódulos de Bouchard y Heberden, lesiones poliarticulares. La osteoartritis generalizada primaria se caracteriza por la aparición temprana de la manifestación de la osteoartritis y su rápida progresión. Radiológicamente, la osteoartritis generalizada primaria no difiere de la osteoartritis no hereditaria. A pesar de que el tema de la etiopatogenia de la osteoartritis generalizada primaria aún se debate, los estudios demuestran el importante papel de la predisposición hereditaria en la aparición y progresión de la osteoartritis generalizada primaria.
Así, JH Kellgren et al. (1963) encontraron nódulos de Boucharay-Heberden en el 36% de los familiares varones y en el 49% de las mujeres, mientras que en la población general estas cifras fueron del 17 y el 26%, respectivamente. En individuos con osteoartritis generalizada primaria, el haplotipo HLA A1B8 y la isoforma MZ de la a1-antitripsina se detectan con mayor frecuencia. En un estudio clásico con gemelos, TD Spector et al. (1996) realizaron radiografías de las articulaciones de la rodilla y de la mano en 130 gemelas monocigóticas y 120 gemelas fraternas para detectar cambios característicos de la osteoartritis. Resultó que la concordancia de los signos radiográficos de la osteoartritis de todas las localizaciones fue 2 veces mayor en los gemelos monocigóticos en comparación con los gemelos fraternos, y la contribución de los factores genéticos osciló entre el 40 y el 70%. Un estudio de osteoartritis nodular realizado por GD Wright et al. (1997) demostraron la aparición temprana de la enfermedad, alta gravedad y una correlación negativa entre la edad de aparición de la enfermedad en los pacientes y la edad de concepción de sus padres.
Entre las artropatías asociadas a cristales, el depósito de cristales de ácido úrico y cristales que contienen calcio en la cavidad articular tiene una predisposición familiar.
Artropatías hereditarias asociadas a cristales (según Williams CJ y Jiménez SA, 1999)
Enfermedad |
Lugar |
Tipo de herencia |
Gen mutado |
Tipo de mutación |
Gota (HPRT)* |
Xq27 |
Ligado al cromosoma X |
HPRT1 |
Sustitución y eliminación de bases |
Gota (PRPS) |
Xq22-q24 |
Ligado al cromosoma X |
PRPS1 |
Reemplazo de la base |
Artropatía primaria por pirofosfato (CCAL1) |
5р15.1-р15.2 |
INFIERNO |
? |
? |
Artropatía por pirofosfato de inicio temprano asociada con 0A (CCAL2) |
8q |
INFIERNO |
? |
? |
*Los símbolos del locus se dan entre paréntesis; AD – autosómico dominante.
En 1958, D. Zintann S. Sitaj presentó descripciones clínicas de una patología denominada «condrocalcinosis» en 27 pacientes. La mayoría de los pacientes pertenecían a cinco familias, lo que indica un componente hereditario en la etiopatogenia de la enfermedad. Posteriormente, D. McCarty y J.L. Hollander (1961) informaron sobre dos pacientes con sospecha de gota, con depósito de cristales de nonurato en la cavidad articular. El examen radiográfico reveló una calcificación anormal del cartílago hialino de muchas articulaciones.
Radiográficamente, la enfermedad por depósito de cristales de pirofosfato de calcio dihidrato, o artropatía por pirofosfato, se asemeja a la artrosis esporádica, pero afecta con mayor frecuencia a articulaciones que no son típicas de las formas comunes de osteoartrosis (p. ej., articulaciones metacarpofalángicas, escaforadiales y femororrotulianas de la rodilla). En la artropatía por pirofosfato, es más frecuente la formación de quistes óseos subcondrales. Aunque en la mayoría de los casos la condrocalcinosis se presenta antes de la manifestación de la osteoartrosis secundaria, en algunos individuos la enfermedad puede comenzar como osteoartrosis idiopática, acompañada de trastornos metabólicos (hemocromatosis, hiperparatiroidismo, hipomagnesemia, etc.).
Lo más probable es que los cambios estructurales en la matriz extracelular (ECM) del cartílago articular induzcan la deposición de cristales de pirofosfato de calcio dihidratado. AO Bjelle (1972, 1981) encontró una disminución en el contenido de colágeno y la fragmentación de las fibras de colágeno en la zona media de la matriz del cartílago articular de familiares suecos con artropatía por pirofosfato. Dado que estas áreas no contenían cristales, los autores sugirieron que la anomalía descrita en la matriz puede predisponer a su deposición y al desarrollo de cambios degenerativos en las articulaciones. Con base en un estudio de casos esporádicos de artropatía por pirofosfato, K. Ishikawa et al. (1989), I. Masuda et al. (1991) concluyeron que la condrocalcinosis es causada por una mutación en los genes que codifican las proteínas de la matriz extracelular. CJ Williams et al. (1993), AJ Reginato et al. (1994) encontraron una mutación heterocigótica COL 2 A (sustitución de bases Argl5 > Cys) en miembros de una familia numerosa con un fenotipo clínico de osteoartritis temprana grave con anquilosis, desarrollo tardío de displasia espondiloepifisaria y condrocalcinosis del cartílago hialino y fibrocartílago. Sin embargo, en los miembros de esta familia, la condrocalcinosis era secundaria a la OA.
También se ha sugerido que los componentes inorgánicos de la matriz extracelular (ECM) contribuyen a la formación de cristales. Por ejemplo, la hipomagnesemia causa condrocalcinosis al inhibir la enzima pirofosfatasa, que a su vez reduce la disolución de los cristales. Se han encontrado niveles elevados de fosfatos inorgánicos en el líquido sinovial de pacientes con artropatía por pirofosfato. Esta y otras observaciones han sugerido que los pacientes con artropatía por pirofosfato tienen un trastorno local del metabolismo del pirofosfato. Se ha descrito la enzima nucleósido trifosfato pirofosfohidrolasa, que puede estar involucrada en la formación de cristales de pirofosfato en el área de su depósito en la ECM. Se han encontrado niveles elevados de esta enzima en casos esporádicos de artropatía por pirofosfato, pero esta anomalía no se ha observado en las formas familiares de la enfermedad (Ryan LM et al., 1986). Sin embargo, al cultivar fibroblastos y linfoblastos de pacientes con artropatía familiar por pirofosfato, se detectó un aumento en el contenido de fosfatos inorgánicos, lo que también confirma la suposición sobre el papel de las alteraciones en el metabolismo local del pirofosfato en la patogénesis de la enfermedad.
En los últimos años, se ha intentado identificar genes responsables de la aparición de casos familiares de artropatía por pirofosfato. Así, el análisis del material genético obtenido de miembros de una gran familia con artropatía por pirofosfato (Maine, EE. UU.), en la que la condrocalcinosis se desarrolló secundaria a una osteoartrosis grave, de rápida progresión y no displásica, excluyó una conexión entre la enfermedad y el locus COL 2. Sin embargo, los autores de este estudio encontraron una conexión entre el fenotipo estudiado de artropatía por pirofosfato y un locus ubicado en el brazo largo del cromosoma 8 (el símbolo del locus CCAL). AG Hughes et al. (1995) encontraron una conexión entre el fenotipo de condrocalcinosis primaria en una familia del Reino Unido y el locus CCAL1, que se localiza en el brazo corto del cromosoma 5, en la región 5p15. Según CJ Williams et al. (1996), el locus CCAL1 en miembros de una familia argentina con artropatía por pirofosfato se localizó algo más proximalmente que en el caso anterior, en la región 5p15.1. Se encontró un genotipo similar en miembros de una familia francesa.
Así pues, los datos de los estudios descritos indican que la forma familiar de la artropatía por pirofosfato es una enfermedad clínica y genéticamente heterogénea, que puede estar causada por mutaciones en al menos tres genes diferentes.

