Médico experto del artículo.
Nuevos artículos
Síntesis, secreción y metabolismo de las catecolaminas
Último revisado: 06.07.2025

Todo el contenido de iLive se revisa médicamente o se verifica para asegurar la mayor precisión posible.
Tenemos pautas de abastecimiento estrictas y solo estamos vinculados a sitios de medios acreditados, instituciones de investigación académica y, siempre que sea posible, estudios con revisión médica. Tenga en cuenta que los números entre paréntesis ([1], [2], etc.) son enlaces a estos estudios en los que se puede hacer clic.
Si considera que alguno de nuestros contenidos es incorrecto, está desactualizado o es cuestionable, selecciónelo y presione Ctrl + Intro.
La médula suprarrenal produce compuestos con una estructura distinta a la de los esteroides. Contienen un núcleo de 3,4-dihidroxifenilo (catecol) y se denominan catecolaminas. Entre estas se encuentran la adrenalina, la noradrenalina y la dopamina beta-hidroxitiramina.
La secuencia de síntesis de catecolaminas es bastante simple: tirosina → dihidroxifenilalanina (DOPA) → dopamina → noradrenalina → adrenalina. La tirosina ingresa al organismo con los alimentos, pero también puede formarse a partir de la fenilalanina en el hígado mediante la acción de la fenilalanina hidroxilasa. Los productos finales de la conversión de tirosina en los tejidos son diferentes. En la médula suprarrenal, el proceso avanza hasta la etapa de formación de adrenalina; en las terminaciones de los nervios simpáticos, hasta la formación de noradrenalina; y en algunas neuronas del sistema nervioso central, la síntesis de catecolaminas culmina con la formación de dopamina.
La conversión de tirosina a DOPA es catalizada por la tirosina hidroxilasa, cuyos cofactores son la tetrahidrobiopterina y el oxígeno. Se cree que esta enzima limita la velocidad de todo el proceso de biosíntesis de catecolaminas y es inhibida por los productos finales del proceso. La tirosina hidroxilasa es el principal objetivo de los efectos reguladores sobre la biosíntesis de catecolaminas.
La conversión de DOPA en dopamina es catalizada por la enzima DOPA descarboxilasa (cofactor: fosfato de piridoxal), que es relativamente inespecífica y descarboxila otros L-aminoácidos aromáticos. Sin embargo, existen indicios de la posibilidad de modificar la síntesis de catecolaminas modificando la actividad de esta enzima. Algunas neuronas carecen de enzimas para la posterior conversión de dopamina, y esta es el producto final. Otros tejidos contienen dopamina beta-hidroxilasa (cofactores: cobre, ácido ascórbico y oxígeno), que convierte la dopamina en noradrenalina. En la médula suprarrenal (pero no en las terminaciones de los nervios simpáticos), está presente la feniletanolamina, una metiltransferasa que forma adrenalina a partir de noradrenalina. En este caso, la S-adenosilmetionina actúa como donante de grupos metilo.
Es importante recordar que la síntesis de feniletanolamina-N-metiltransferasa es inducida por glucocorticoides que entran a la médula desde la corteza a través del sistema venoso portal. Esto podría explicar la combinación de dos glándulas endocrinas diferentes en un mismo órgano. La importancia de los glucocorticoides para la síntesis de adrenalina se ve reforzada por el hecho de que las células de la médula suprarrenal que producen noradrenalina se localizan alrededor de los vasos arteriales, mientras que las células productoras de adrenalina reciben sangre principalmente de los senos venosos ubicados en la corteza suprarrenal.
La degradación de las catecolaminas se produce principalmente bajo la influencia de dos sistemas enzimáticos: la catecol-O-metiltransferasa (COMT) y la monoaminooxidasa (MAO). Las principales vías de degradación de la adrenalina y la noradrenalina se muestran esquemáticamente en la figura 54. Bajo la influencia de la COMT, en presencia del donante de grupos metilo S-adrenosilmetionina, las catecolaminas se convierten en normetanefrina y metanefrina (derivados 3-O-metil de la noradrenalina y la adrenalina), que, bajo la influencia de la MAO, se convierten en aldehídos y, posteriormente (en presencia de la aldehído oxidasa), en ácido vanililmandélico (VMA), el principal producto de degradación de la noradrenalina y la adrenalina. En el mismo caso, cuando las catecolaminas se exponen inicialmente a la MAO en lugar de a la COMT, se convierten en aldehído 3,4-dioxomandélico y, posteriormente, bajo la influencia de la aldehído oxidasa y la COMT, en ácido 3,4-dioxomandélico y VMC. En presencia de la alcohol deshidrogenasa, el 3-metoxi-4-oxifenilglicol, principal producto final de la degradación de la adrenalina y la noradrenalina en el SNC, puede formarse a partir de las catecolaminas.
La descomposición de la dopamina es similar, excepto que sus metabolitos carecen del grupo hidroxilo en el átomo de carbono beta y, por lo tanto, en lugar de ácido vanililmandélico, se forma ácido homovanílico (HVA) o ácido 3-metoxi-4-hidroxifenilacético.
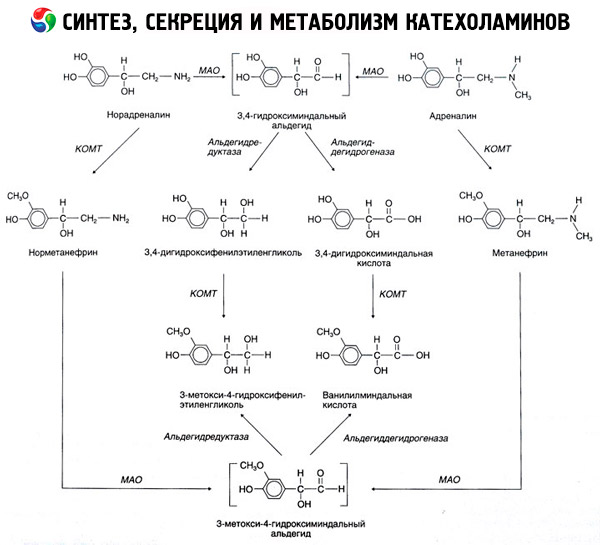
También se postula la existencia de una vía quinoide de oxidación de la molécula de catecolamina, que puede producir productos intermedios con pronunciada actividad biológica.
La noradrenalina y la adrenalina, formadas por la acción de las enzimas citosólicas en las terminaciones nerviosas simpáticas y la médula suprarrenal, penetran en los gránulos secretores, lo que los protege de la acción de las enzimas de degradación. La captación de catecolaminas por los gránulos requiere gasto energético. En los gránulos cromafines de la médula suprarrenal, las catecolaminas se unen estrechamente al ATP (en una proporción de 4:1) y a proteínas específicas, las cromograninas, lo que impide la difusión de hormonas desde los gránulos al citoplasma.
El estímulo directo para la secreción de catecolaminas es aparentemente la penetración de calcio en la célula, estimulando la exocitosis (fusión de la membrana granular con la superficie celular y su ruptura con liberación completa del contenido soluble - catecolaminas, dopamina beta-hidroxilasa, ATP y cromograninas - al líquido extracelular).
Efectos fisiológicos de las catecolaminas y su mecanismo de acción
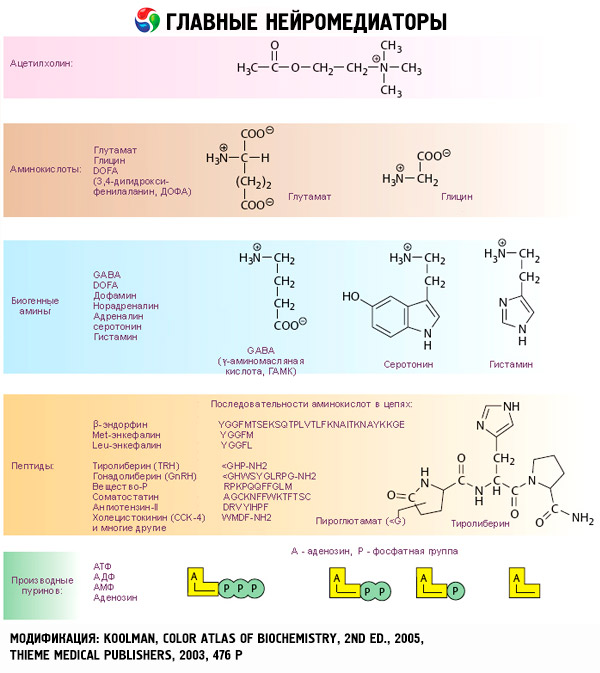
Los efectos de las catecolaminas comienzan con la interacción con receptores específicos de las células diana. Mientras que los receptores para las hormonas tiroideas y esteroideas se localizan en el interior de las células, los receptores para las catecolaminas (así como para la acetilcolina y las hormonas peptídicas) se encuentran en la superficie celular externa.
Se ha establecido desde hace tiempo que, en relación con algunas reacciones, la adrenalina o la noradrenalina son más eficaces que la catecolamina sintética isoproterenol, mientras que en relación con otras, el efecto del isoproterenol es superior a las acciones de la adrenalina o la noradrenalina. Sobre esta base, se desarrolló un concepto sobre la presencia de dos tipos de adrenorreceptores en los tejidos: alfa y beta, y en algunos de ellos solo puede estar presente uno de estos dos tipos. El isoproterenol es el agonista más potente de los beta-adrenorreceptores, mientras que el compuesto sintético fenilefrina es el agonista más potente de los alfa-adrenorreceptores. Las catecolaminas naturales (adrenalina y noradrenalina) pueden interactuar con receptores de ambos tipos, pero la adrenalina muestra una mayor afinidad por los beta-receptores y la noradrenalina por los alfa-receptores.
Las catecolaminas activan los receptores beta-adrenérgicos cardíacos con mayor intensidad que los receptores beta del músculo liso, lo que permitió dividir el tipo beta en subtipos: receptores beta1 (corazón, células grasas) y receptores beta2 (bronquios, vasos sanguíneos, etc.). El efecto del isoproterenol sobre los receptores beta1 es solo diez veces superior al de la adrenalina y la noradrenalina, mientras que sobre los receptores beta2 actúa entre 100 y 1000 veces más intensamente que las catecolaminas naturales.
El uso de antagonistas específicos (fentolamina y fenoxibenzamina para los receptores alfa y propranolol para los beta) confirmó la pertinencia de la clasificación de los adrenorreceptores. La dopamina puede interactuar con los receptores alfa y beta, pero diversos tejidos (cerebro, hipófisis, vasos sanguíneos) también poseen sus propios receptores dopaminérgicos, cuyo bloqueador específico es el haloperidol. El número de receptores beta varía de 1000 a 2000 por célula. Los efectos biológicos de las catecolaminas mediados por los receptores beta suelen estar asociados a la activación de la adenilato ciclasa y a un aumento del contenido intracelular de AMPc. Aunque el receptor y la enzima están funcionalmente conectados, son macromoléculas diferentes. El guanosín trifosfato (GTP) y otros nucleótidos de purina participan en la modulación de la actividad de la adenilato ciclasa bajo la influencia del complejo hormona-receptor. Al aumentar la actividad enzimática, parecen reducir la afinidad de los receptores beta por los agonistas.
El fenómeno del aumento de la sensibilidad de las estructuras desnervadas se conoce desde hace tiempo. Por el contrario, la exposición prolongada a agonistas reduce la sensibilidad de los tejidos diana. El estudio de los receptores beta ha permitido explicar estos fenómenos. Se ha demostrado que la exposición prolongada al isoproterenol provoca una pérdida de sensibilidad de la adenilato ciclasa debido a una disminución del número de receptores beta.
El proceso de desensibilización no requiere la activación de la síntesis proteica y probablemente se deba a la formación gradual de complejos hormona-receptor irreversibles. Por el contrario, la introducción de 6-oxidopamina, que destruye las terminaciones simpáticas, se acompaña de un aumento del número de receptores beta reactivos en los tejidos. Es posible que un aumento de la actividad simpática también provoque la desensibilización de los vasos sanguíneos y el tejido adiposo relacionada con la edad en relación con las catecolaminas.
El número de adrenorreceptores en diferentes órganos puede ser controlado por otras hormonas. Así, el estradiol aumenta y la progesterona disminuye el número de adrenorreceptores alfa en el útero, lo que se acompaña de un aumento y una disminución correspondientes en su respuesta contráctil a las catecolaminas. Si el "segundo mensajero" intracelular formado por la acción de los agonistas de los receptores beta es ciertamente el AMPc, entonces la situación con respecto al transmisor de los efectos alfa-adrenérgicos es más compleja. Se asume la existencia de varios mecanismos: una disminución en el nivel de AMPc, un aumento en el contenido de AMPc, modulación de la dinámica del calcio celular, etc.
Para reproducir diversos efectos en el organismo, se requieren dosis de adrenalina de 5 a 10 veces menores que las de noradrenalina. Si bien esta última es más eficaz contra los receptores adrenérgicos α y β1, es importante recordar que ambas catecolaminas endógenas pueden interactuar con ambos receptores. Por lo tanto, la respuesta biológica de un órgano a la activación adrenérgica depende en gran medida del tipo de receptores presentes en él. Sin embargo, esto no impide la activación selectiva del sistema nervioso o humoral del sistema simpático-adrenal. En la mayoría de los casos, se observa un aumento de la actividad de sus diversos enlaces. Por lo tanto, se acepta generalmente que la hipoglucemia activa de forma refleja la médula suprarrenal, mientras que la disminución de la presión arterial (hipotensión postural) se acompaña principalmente de la liberación de noradrenalina desde las terminaciones nerviosas simpáticas.
Los adrenorreceptores y los efectos de su activación en diversos tejidos
Sistema, órgano |
Tipo de receptor adrenérgico |
Reacción |
Sistema cardiovascular: |
||
Corazón |
Beta |
Aumento de la frecuencia cardíaca, la conductividad y la contractilidad. |
Arteriolas: |
||
Piel y mucosas |
Alfa |
Reducción |
Músculos esqueléticos |
Beta |
Expansión Contracción |
Órganos abdominales |
Alfa (más) |
Reducción |
Beta |
Extensión |
|
Venas |
Alfa |
Reducción |
Sistema respiratorio: |
||
Músculos de los bronquios |
Beta |
Extensión |
Sistema digestivo: |
||
Estómago |
Beta |
Disminución de las habilidades motoras |
Intestinos |
Alfa |
Contracción de los esfínteres |
Bazo |
Alfa |
Reducción |
Beta |
Relajación |
|
Páncreas exocrino |
Alfa |
Disminución de la secreción |
Sistema urogenital: |
Alfa |
Contracción del esfínter |
Vejiga |
Beta |
Relajación del músculo eyector |
Genitales masculinos |
Alfa |
Eyaculación |
Ojos |
Alfa |
Dilatación de la pupila |
Cuero |
Alfa |
Aumento de la sudoración |
Glándulas salivales |
Alfa |
Excreción de potasio y agua |
Beta |
Secreción de amilasa |
|
Glándulas endocrinas: |
||
Islotes del páncreas |
||
Células beta |
Alfa (más) |
Disminución de la secreción de insulina |
Beta |
Aumento de la secreción de insulina |
|
Células alfa |
Beta |
Aumento de la secreción de glucagón |
8 celdas |
Beta |
Aumento de la secreción de somatostatina |
Hipotálamo y glándula pituitaria: |
||
Somatotrofos |
Alfa |
Aumento de la secreción de STH |
Beta |
Disminución de la secreción de STH |
|
Lactotrofos |
Alfa |
Disminución de la secreción de prolactina |
Tirotrofos |
Alfa |
Disminución de la secreción de TSH |
Corticotrofos |
Alfa |
Aumento de la secreción de ACTH |
| beta | Disminución de la secreción de ACTH | |
Glándula tiroides: |
||
Células foliculares |
Alfa |
Disminución de la secreción de tiroxina |
Beta |
Aumento de la secreción de tiroxina |
|
Células parafoliculares (K) |
Beta |
Aumento de la secreción de calcitonina |
Glándulas paratiroides |
Beta |
Aumento de la secreción de PTH |
Riñones |
Beta |
Aumento de la secreción de renina |
Estómago |
Beta |
Aumento de la secreción de gastrina |
BX |
Beta |
Aumento del consumo de oxígeno |
Hígado |
? |
Aumento de la glucogenólisis y la gluconeogénesis con liberación de glucosa; aumento de la cetogénesis con liberación de cuerpos cetónicos. |
Tejido adiposo |
Beta |
Aumento de la lipólisis con liberación de ácidos grasos libres y glicerol. |
Músculos esqueléticos |
Beta |
Aumento de la glucólisis con liberación de piruvato y lactato; disminución de la proteólisis con disminución de la liberación de alanina, glutamina. |
Es importante tener en cuenta que los resultados de la administración intravenosa de catecolaminas no siempre reflejan adecuadamente los efectos de los compuestos endógenos. Esto se aplica principalmente a la noradrenalina, ya que en el organismo se libera principalmente no a la sangre, sino directamente en las hendiduras sinápticas. Por lo tanto, la noradrenalina endógena activa, por ejemplo, no solo los receptores alfa vasculares (aumento de la presión arterial), sino también los receptores beta del corazón (aumento de la frecuencia cardíaca), mientras que la administración de noradrenalina desde el exterior provoca principalmente la activación de los receptores alfa vasculares y una ralentización refleja (a través del nervio vago) de la frecuencia cardíaca.
Dosis bajas de adrenalina activan principalmente los receptores beta de los vasos musculares y del corazón, lo que resulta en una disminución de la resistencia vascular periférica y un aumento del gasto cardíaco. En algunos casos, el primer efecto puede prevalecer y desarrollar hipotensión tras la administración de adrenalina. En dosis más altas, la adrenalina también activa los receptores alfa, lo que se acompaña de un aumento de la resistencia vascular periférica y, en el contexto de un aumento del gasto cardíaco, conduce a un aumento de la presión arterial. Sin embargo, su efecto sobre los receptores beta vasculares también se mantiene. Como resultado, el aumento de la presión sistólica supera el indicador similar de la presión diastólica (aumento de la presión del pulso). Con la administración de dosis aún más altas, los efectos alfa-miméticos de la adrenalina comienzan a prevalecer: la presión sistólica y diastólica aumentan simultáneamente, como bajo la influencia de la noradrenalina.
El efecto de las catecolaminas sobre el metabolismo se compone de sus efectos directos e indirectos. Los primeros se realizan principalmente a través de los receptores beta. Procesos más complejos se asocian con el hígado. Si bien tradicionalmente se considera que el aumento de la glucogenólisis hepática se debe a la activación de los receptores beta, también existe evidencia de la participación de los receptores alfa. Los efectos indirectos de las catecolaminas se asocian con la modulación de la secreción de muchas otras hormonas, como la insulina. En el efecto de la adrenalina sobre su secreción, el componente alfa adrenérgico predomina claramente, ya que se ha demostrado que cualquier estrés se acompaña de la inhibición de la secreción de insulina.
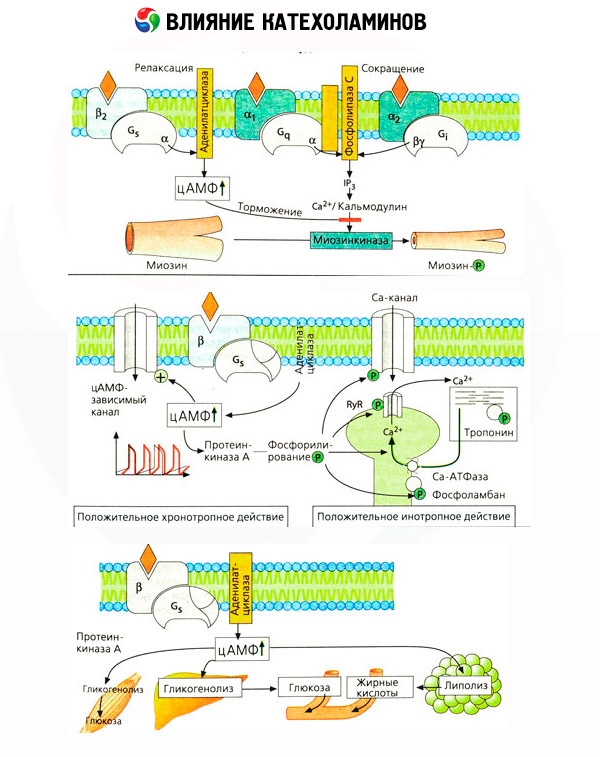
La combinación de los efectos directos e indirectos de las catecolaminas causa hiperglucemia, asociada no solo al aumento de la producción hepática de glucosa, sino también a la inhibición de su utilización por los tejidos periféricos. La aceleración de la lipólisis causa hiperlipacidemia con un mayor aporte de ácidos grasos al hígado y una intensificación de la producción de cuerpos cetónicos. El aumento de la glucólisis muscular conlleva un aumento de la liberación de lactato y piruvato a la sangre, que, junto con el glicerol liberado por el tejido adiposo, actúan como precursores de la gluconeogénesis hepática.
Regulación de la secreción de catecolaminas. La similitud de los productos y métodos de reacción del sistema nervioso simpático y la médula suprarrenal fue la base para la combinación de estas estructuras en un único sistema simpático-suprarrenal, con la asignación de sus enlaces nerviosos y hormonales. Diversas señales aferentes se concentran en el hipotálamo y en los centros de la médula espinal y el bulbo raquídeo, desde donde se originan los mensajes eferentes, que se dirigen a los cuerpos celulares de las neuronas preganglionares ubicadas en las astas laterales de la médula espinal, a nivel de los segmentos cervicales VIII y lumbares II-III.
Los axones preganglionares de estas células salen de la médula espinal y forman conexiones sinápticas con neuronas ubicadas en los ganglios de la cadena simpática o con células de la médula suprarrenal. Estas fibras preganglionares son colinérgicas. La primera diferencia fundamental entre las neuronas simpáticas posganglionares y las células cromafines de la médula suprarrenal es que estas últimas transmiten la señal colinérgica que reciben no por conducción nerviosa (nervios adrenérgicos posganglionares), sino por la vía humoral, liberando compuestos adrenérgicos a la sangre. La segunda diferencia radica en que los nervios posganglionares producen noradrenalina, mientras que las células de la médula suprarrenal producen principalmente adrenalina. Estas dos sustancias tienen efectos diferentes en los tejidos.

