Médico experto del artículo.
Nuevos artículos
Diagnóstico de las fases del curso del cáncer de próstata
Último revisado: 04.07.2025

Todo el contenido de iLive se revisa médicamente o se verifica para asegurar la mayor precisión posible.
Tenemos pautas de abastecimiento estrictas y solo estamos vinculados a sitios de medios acreditados, instituciones de investigación académica y, siempre que sea posible, estudios con revisión médica. Tenga en cuenta que los números entre paréntesis ([1], [2], etc.) son enlaces a estos estudios en los que se puede hacer clic.
Si considera que alguno de nuestros contenidos es incorrecto, está desactualizado o es cuestionable, selecciónelo y presione Ctrl + Intro.
Clínicamente se distingue entre cáncer localizado (T 1-2, N 0, M 0 ), localmente avanzado (T 3-4, N 0-1, M 0 ) y generalizado (T 1-4, N 0-1, M 1 ).
Los pacientes con estadios clínicamente localizados y localmente avanzados se clasifican según el grado de riesgo (D'Amico A V. et al., 2003):
- bajo: estadio T 1a-c; nivel de PSA menor de 10 ig/ml: clasificación de Gleason - 2-5; en biopsia - lesión unilateral menor del 50%:
- moderado: estadio T 2a; nivel de PSA menor de 10 ng/ml; puntuación de Gleason - 3 + 4 = 7; en biopsia - lesión bilateral menor del 50%;
- estadio alto T 2b, T 3a-b; nivel de PSA - 10-20 ng/ml; clasificación de Gleason - más de 4 + 3 - 7; en biopsia - daño más del 50%, invasión perineural;
- muy alto: estadio T 4; nivel de PSA superior a 20 ng/ml; puntuación de Gleason superior a 8; la biopsia muestra invasión linfovascular.
Tras aclarar el diagnóstico y determinar la extensión del proceso (localizado, localmente avanzado o generalizado), el médico y el paciente deben elegir el método de tratamiento. En la sociedad actual, se concede gran importancia a la calidad de vida de los pacientes tras el inicio del tratamiento. La calidad de vida sin tratamiento se corresponde con la evolución de la enfermedad subyacente y depende de la progresión del proceso oncológico. Los cambios en la calidad de vida se producen principalmente tras el inicio del tratamiento y el uso de algún método terapéutico o quirúrgico. Determinar claramente la etapa del proceso permite no solo elegir el método de tratamiento óptimo, sino también predecir la evolución de la enfermedad.
La determinación del nivel de PSA, en combinación con el cuadro clínico del cáncer de próstata y la gradación del tumor según la escala de Gleason, aumenta significativamente la información de cada uno de los indicadores mencionados para establecer el estadio patológico del cáncer. AV Partin et al. (1997) propusieron tablas pronósticas que permiten predecir la propagación del tumor, la elección del método de tratamiento, el grado de radicalidad y el pronóstico de la eficacia del tratamiento.
Para evaluar la extensión del tumor, los métodos más comunes son el tacto rectal, la ecografía transesofágica (ETR), la determinación del nivel de PSA y la gammagrafía ósea. Si es necesario, se prescriben tomografía computarizada (TC), resonancia magnética (RM) y radiografía de tórax.
Cualquier método de imagen está diseñado para determinar el estadio y evaluar la eficacia del tratamiento. Tras confirmar el diagnóstico, el urólogo debe determinar el volumen del tumor primario, sus límites y su potencial invasivo o metastásico. Todos estos indicadores son fundamentales para el pronóstico de la enfermedad y la elección del tratamiento.
Tumor primario (T)
En primer lugar, es necesario determinar si el tumor se limita a la glándula prostática (T 1-2 ) o se extiende más allá de la cápsula (T 3-4 ). El tacto rectal a menudo no permite evaluar la extensión del tumor. Según algunos datos, los resultados del tacto rectal coinciden con los del examen histológico en menos del 50% de los pacientes. Sin embargo, un examen más detallado solo está indicado cuando se decide un tratamiento radical.
El nivel de PSA puede reflejar la extensión del tumor, pero no permite determinar con precisión el estadio morfológico. La combinación del nivel de PSA, el índice de Gleason y los datos de palpación permite una mejor predicción del estadio morfológico que cada uno de estos parámetros por separado. El valor del PSA libre es controvertido: en un estudio, la determinación del contenido de PSA libre ayudó a aclarar el estadio en tumores localizados, pero otros estudios no lo confirmaron. Solo estudios exhaustivos ayudarán a resolver esta cuestión.
La ecografía transrectal se utiliza con mayor frecuencia para examinar el estado de la próstata. Este método puede detectar solo el 60% de los tumores y no siempre muestra invasión de la cápsula. Casi el 60% de los pacientes con estadio T3 . La ecografía indica un proceso menos común. Los signos ecográficos de invasión de la cápsula son abultamiento, irregularidades y rotura del contorno glandular. La invasión de células tumorales en las vesículas seminales es un signo de mal pronóstico, pero la información al respecto es fundamental para elegir el método de tratamiento. Al realizar una ecografía transrectal, se debe prestar atención a la ecoestructura de las vesículas (hiperecogenicidad), su asimetría, deformación y expansión. Además, el daño a las vesículas seminales se indica por la pérdida de redondez y la compactación en la base de la glándula. Estos signos son bastante subjetivos, por lo que no es apropiado confiar completamente en los datos ecográficos. La invasión de las vesículas seminales indica un alto riesgo de recidiva local y metástasis, y su biopsia está indicada para su aclaración (antes de la cirugía). El examen no debe iniciarse con este procedimiento, pero si el riesgo de invasión es alto y la elección del tratamiento depende del resultado de la biopsia, entonces su implementación está justificada. Un resultado negativo no excluye la invasión microscópica. Como regla general, una biopsia de las vesículas seminales se realiza en el estadio clínico T 2b y superior y el contenido de PSA es superior a 10 ng/ml. El resultado se considera positivo si al menos una biopsia de la base de la glándula prostática contiene células tumorales. No solo los estudios adicionales, sino también un análisis exhaustivo de los resultados de la biopsia primaria permiten aumentar la precisión de la determinación clínica del estadio (el número y la extensión de los focos tumorales y la invasión de la cápsula juegan un papel importante). El grado de diferenciación también es importante: con un índice de Gleason inferior a 6, el tumor está localizado en el 70% de los casos.
El flujo sanguíneo en la próstata con cáncer es mayor que en una glándula normal o con hiperplasia. Tras la castración, la intensidad del flujo sanguíneo en la glándula se reduce. El desarrollo de mapas eco-Dopplerográficos para el diagnóstico y seguimiento del cáncer de próstata es prometedor, pero actualmente no existen datos fiables sobre su uso para determinar el estadio del proceso local. Este método permite obtener material adicional durante la biopsia dirigida de focos de vascularización patológica.
Los resultados de la visualización del cáncer de próstata dependen directamente del equipo técnico de la clínica y de la experiencia del especialista. Por ello, todos los métodos de visualización modernos desempeñan un papel no determinante, sino esclarecedor, y la elección del método de tratamiento se basa en una combinación de datos de exploración clínica y estudios instrumentales.
La resonancia magnética (RM) ofrece las mejores capacidades para visualizar la estructura de la glándula prostática. El estándar moderno para examinar los órganos pélvicos mediante RM es el uso de un sensor endorrectal, que permite obtener una imagen con la mayor resolución espacial posible de 0,5 a 1 mm. La introducción forzada de aire en el sensor endorrectal proporciona una visualización nítida de la cápsula prostática, los ángulos rectoprostáticos y la fascia rectoprostática de Denonvilliers. El uso de un sensor endorrectal en la RM no limita la visualización de los ganglios linfáticos regionales (hasta el nivel de la bifurcación de la aorta abdominal). El cáncer de próstata se caracteriza por una baja intensidad de señal en las imágenes ponderadas en T2 contra el fondo de una señal de alta intensidad procedente de una zona periférica inalterada de la glándula. La forma irregular, la extensión difusa con efecto de masa y los contornos borrosos e irregulares son características morfológicas de los focos de baja intensidad de señal en la zona periférica de la glándula prostática, lo que sugiere una naturaleza neoplásica de la lesión. Al realizar contraste dinámico, los focos de cáncer acumulan rápidamente el agente de contraste en la fase arterial y lo eliminan rápidamente, lo que refleja el grado de angiogénesis y, en consecuencia, el grado de malignidad del tumor. La baja intensidad de señal también es característica de focos de hemorragias posbiopsia, prostatitis, hiperplasia benigna del estroma de la zona neutra de la glándula, cambios fibrocicatriciales, hiperplasia fibromuscular y consecuencias de la terapia hormonal o radioterapia. La resonancia magnética sin contraste dinámico no permite una diferenciación fiable de la mayoría de los cambios y enfermedades mencionados.
Como se mencionó anteriormente, una de las principales funciones de cualquier método de diagnóstico por imagen para el cáncer de próstata es determinar el volumen de la lesión glandular y la extensión del tumor más allá de la cápsula. Determinar el volumen tumoral es importante para el pronóstico. Un volumen tumoral inferior a 4 cm³ indica metástasis a distancia, y 12 cm³ indica una probabilidad extremadamente alta de metástasis. Según estudios, la precisión de la resonancia magnética para detectar focos de lesiones neoplásicas en la próstata oscila entre el 50 y el 90 %. La sensibilidad de la resonancia magnética para determinar la localización del cáncer de próstata es de aproximadamente el 70-80 %, mientras que los focos microscópicos de cáncer no pueden detectarse mediante resonancia magnética.
La principal ventaja de la resonancia magnética endorrectal es su capacidad para localizar lesiones neoplásicas en zonas inaccesibles a otros métodos diagnósticos y para esclarecer la naturaleza y dirección del crecimiento tumoral. Por ejemplo, la resonancia magnética permite detectar lesiones neoplásicas en la parte anterior de la zona periférica de la próstata, inaccesible con la biopsia transrectal. En general, la resonancia magnética complementa significativamente los datos del tacto rectal y la ecografía transrectal en la localización tumoral.
La resonancia magnética endorrectal permite visualizar la cápsula glandular, los haces vasculares y nerviosos, las vesículas seminales, el ápice glandular y el plexo venoso periprostático, así como determinar la prevalencia local del tumor glandular. Cabe destacar que la penetración de la cápsula se considera un signo microscópico, e incluso los dispositivos de resonancia magnética modernos (bobina endorrectal) no pueden proporcionar dicha información. Solo es posible obtener datos sobre el crecimiento más allá de la cápsula glandular.
Criterios diagnósticos de extensión extracapsular mediante resonancia magnética:
- la presencia de un tumor extracapsular;
- contorno desigual de la glándula (deformación, angularidad);
- asimetría de los haces neurovasculares;
- obliteración de los ángulos rectoprostáticos;
- amplio contacto del tumor con la cápsula.
La máxima especificidad (hasta un 95-98%) y precisión en los resultados de la resonancia magnética se alcanzan al examinar a pacientes con riesgo medio o alto de invasión extracapsular. Se cree que la invasión extracapsular (según los datos de la resonancia magnética) indica la inadecuación del tratamiento quirúrgico y un pronóstico desfavorable para la enfermedad. La terapia hormonal o la radioterapia no afectan la precisión en la detección de la diseminación extracapsular del tumor de próstata. La principal dificultad para detectar focos de cáncer y la diseminación extracapsular del tumor reside en la alta variabilidad en la interpretación de las tomografías por parte de los diferentes especialistas. La principal tarea de un especialista en radiodiagnóstico es lograr una alta especificidad diagnóstica (incluso a expensas de la sensibilidad) para no privar a los pacientes operables de la posibilidad de un tratamiento radical.
La similitud de la densidad del tejido prostático canceroso, hiperplásico y normal en la TC hace que este método sea poco útil para evaluar la diseminación local del tumor. La invasión de las vesículas seminales es más importante que la invasión de las cápsulas, pero incluso en este caso, la TC solo proporciona información en casos avanzados. No obstante, este método se utiliza activamente para marcar el área de impacto antes de la radioterapia.
El lento desarrollo del diagnóstico por radiación en nuestro país ha provocado un diagnóstico tardío del cáncer de próstata y, en consecuencia, una prevalencia insuficiente de métodos radicales de tratamiento (por ejemplo, la prostatectomía), la baja disponibilidad de tomógrafos modernos y la ausencia de programas de formación adecuados para especialistas en radiodiagnóstico y urólogos. A pesar de la amplia difusión de la TC y la RM, el nivel de equipamiento de las consultas y la formación de los especialistas en radiodiagnóstico es insuficiente para que la información obtenida sea decisiva a la hora de elegir un método de tratamiento para pacientes con cáncer de próstata.
Ganglios linfáticos regionales (N)
Los ganglios linfáticos regionales solo deben evaluarse cuando esto afecte directamente la estrategia de tratamiento (generalmente al planificar un tratamiento radical). Los niveles elevados de PSA, los tumores T2c -T3a, la baja diferenciación y la invasión perineural se asocian con un alto riesgo de metástasis ganglionar. La evaluación del estado ganglionar basada en los niveles de PSA se considera insuficiente.
Solo la linfadenectomía (abierta o laparoscópica) proporciona la información necesaria. Estudios recientes de linfadenectomía extendida han demostrado que el cáncer de próstata no siempre afecta a los ganglios linfáticos obturadores. En tumores asintomáticos y con niveles de PSA inferiores a 20 kg/ml, la TC confirma la presencia de ganglios linfáticos agrandados solo en el 1% de los casos. El uso de la RMN o la TC está justificado en casos de alto riesgo de metástasis, ya que la especificidad de estos métodos alcanza el 93-96%. Sin embargo, incluso un resultado positivo al utilizarlos puede ser falso, y solo la punción de un ganglio linfático sospechoso permite rechazar la linfadenectomía. Según un análisis retrospectivo, el tamaño del ganglio linfático no siempre indica la presencia de metástasis; la asimetría de los ganglios linfáticos afectados se considera un signo más informativo. Actualmente, solo al 2-3% de los pacientes sometidos a prostatectomía radical por cáncer de próstata localizado se les diagnostica metástasis en los ganglios linfáticos según el examen histológico posoperatorio.
La tomografía por emisión de positrones (PET) y la gammagrafía con anticuerpos marcados se recomiendan como métodos para detectar metástasis en los ganglios linfáticos, pero su uso aún es limitado debido a la sensibilidad insuficiente.
Los nomogramas de Partin (2001) permiten evaluar el riesgo de afectación ganglionar regional. Los nomogramas son algoritmos matemáticos que se utilizan para un paciente o grupo de pacientes. Estas tablas permiten determinar la probabilidad de diseminación tumoral local (cápsula, vesículas seminales) y afectación ganglionar en función del estadio clínico, el nivel de PSA y el índice de Gleason. En particular, permiten identificar un grupo de pacientes con baja probabilidad (menos del 10%) de metástasis ganglionar (con un nivel de PSA superior a 20 ng/md, estadio T 1-2a e índice de Gleason 2-6); en este grupo, es posible que no se especifique el estado de los ganglios linfáticos antes del tratamiento radical. El riesgo de metástasis ganglionar también puede evaluarse detectando áreas tumorales con anaplasia pronunciada (4-5 puntos): si dichas áreas se encuentran en cuatro o más biopsias o predominan en al menos una, el riesgo alcanza el 20-45%. En otros pacientes no supera el 2,5%. En estos casos no se requieren exámenes adicionales.
Metástasis a distancia (M)
En el 85% de los pacientes que fallecen por cáncer de próstata, se detectan lesiones del esqueleto axial. Las metástasis óseas se producen debido a la penetración de células cancerosas en la médula ósea a través del torrente sanguíneo, lo que conduce al crecimiento tumoral y la lisis de las estructuras óseas. La prevalencia de metástasis óseas afecta el pronóstico, y su detección temprana advierte al médico sobre posibles complicaciones. En el 70% de los casos, la metástasis se combina con un aumento en la actividad de la isoenzima ósea de la fosfatasa alcalina (ALP). La determinación de la actividad de la ALP y el nivel de PSA en la gran mayoría de los casos permite detectar la metástasis ósea. Según el análisis multivariante, estos indicadores se ven afectados únicamente por el número de metástasis óseas. Es importante que la actividad de la isoenzima ósea ALP refleje el grado de daño óseo con mayor precisión que el nivel de PSA.
La gammagrafía se considera el método más sensible para detectar metástasis óseas (es superior a la radiografía y a la determinación de la actividad de las fosfatasas alcalinas y ácidas). Los difosfonatos de tecnecio se utilizan mejor como radiofármaco, ya que su acumulación en los huesos es mucho más activa que en los tejidos blandos. Se ha demostrado una correlación entre la evaluación semicuantitativa del daño óseo y la supervivencia. La detección de metástasis a distancia es posible en cualquier órgano. Se presentan con mayor frecuencia en ganglios linfáticos no regionales, pulmones, hígado, cerebro y piel. En caso de quejas y síntomas correspondientes, se utilizan radiografías de tórax, ecografías, tomografías computarizadas y resonancias magnéticas para detectarlas. Las tácticas ante la sospecha de metástasis ósea se presentan en el diagrama.
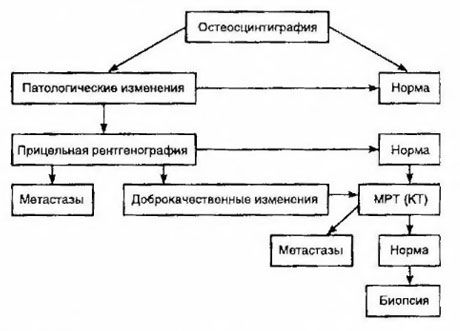
El indicador de laboratorio más fiable para determinar el grado de metástasis es el nivel de PSA. Se ha demostrado que un aumento superior a 100 ng/ml es el único parámetro que indica con fiabilidad la presencia de metástasis a distancia. La determinación del nivel de PSA reduce el número de pacientes que necesitan gammagrafía ósea. La probabilidad de detectar metástasis óseas con una disminución del nivel de PSA es muy baja. En ausencia de molestias y con un nivel inicial de PSA inferior a 20 ng/ml, se puede evitar la gammagrafía al detectar tumores altamente y moderadamente diferenciados. Al mismo tiempo, en caso de tumores poco diferenciados e invasión de la cápsula, está indicada la gammagrafía (independientemente del nivel de PSA).


 [
[