Médico experto del artículo.
Nuevos artículos
Oligofrenia fenilpirúvica o fenilcetonuria
Último revisado: 05.07.2025

Todo el contenido de iLive se revisa médicamente o se verifica para asegurar la mayor precisión posible.
Tenemos pautas de abastecimiento estrictas y solo estamos vinculados a sitios de medios acreditados, instituciones de investigación académica y, siempre que sea posible, estudios con revisión médica. Tenga en cuenta que los números entre paréntesis ([1], [2], etc.) son enlaces a estos estudios en los que se puede hacer clic.
Si considera que alguno de nuestros contenidos es incorrecto, está desactualizado o es cuestionable, selecciónelo y presione Ctrl + Intro.
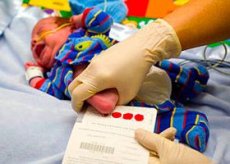
Según las estadísticas, a uno de cada 10-15 mil recién nacidos se le diagnostica una patología neurocognitiva determinada genéticamente: la oligofrenia fenilpirúvica, que se desarrolla debido a un trastorno congénito del metabolismo del aminoácido esencial fenilalanina.
La enfermedad fue identificada por primera vez en la década de 1930 en Noruega por el médico Ivar Foelling, quien la denominó hiperfenilalaninemia. Actualmente, la patología se denomina comúnmente fenilcetonuria y su código CIE-10 es E70.0.
Causas de la oligofrenia fenilpirúvica
Las causas genéticas de la oligofrenia fenilpirúvica son la herencia recesiva de padres portadores de dos alelos mutados de la enzima fenilalanina hidroxilasa (fenilalanina-4-monooxigenasa). Como resultado, el niño carece total o parcialmente de esta enzima, necesaria para la degradación de la fenilalanina (ácido proteinógeno α-amino-β-fenilpropiónico) a tirosina [ácido 2-amino-3-(4-hidroxifenil)propanoico].
Los genetistas han establecido que la patogénesis de esta enfermedad se asocia con más de 500 mutaciones estructurales homocigóticas o heterocigóticas diferentes en el cromosoma 12, en los genes de la enzima hepática fenilalanina hidroxilasa 12q23.2 o 12q22-q24.1. Esta mutación genética provoca una disminución de 4 o más veces en el nivel de esta enzima, necesaria para la oxidación de la fenilalanina presente en los alimentos proteicos.
Como resultado, por un lado, se produce una acumulación excesiva de fenilalanina en la sangre, lo cual resulta tóxico para el desarrollo cerebral. En este caso, la fenilalanina, que no puede convertirse en tirosina, se descompone por desaminación para producir ácido fenilpirúvico (ácido 2-oxo-3-fenilpropiónico o fenilpiruvato). Este ácido, a su vez, se convierte en ácido fenilacético (fenilacetato) y ácido feniláctico (fenillactato), que tienen un efecto negativo en las células del cerebro y del sistema nervioso central.
Por otra parte, las causas primarias de la oligofrenia fenilpirúvica (deficiencia congénita de fenilalanina hidroxilasa y su consecuencia, el exceso de fenilalanina) conducen a una disminución de los niveles de otros aminoácidos en el cerebro (triptófano, treonina, metionina, valina, isoleucina, leucina), lo que altera por completo el proceso de biosíntesis de los neurotransmisores que transmiten los impulsos nerviosos - dopamina y noradrenalina - y provoca un deterioro progresivo del desarrollo mental y físico en los niños.
Síntomas de la oligofrenia fenilpirúvica
El exceso de fenilalanina en el cuerpo se manifiesta en los bebés, y sus primeros signos son: letargo y somnolencia; problemas con la succión; convulsiones; vómitos; lesiones eccematosas de la epidermis; olor a humedad (a ratón) del cuerpo, la orina y el aliento (debido al aumento del contenido de fenilacetato, que se oxida en fenilcetonas).
Se observan los siguientes síntomas típicos de la oligofrenia fenilpirúvica: retraso del crecimiento; hipercinesia muscular, temblor o disminución del tono muscular; ataques psicóticos acompañados de irritabilidad y enojo desmotivados; disminución de las capacidades intelectuales o retraso mental.
Los niños con fenilcetonuria también presentan hipopigmentación: piel, cabello y ojos significativamente más claros y finos que los de sus padres. La causa inmediata de este síntoma es una deficiencia de tirosina, que, al oxidarse en los melanocitos de la epidermis, forma el pigmento melanina.
Como señalan especialistas en psiquiatría infantil, el cuadro clínico de la oligofrenia fenilpirúvica depende del grado de daño a las células cerebrales, y un bebé con esta patología puede parecer normal durante los primeros meses de vida. Si la enfermedad no se detecta inmediatamente después del nacimiento y el niño no recibe tratamiento durante un tiempo prolongado, las consecuencias son: daño cerebral irreversible y sus complicaciones, en forma de retraso mental grave o profundo (imbecilidad o idiotez).
Y luego pueden aparecer los siguientes síntomas de oligofrenia fenilpirúvica: baja estatura, anomalías craneofaciales (microcefalia, mandíbula superior prominente, dientes muy espaciados, desarrollo deficiente del esmalte dental), aumento del tono muscular y de los reflejos tendinosos, hiperactividad, mala coordinación de movimientos y marcha torpe, aumento de la irritabilidad y otros problemas de comportamiento y neurológicos hasta trastornos mentales.
Diagnóstico de la oligofrenia fenilpirúvica
El diagnóstico precoz de la oligofrenia fenilpirúvica y el tratamiento rápido son extremadamente importantes, reduciendo el riesgo de desarrollar retraso mental del 80-90% al 6-8% (según CLIMB – Centro Nacional de Información sobre Enfermedades Metabólicas, Reino Unido).
Para este fin, se debe realizar una prueba de detección de fenilcetonuria neonatal en los bebés el tercer o cuarto día después del nacimiento (en circunstancias excepcionales entre el quinto y el octavo día) mediante un análisis de sangre microbiológico para determinar el contenido de fenilalanina, la llamada prueba de Guthrie.
Las pruebas bioquímicas de orina para fenilpiruvato también revelan fenilcetonuria en recién nacidos, pero esta prueba solo debe realizarse entre 10 y 12 días después del nacimiento. Por lo tanto, el estándar diagnóstico internacional es la determinación de la concentración de fenilalanina en el plasma sanguíneo.
El diagnóstico instrumental moderno, basado en nuevas tecnologías como la espectrometría de masas en tándem, permite detectar numerosos trastornos metabólicos congénitos que conducen a discapacidades intelectuales. Esto garantiza el diagnóstico diferencial de patologías metabólicas genéticas, como galactosemia, cetonuria (trastornos del metabolismo de la leucina, isoleucina y valina), homocistinuria, aciduria glutárica, acidemia isovalérica, anemia de células falciformes, tirosinemia, hipotiroidismo congénito, etc.
¿A quién contactar?
Tratamiento de la oligofrenia fenilpirúvica
La dietoterapia es prácticamente el único tratamiento eficaz para la oligofrenia fenilpirúvica, que permite el desarrollo normal del cerebro. Sin embargo, al iniciar el tratamiento en niños mayores de tres o cuatro años, la dietoterapia no eliminará los síntomas de la patología ya existentes.
Los bebés con deficiencia de fenilalanina hidroxilasa no pueden consumir leche materna y existen fórmulas especiales sin fenilalanina para ellos: Lofenalac, Afenilak, Aminogran, Milupa pku1 (pku2 y pku3), Periflex Infanta, XP Maxamum.
La dieta excluye el consumo de carne, pescado, aves, leche, huevos, queso, requesón, helados, legumbres, frutos secos y muchos otros productos que contienen proteínas. El hidrolizado de caseína se utiliza como sustituto alimentario de productos prohibidos para mantener el equilibrio proteico en el organismo: una mezcla de aminoácidos sin fenilalanina extraída de la proteína de la leche (medicamentos como Berlofan o Ipofenato).
Si antes los médicos creían que tomar mezclas sin fenilalanina y seguir una dieta especial debía continuar hasta 10 años (es decir, hasta el final de los procesos de mielinización cerebral), ahora se sabe que suspender el tratamiento puede agravar la oligofrenia fenilpirúvica y causar consecuencias irreversibles. Si bien los pacientes que siguen restricciones dietéticas no presentan síntomas.
Actualmente, los medicamentos para el tratamiento de la oligofrenia fenilpirúvica (fenilcetonuria) están representados por el fármaco Kuvan, basado en diclorhidrato de sapropterina, un sustituto sintético del cofactor de la enzima fenilalanina hidroxilasa tetrahidrobiopterina (BH4). Los comprimidos de Kuvan, disueltos en agua, se toman una vez al día, por la mañana, con las comidas. La dosis se calcula individualmente, según el peso corporal del paciente (10 mg por kilogramo). Los efectos secundarios del fármaco incluyen secreción nasal acuosa, congestión nasal, dolor de cabeza, dolor de laringe, vómitos, diarrea y, ocasionalmente, dolor abdominal. Tomar este fármaco no cancela la dieta antifenilalanina. Las instrucciones del fármaco indican que no se ha estudiado su uso en niños menores de cuatro años.
En este caso, el tratamiento de la oligofrenia fenilpirúvica se realiza con un control constante del nivel de fenilalanina en la sangre.
La oligofrenia fenilpirúvica o fenilcetonuria es una enfermedad hereditaria y no se puede prevenir. Sin embargo, al planificar la maternidad, es posible prevenirla mediante un análisis de enzimas en sangre y una prueba genética para determinar si los futuros padres son portadores del gen mutante. También se pueden realizar análisis de fenilalanina en sangre durante el embarazo.
Como escribe el Journal of Inherited Metabolic Disease, “el pronóstico para los pacientes con esta patología, si no se trata, es una esperanza de vida máxima de hasta 30 años en el estado de una persona discapacitada con un deterioro grave de la función cerebral (ya que el nivel de fenilalanina en la sangre aumentará con el tiempo), y con tratamiento, hasta la vejez, con educación superior y una carrera exitosa”.


 [
[