Médico experto del artículo.
Nuevos artículos
Paludismo
Último revisado: 04.07.2025

Todo el contenido de iLive se revisa médicamente o se verifica para asegurar la mayor precisión posible.
Tenemos pautas de abastecimiento estrictas y solo estamos vinculados a sitios de medios acreditados, instituciones de investigación académica y, siempre que sea posible, estudios con revisión médica. Tenga en cuenta que los números entre paréntesis ([1], [2], etc.) son enlaces a estos estudios en los que se puede hacer clic.
Si considera que alguno de nuestros contenidos es incorrecto, está desactualizado o es cuestionable, selecciónelo y presione Ctrl + Intro.
La malaria (en inglés malaria; en francés paludisme) es una enfermedad protozoaria transmisible antroponótica aguda con un mecanismo de infección transmisible, caracterizada por síntomas pronunciados de intoxicación, un curso cíclico con ataques alternados de fiebre y períodos de apirexia, un bazo y un hígado agrandados, el desarrollo de anemia hemolítica con un curso progradiente y recaídas de la enfermedad.
Epidemiología
La fuente del agente infeccioso es una persona enferma o portadora del parásito cuya sangre contiene gametocitos. La malaria es una infección transmisible que se transmite por la picadura de un mosquito. Los gametocitos de P. vivax, P. ovale y P. malariae se encuentran en la sangre durante los primeros días de la enfermedad; su número aumenta tras varios ciclos de esquizogonia eritrocítica. Cuando una persona se infecta con P. falciparum, se convierte en fuente de infección entre 10 y 12 días después del inicio de la parasitemia y puede permanecer así durante dos meses o más.
En el caso de la malaria, son posibles diversos mecanismos de transmisión de la infección:
Mecanismo de transmisión (picadura de mosquito)
Este mecanismo es el principal que garantiza la existencia de los plasmodios como especie biológica. La fuente de infección es una persona (enferma de malaria o portadora del parásito), en cuya sangre se encuentran gametocitos maduros (células reproductoras masculinas y femeninas del parásito). Los únicos mosquitos hembra del género Anopheles portadores de malaria son los mosquitos hembra.
En el estómago del mosquito, donde los gametocitos masculinos y femeninos dentro de los eritrocitos ingresan junto con la sangre, se produce su maduración posterior (tras la lisis de los eritrocitos), fusión y división múltiple, con la formación de esporozoítos, que se acumulan en las glándulas salivales del mosquito. Las formas asexuales del parásito (trofozoítos, esquizontes), al entrar en el estómago del mosquito, mueren.
Así, en el cuerpo humano se produce una vía asexual de desarrollo del parásito (esquizogonia) con la formación y acumulación de gametocitos, y en el cuerpo del mosquito se produce una vía sexual (esporogonia), la fusión de los gametocitos masculinos y femeninos con su posterior desarrollo y la formación de esporozoitos.
 [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ]
[ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ]
Mecanismo de transmisión vertical
Mecanismo de transmisión vertical (de madre a feto) o de madre a recién nacido (durante el parto - vía parenteral). En la transmisión vertical, el feto rara vez se infecta a través de la placenta. Con mayor frecuencia, la infección ocurre durante el parto cuando cierta cantidad de sangre materna entra en el torrente sanguíneo del recién nacido, en cuyos eritrocitos se encuentran formas asexuales del parásito.
Mecanismo de transmisión parenteral
El mecanismo parenteral de infección conduce al desarrollo de la denominada malaria esquizonte. Se produce durante transfusiones de sangre o, con menor frecuencia, por violaciones de la asepsia durante las inyecciones (por ejemplo, entre drogadictos que utilizan la misma jeringa). En caso de infección durante una transfusión de sangre, la fuente de infección es un donante portador del parásito, a menudo con parasitemia sublatente (el número de parásitos es inferior a cinco en un μl de sangre). Por lo tanto, en regiones del mundo endémicas de malaria, es necesario utilizar, junto con los métodos parasitológicos (detección del parásito en preparaciones de gota gruesa y frotis de sangre), métodos serológicos (inmunológicos) de diagnóstico de laboratorio de malaria (RNIF, ELISA, etc.) para controlar la sangre del donante. Teniendo en cuenta que con la infección parenteral, por lo general solo se introducen unos pocos parásitos (especialmente con inyecciones), el período de incubación puede extenderse a 3 meses (con una infección masiva, el período de incubación, por el contrario, puede ser muy corto: varios días), lo cual es importante saber al diagnosticar la malaria en pacientes que se han sometido a cirugía y drogadictos.
Condiciones de propagación de la malaria
Para que la malaria se propague en una región determinada (país, territorio, zona) son necesarias las siguientes condiciones:
- Fuente de infección (un paciente con malaria o portador del parásito).
- La presencia de un portador eficaz (mosquitos del género Anopheles). La susceptibilidad a los parásitos de la malaria es la principal cualidad de una especie específica de mosquitos del género Anopheles. El número de mosquitos del género Anopheles entre poblaciones de otras especies no es tan alto como el de mosquitos no portadores de malaria, y rara vez causan molestias graves con sus picaduras. Sin embargo, incluso especies pequeñas, en otras circunstancias favorables (la proximidad de criaderos de mosquitos a viviendas humanas), pueden desempeñar un papel bastante importante. Más de 70 especies de mosquitos del género Anopheles (de más de 200 especies conocidas) pueden ser portadores eficaces de la malaria.
- Condiciones climáticas favorables: temperatura media diaria del aire superior a 16 °C y presencia de criaderos de mosquitos: cuerpos de agua, embalses, estructuras de riego, etc. La temperatura media diaria mínima del aire necesaria para el desarrollo en el cuerpo del mosquito Pl. vivax es de 16 °C, para Pl. falciparum - 18 °C, a temperaturas más bajas no se produce esporogonia. La duración de la esporogonia es menor cuanto más alta es la temperatura (hasta cierto nivel, ya que una temperatura media diaria de 30 °C o superior es desfavorable para la esporogonia). A una temperatura media diaria óptima (25-26 °C), la esporogonia en Pl. vivax tarda entre 8 y 9 días, en Pl. falciparum, entre 10 y 11 días.
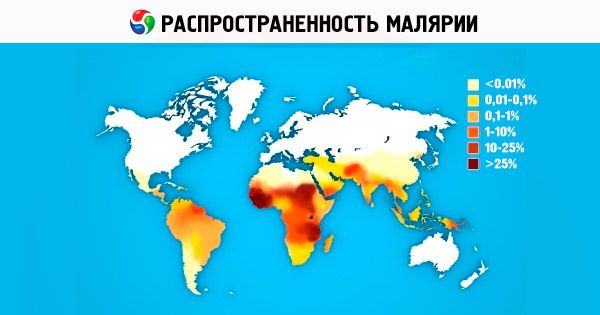
Toda el área de distribución de la malaria en el globo (entre 45° N y 40° S a 64° N y 45° S en diferentes años) está ocupada por malaria vivax. Las áreas de malaria falciparum y malariae malariae son algo más pequeñas debido a la mayor temperatura requerida para una esporogonia efectiva; el área de malaria ovale se encuentra en dos regiones que no están conectadas territorialmente entre sí: África tropical y los estados de la parte occidental del Océano Pacífico (Indonesia, Vietnam, Filipinas, Nueva Guinea, etc.). En países montañosos, los focos de malaria pueden formarse a altitudes de hasta 1000 m en la zona climática templada y hasta 1500-2500 m en la zona subtropical y tropical, con focos solo de malaria vivax que ocurren a grandes altitudes (1000-1500 m y más).
La malaria se caracteriza por una marcada estacionalidad. En climas templados y subtropicales, la temporada de malaria se divide en períodos de infección efectiva por mosquitos, transmisión de la infección y manifestaciones masivas de la enfermedad. El inicio del período de infección efectiva por mosquitos (en presencia de una fuente de infección: pacientes, portadores del parásito) coincide con el momento de un aumento estable de la temperatura media diaria a 16 °C. El inicio del período de transmisión se asocia con la finalización de la esporogonia en el cuerpo del mosquito, que depende de las temperaturas medias diarias específicas de un año determinado. En la región de Moscú, el período de transmisión de la malaria vivax puede alcanzar de 1,5 a 2 meses o más, hasta las primeras heladas de otoño. Los límites del período de manifestaciones masivas están menos definidos. En focos donde la malaria solo se transmite durante tres días, la morbilidad masiva puede comenzar mucho antes del inicio del período de transmisión. Los casos observados son manifestaciones primarias de malaria vivax con un largo período de incubación (3-10 meses) debido a la infección en la temporada anterior y la preservación de hipnozoitos en el hígado (sin manifestaciones primarias con un corto período de incubación), así como recaídas exoeritrocíticas a distancia (después de una serie de ataques de malaria con un corto período de incubación en la temporada anterior, sin una terapia antirrecaída adecuada).
La susceptibilidad a la malaria es universal. El desenlace de la infección tras la entrada del patógeno en el torrente sanguíneo y la evolución clínica de la enfermedad están determinados por el estado inmunológico individual, la actividad de factores de resistencia innatos no específicos, la intensidad de la inmunidad postinfección y, en el caso de los recién nacidos, el nivel de anticuerpos específicos de clase G recibidos de la madre. La excepción son los pueblos indígenas de África Occidental y Nueva Guinea, que son mayoritariamente inmunes a la infección por Pl. vivax, lo que se asocia a la ausencia, genéticamente determinada, de isoantígenos eritrocitarios del grupo Duffy, que actúan como receptores para los merozoitos de Pl. vivax. En consecuencia, en esta región, los casos de infección por malaria por vivax se observan con una frecuencia significativamente menor que en otras regiones de África tropical.
Las personas portadoras de hemoglobina anormal (talasemia, anemia de células falciformes, hemoglobina E, C, etc.), con anomalías en la estructura del citoesqueleto eritrocítico (esferocitosis hereditaria, ovalocitosis sudoriental, eliptocitosis hereditaria) o que tienen una deficiencia de la enzima glucosa-6-fosfato deshidrogenasa de los eritrocitos tienen una resistencia relativa a la infección por todos los tipos de plasmodios. En caso de infección con malaria, presentan una enfermedad leve, el número de parásitos en la sangre se mantiene en un nivel relativamente bajo y los casos de progresión maligna (malaria cerebral - falciparum) son prácticamente inexistentes. Por otro lado, las personas con una deficiencia de glucosa-6-fosfato deshidrogenasa corren el riesgo de desarrollar hemólisis aguda al utilizar varios fármacos antipalúdicos (primaquina, quinina, etc.). Los mecanismos de resistencia natural a los diversos tipos de malaria aún son en gran parte inciertos y continúan siendo estudiados.
Los recién nacidos también presentan cierta resistencia a la infección por todas las formas de malaria. Esto se debe a:
- la presencia de inmunidad pasiva debido a los anticuerpos de clase G recibidos por el recién nacido de una madre hiperinmune (en zonas con alta incidencia de malaria);
- mantener la inmunidad específica después del nacimiento debido a los anticuerpos de clase A que recibe el recién nacido con la leche materna;
- la presencia de hemoglobina fetal en el recién nacido, que es de poca utilidad para alimentar al parásito de la malaria.
Después de los primeros tres a seis meses de vida, los recién nacidos tienen un riesgo significativamente mayor de desarrollar formas malignas y graves de malaria falciparum (cambio de glóbulos rojos que contienen hemoglobina fetal a glóbulos rojos que contienen hemoglobina normal; transición a la alimentación mixta - ingesta de ácido para-aminobenzoico, necesario para el desarrollo del parásito, que está ausente en la leche materna).
 [ 10 ], [ 11 ], [ 12 ], [ 13 ]
[ 10 ], [ 11 ], [ 12 ], [ 13 ]
Inmunidad en la malaria
La inmunidad a la malaria no es estéril, específica de especie y cepa, inestable y de corta duración. Para mantener el nivel protector de anticuerpos, es necesaria la estimulación antigénica constante mediante infecciones repetidas de malaria. La inmunidad a Pl. malariae y Pl. vivax se establece antes y se mantiene durante más tiempo que a Pl. falciparum. La inmunidad antimalárica incluye respuestas celulares y humorales. Los procesos inmunitarios que estimulan la síntesis de anticuerpos comienzan con la fagocitosis de los parásitos de la malaria por los macrófagos. Esto se manifiesta por la hiperplasia del sistema histiofagocítico del bazo, el hígado y la médula ósea.
Prevalencia de la malaria
De las cuatro especies de patógenos de malaria humana, P. vivax es la más común en el mundo. En los trópicos y subtrópicos, los esporozoitos predominan en el acervo genético de la población de P. vivax. Causan la enfermedad después de una incubación corta (10-21 días). En el continente africano, P. vivax se encuentra constantemente en los países del este de África entre árabes, indios, etíopes y europeos. En los países del oeste de África, que está poblado principalmente por representantes de la raza negroide, P. vivax no se encuentra, lo que se explica por la inmunidad innata determinada genéticamente de los negros africanos a P. vivax [los eritrocitos carecen de un receptor para los merozoitos de P. vivax - isoantígenos Duffy (Fy d o Fy b )]. El rango de P. ovale es pequeño y consta de dos partes. La parte principal, africana, ocupa el África tropical desde Gambia en el norte hasta el Congo en el sur del continente. La segunda parte del área de distribución abarca los países del Océano Pacífico Occidental y el Sudeste Asiático. La malaria tropical se distribuye geográficamente hasta los 40° de latitud norte y los 20° de latitud sur. P. falciparum causa hasta el 50% de los casos de malaria en el mundo. La malaria de cuatro días se encuentra actualmente en África, algunas zonas de América Central y del Sur, y el Caribe.
La mayoría de las personas son susceptibles a la malaria. La excepción es la población indígena de África Occidental. Las zonas hiperendémicas de África tropical, donde predomina P. falciparum, se caracterizan por una estructura inmunitaria relativamente estable en la población indígena:
- Los niños menores de 6 meses no se enferman debido a la inmunidad pasiva que reciben de la madre:
- La mayoría de los niños de 6 a 24 meses están infectados con P. falciparum; la inmunidad pasiva se ha desvanecido, la inmunidad activa aún no se ha desarrollado; este grupo tiene la mayor mortalidad por malaria:
- En niños mayores de 2 años, P. falciparum se detecta con menor frecuencia, el curso de la malaria se atenúa como resultado de la inmunidad adquirida y la intensidad de la parasitemia disminuye con la edad:
- En adultos, P. falciparum rara vez se detecta debido a la alta tensión inmune; cuando hay infección, no hay manifestaciones clínicas.
La malaria tropical también es fácilmente tolerada por portadores de hemoglobina S anormal (anemia de células falciformes) y personas con ciertas otras anomalías determinadas genéticamente de la hemoglobina y de las enzimas de los glóbulos rojos (deficiencia de G-6-PDH).
Historia de la investigación sobre la malaria
El estudio de la malaria (una de las enfermedades humanas más antiguas) está inextricablemente ligado a la historia de la civilización humana. Se supone que la malaria comenzó a propagarse por la Tierra (desde la región africana del Mediterráneo) hace unos 10.000 años debido al desarrollo intensivo de la agricultura, el comercio y la exploración de nuevas tierras. En los papiros egipcios, la literatura china y los cánones de la medicina clásica india (ayurveda), las descripciones del cuadro clínico y las epidemias de malaria han sobrevivido hasta nuestros días; incluso entonces, se suponía una posible conexión entre el desarrollo de la enfermedad y las picaduras de mosquitos. Posteriormente (siglos V-VI a. C.), los médicos griegos Hipócrates, Heradoto y Empédocles describieron el cuadro clínico de la malaria en detalle. A Hipócrates se le atribuye la distinción de la malaria del grupo de enfermedades febriles: propuso distinguir tres formas de la enfermedad: “cotidiana” (ataques diarios), “terciana” (ataques cada dos días) y “cuartana” (ataques cada 2 días).
El inicio de la era de los descubrimientos científicos en el estudio de la malaria se remonta a 1640, cuando el médico y conquistador español Juan del Vego utilizó por primera vez una infusión de corteza de quina para tratar a pacientes con malaria, previamente utilizada por los indígenas de Perú y Ecuador como antipirético. El mérito de nombrar la enfermedad como "malaria" (del italiano: "mal aria" - aire malo) se atribuye al italiano Lancisi (1717), quien asoció la infección de las personas con malaria a través de vapores "venenosos" provenientes de los pantanos. En 1880, el médico francés A. Laveran, trabajando en Argelia, describió en detalle la morfología del patógeno de la malaria. En 1897, el médico militar inglés Ronald Ross, en la India, estableció el mecanismo de transmisión de la malaria.
Actualmente, la malaria es uno de los problemas de salud más graves en más de 100 países de África, Asia y Sudamérica. Aproximadamente la mitad de la población mundial corre el riesgo de contraerla. Casi todos los países de Europa y Norteamérica registran anualmente cientos de casos importados de malaria entre personas procedentes de regiones donde está extendida, y el número de casos de la llamada malaria de aeropuerto está en aumento. Según la OMS, entre 200 y 250 millones de personas en el mundo contraen malaria cada año; al menos el 80 % de los casos se registran en países africanos al sur del Sahara. Cada año, entre 1 y 2 millones de personas mueren a causa de la malaria, principalmente niños menores de 5 años. Las pérdidas sociales y económicas, solo en África, se estiman en 2000 millones de dólares estadounidenses al año. Desde 1998, bajo los auspicios de la OMS, el Banco Mundial y UNICEF, se ha implementado un programa científico y práctico (Iniciativa para Hacer Retroceder la Malaria) para el control de la malaria (principalmente en países en desarrollo). El programa está previsto que se extienda hasta el período 2010-2015. Se están desarrollando activamente para crear una vacuna eficaz contra la malaria, pero esto requerirá al menos otros 10 a 15 años. La búsqueda, el desarrollo y la mejora de medicamentos para el tratamiento de la malaria son uno de los programas prioritarios de la OMS, diversas compañías farmacéuticas e institutos de investigación de todo el mundo. En los últimos años, Rusia ha experimentado un aumento de casos importados de malaria como resultado del aumento de la migración y el desarrollo intensivo del turismo internacional.
Causas malaria
El nombre de la enfermedad "malaria" en realidad generaliza cuatro enfermedades protozoarias distintas causadas por cuatro tipos de patógenos, respectivamente.
La malaria es causada por parásitos pertenecientes al tipo Protozoa, clase Sporozoa, familia Plasmodiidae, género Plasmodium. Cuatro tipos de patógenos parasitan a los humanos: P. vivax causa malaria de tres días, P. malariae causa malaria de cuatro días, P. falciparum causa malaria tropical y P. ovale causa malaria ovale de tres días.
Patógenos de la malaria
Excitante |
Forma de malaria (según la CIE-10) |
Plasmodium (Laverania) falciparum |
Malaria causada por Plasmodium falciparum (malaria falciparum) |
Plasmodium (Plasmodium) vivax |
Malaria causada por Plasmodium vivax (malaria-vivax) |
Plasmodium (Plasmodium) ovale |
Malaria causada por Plasmodium ovale (malaria ovale) |
Plasmodium (Plasmodium) malariae |
Malaria causada por Plasmodium malariae (malaria-malariae) |
En la mayoría de las publicaciones nacionales (libros de texto, manuales, libros de referencia) se conservan los nombres anteriores de las formas de malaria: malaria tropical (malaria-falciparum), malaria de tres días (malaria-vivax), malaria oval (malaria-ovale) y malaria de cuatro días (malaria-malariae).
Cada una de las cuatro formas de malaria se caracteriza por sus propias características clínicas, patogénicas y epidemiológicas. La malaria falciparum ocupa el lugar más importante, representando entre el 80% y el 90% de todos los casos de malaria en el mundo, y cuyo agente causal pertenece a un subgénero específico (Laverania). Solo la malaria falciparum puede desarrollar una enfermedad maligna, con desenlace mortal.
Durante su ciclo de vida, los patógenos de la malaria experimentan el siguiente ciclo de desarrollo con un cambio de huéspedes:
- El desarrollo asexual (esquizogonia) ocurre en el cuerpo del huésped intermediario: un ser humano;
- El desarrollo sexual (esporogonia) ocurre en el cuerpo del huésped final: el mosquito hembra del género Anopheles.
Los esporozoítos entran al cuerpo humano a través de la picadura de un mosquito infectado con malaria. Tras entrar en la sangre, los esporozoítos penetran en los hepatocitos desde los vasos sinusoidales del hígado en 15-45 minutos e inician el ciclo exoeritrocítico (esquizogonia tisular). La selectividad y velocidad de invasión se deben a la presencia de receptores específicos en las membranas de los hepatocitos. Los parásitos aumentan de tamaño, se dividen repetidamente y forman muchas formaciones mononucleares pequeñas: merozoítos. La duración mínima del ciclo exoeritrocítico es de 5-7 días para P. falciparum, 6-8 días para P. vivax, 9 días para P. ovale y 14-16 días para P. malariae. Posteriormente, los merozoítos abandonan los hepatocitos hacia la sangre y penetran en los eritrocitos, donde se produce la esquizogonia eritrocitaria. La malaria de tres días y la malaria oval se caracterizan por un tipo especial de desarrollo exoeritrocítico: todos los parásitos, o algunos de ellos, pueden permanecer en los hepatocitos durante un período prolongado (7-14 meses o más) en estado latente (hipnozoítos), y solo después de este período comienzan a transformarse en merozoítos capaces de infectar los eritrocitos. Esto determina la posibilidad de una incubación prolongada y la aparición de recaídas remotas de hasta tres años.
La esquizogonia eritrocítica se acompaña del desarrollo cíclico y la división múltiple de los parásitos, y los plasmodios palúdicos pasan por las siguientes etapas: trofozoíto joven (tiene forma de anillo); trofozoíto en desarrollo; trofozoíto maduro (tiene un núcleo grande); esquizonte en desarrollo; esquizonte maduro. Después de completarse el proceso de esquizogonia, el eritrocito se destruye. Los merozoítos libres penetran activamente en nuevos eritrocitos, pero la mayoría mueren por los efectos de los mecanismos inmunitarios protectores del huésped. La duración de la esquizogonia eritrocítica es de 48 horas en P. vivax, P. ovale, P. falciparum y de 72 horas en P. malariae. Durante el ciclo eritrocítico, algunos merozoítos se transforman en formas sexuales: femeninas (macrogametocitos) o masculinas (microgametocitos).
Los gametocitos entran al cuerpo del mosquito portador cuando este se alimenta de la sangre de un paciente con malaria o de un portador del parásito. que contiene gametocitos maduros. En el estómago del mosquito, después de 9-12 minutos, el gametocito masculino expulsa ocho flagelos móviles delgados. Los flagelos libres (microgametos) penetran en la célula femenina (macrogameto); después de la fusión de los núcleos, se forma un cigoto: una célula fecundada redonda. Luego, los oocinetos, ooquistes con esporozoitos, se desarrollan sucesivamente, y su maduración ocurre en las glándulas salivales del mosquito. A una temperatura ambiente óptima del aire (25 °C), la esporogonia dura 10 días en P. vivax, 12 días en P. falciparum, 16 días en P. malariae y P. ovale; a una temperatura del aire inferior a 15 °C, los esporozoitos no se desarrollan.
Patogenesia
Todos los síntomas de la malaria son causados por la esquizogonia eritrocítica, es decir, el crecimiento y la reproducción de formas eritrocíticas asexuales del parásito en la sangre. La esquizogonia tisular no se manifiesta clínicamente.
Un ataque palúdico se asocia con la finalización de la esquizogonia eritrocítica, la desintegración masiva de eritrocitos y la entrada en la sangre de una gran cantidad de merozoítos, productos metabólicos de parásitos con propiedades pirogénicas y tóxicas que provocan el desarrollo de una reacción febril. Debido a la naturaleza cíclica de la esquizogonia eritrocítica, los ataques febriles se repiten cada 48 horas en la malaria de tres días, ovalada y tropical, y cada 72 horas en la malaria de cuatro días. Cuando una persona se infecta, una población heterogénea de parásitos palúdicos ingresa al cuerpo, y la esquizogonia en el período inicial ocurre de forma asincrónica, debido a lo cual el tipo de fiebre puede ser irregular. A medida que se desarrollan las reacciones inmunitarias, la capacidad de parasitar en los eritrocitos se conserva en una generación principal de plasmodios, lo que determina el ritmo febril característico de esta especie. Sólo en la malaria tropical puede haber varias (2-3) generaciones principales de plasmodios, por lo que la fiebre suele ser irregular.
La anemia, característica de la malaria, es consecuencia de la destrucción de los glóbulos rojos por los parásitos que se encuentran en ellos. Se sabe que P. vivax y P. ovale penetran principalmente en los glóbulos rojos jóvenes, mientras que P. malariae lo hace en los maduros. P. falciparum infecta glóbulos rojos con diferentes grados de madurez, lo que contribuye a un mayor daño y hemólisis. Por lo tanto, en la malaria tropical, la hemólisis desempeña un papel fundamental en la génesis de la anemia. Otros factores que contribuyen a la hemólisis de los glóbulos rojos son los mecanismos autoinmunes que dañan a los glóbulos rojos no infectados. La hiperplasia de los elementos reticuloendoteliales del bazo, que se desarrolla en la malaria, inhibe la hematopoyesis, lo que aumenta la anemia y la trombocitopenia.
El agrandamiento del hígado y el bazo se debe inicialmente a la congestión en estos órganos, pero pronto se presenta hiperplasia linfoide y reticuloendotelial. Como resultado de la hemólisis de los eritrocitos, así como del daño a los hepatocitos, se desarrolla ictericia. La disminución de la absorción de carbohidratos y la inhibición de la gluconeogénesis hepática causan hipoglucemia. La activación de la glucólisis anaeróbica provoca la acumulación de lactato en la sangre y el líquido cefalorraquídeo, y la aparición de acidosis láctica, una de las causas de la malaria tropical grave.
En la malaria tropical, las propiedades de los eritrocitos se alteran, lo que provoca una alteración de la microcirculación (citoadhesión, secuestro, formación de rosetas). La citoadhesión es la adhesión de eritrocitos infectados a las células endoteliales, lo que provoca el secuestro en capilares y vénulas poscapilares. El papel principal en la citoadhesión recae en proteínas ligando específicas (cuya expresión en la superficie de los eritrocitos es inducida por el parásito) y en receptores ubicados en la superficie externa de las células endoteliales. La oclusión de los vasos sanguíneos provoca isquemia en los órganos afectados. Aparecen protuberancias (bultos) en las membranas de los eritrocitos, que entran en contacto con excrecencias en forma de pseudópodo formadas en las células endoteliales. Algunas variedades de P. falciparum hacen que los eritrocitos sanos se adhieran a los infectados, lo que resulta en la formación de "rosetas". Los glóbulos rojos se vuelven rígidos, lo que empeora las propiedades reológicas de la sangre y agrava el trastorno de la microcirculación. Un factor perjudicial importante es la hipoxia causada por la función insuficiente del transporte de oxígeno de los glóbulos rojos infectados. El tejido cerebral es el menos resistente a la hipoxia, lo que contribuye al desarrollo de la malaria cerebral. Se producen trastornos en el sistema de coagulación sanguínea: en la malaria tropical grave, se observan signos del síndrome DIC, trombocitopenia e hipofibrinogenemia. Se le da un cierto papel en la patogénesis de la malaria tropical a la reacción inflamatoria inespecífica generalizada. El daño vascular es causado principalmente por la acción de mediadores inflamatorios. Los más activos son los productos de peroxidación lipídica y las proteasas secretadas por los granulocitos. En la patogénesis de la malaria grave, se presta considerable atención a las citocinas, en particular TNF e IL (IL-2 e IL-6). Los cambios más característicos de la malaria tropical grave se producen en el cerebro, donde se observan edema, inflamación de la masa encefálica y crecimientos perivasculares y periganglionares de neuroglia (granulomas de Durk). Los capilares se obstruyen por la invasión de eritrocitos y parásitos; se observa hemostasia extensa. Se desarrolla edema perivascular con hemorragias y necrosis focal. A partir del cuadro patológico, se puede concluir que, en casos de coma palúdico, se desarrolla meningoencefalitis específica.
La infección por malaria puede alterar la respuesta inmunitaria del huésped, lo que desencadena una cascada de reacciones inmunopatológicas. La fijación de inmunoglobulinas y complemento en las membranas basales glomerulares causa nefropatía aguda. El síndrome nefrótico, que se presenta en pacientes con malaria de cuatro días de evolución, se clasifica como una glomerulopatía por inmunocomplejos.
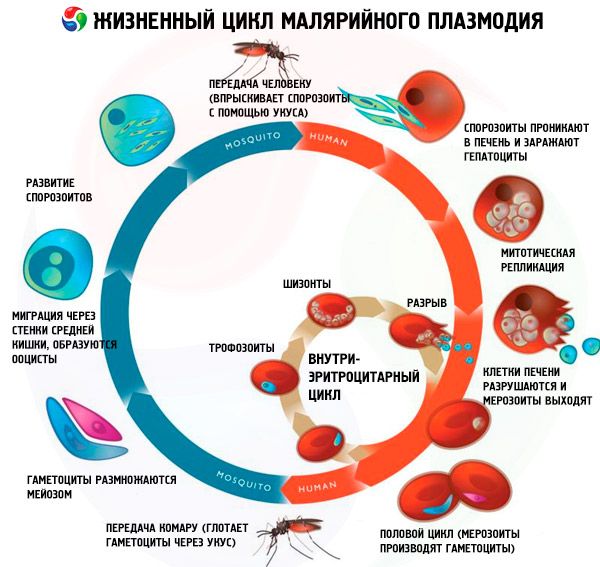
Ciclo de vida de todos los patógenos de la malaria
El ciclo de vida de todos los patógenos de la malaria incluye dos huéspedes: los humanos (esquizogonia - ciclo de desarrollo asexual) y los mosquitos del género Anopheles (esporogonia - ciclo de desarrollo sexual).
Tradicionalmente, se distinguen tres etapas en el ciclo de esquizogonia de todas las especies de parásitos de la malaria: esquizogonia exoeritrocítica (EESh), esquizogonia eritrocítica (ESH) y gametocitogonia. Además, se distingue una etapa separada en los ciclos de vida de Pl. vivax y Pl. ovale —la hibernación— debido a la posible introducción de un grupo morfológicamente heterogéneo de esporozoítos (taquisporozoítos y bradisporozoítos o solo bradisporozoítos) en el cuerpo humano durante la picadura de un mosquito. En estos casos, los bradisporozoítos (hipnozoítos) se conservan en los hepatocitos durante un largo periodo en estado inactivo hasta la aparición de la EES.
 [ 19 ], [ 20 ], [ 21 ], [ 22 ]
[ 19 ], [ 20 ], [ 21 ], [ 22 ]
Esquizogonia exoeritrocítica
Los esporozoítos introducidos en el cuerpo humano con la saliva del mosquito muy rápidamente (en 15-30 minutos) entran al hígado con el torrente sanguíneo, donde penetran activamente en los hepatocitos sin dañarlos. Los esporozoítos de Pl. falciparum, Pl. malariae y los taquisporozoítos de Pl. vivax y Pl. ovale comienzan inmediatamente la EES con la formación de un gran número de merozoítos exoeritrocíticos (hasta 40.000 de un esporozoíto en la malaria falciparum). Los hepatocitos son destruidos y los merozoítos entran de nuevo al torrente sanguíneo con la subsiguiente penetración rápida (en 15-30 minutos) en los eritrocitos. La duración de la EES para la malaria falciparum suele ser de 6 días, para la malaria vivax - 8 días, para la malaria ovafe - 9 días, para la malaria malariae - 15 días.
 [ 23 ], [ 24 ], [ 25 ], [ 26 ], [ 27 ], [ 28 ], [ 29 ]
[ 23 ], [ 24 ], [ 25 ], [ 26 ], [ 27 ], [ 28 ], [ 29 ]
Etapa latente
En la malaria vivax y la malaria ovale, los bradisporozoítos que han penetrado en los hepatocitos se transforman en formas inactivas (hipnozoítos), que pueden permanecer sin dividirse durante varios meses o incluso años hasta su posterior reactivación (división y formación de merozoítos). Por lo tanto, los hipnozoítos se asocian con una incubación prolongada (de hasta 3 a 10 meses o más) y con el desarrollo de recaídas exoeritrocíticas remotas, características exclusivas de estas formas de malaria.
Esquizogonia eritrocitaria
Tras la introducción de los merozoítos en los eritrocitos, los parásitos de la malaria pasan repetidamente (cíclicamente) por las etapas de trofozoíto (célula mononuclear en proceso de alimentación), esquizonte (célula multinuclear en división) y mórula (parásitos formados en el interior del eritrocito). Posteriormente, tras la destrucción de los eritrocitos, los merozoítos entran al plasma sanguíneo. La mayor cantidad de merozoítos hijos se forma en la malaria tropical: hasta 40 por eritrocito. La etapa de ES tiene una duración estrictamente definida: 48 horas para la malaria por P. falciparum, P. vivax y P. ovale, y 72 horas para la malariae.
Características del ciclo esquizogónico eritrocítico y principales mecanismos patogénicos del desarrollo de las formas graves y complicadas del paludismo por P. falciparum:
- acumulación (secuestro) de eritrocitos invadidos que contienen trofozoítos adultos (de la etapa de trofozoíto ameboide), esquizontes en los vasos de los órganos internos, principalmente el cerebro, así como los riñones, el hígado, los intestinos, la médula ósea, la placenta, etc.;
- la formación de las llamadas rosetas, constituidas por eritrocitos invadidos y no infectados;
- desarrollo de trastornos de la microcirculación, hipoxia tisular, acidosis metabólica (acumulación significativa de ácido láctico);
- activación de la MFS (principalmente respuesta inmune Th-1) con aumento de la síntesis de factor de necrosis tumoral-a, interferón y, interleucina-1 y otras citocinas que dañan el endotelio vascular y provocan la adhesión de eritrocitos al endotelio de los vasos sanguíneos.
En los últimos años se ha considerado el papel especial del aumento de la síntesis de óxido nítrico (NO) por las células endoteliales vasculares cerebrales en el desarrollo de la forma cerebral de la malaria por P. falciparum.
Un mecanismo fisiopatológico importante en el desarrollo de formas graves de malaria por P. falciparum, en comparación con otras formas de malaria, es la hipoglucemia, que agrava los trastornos microcirculatorios y metabólicos (acidosis metabólica) en pacientes, especialmente en niños y mujeres embarazadas. Se distinguen tres factores principales en el desarrollo de hipoglucemia en la malaria por P. falciparum: disminución de la glucogénesis hepática, utilización de glucosa por los parásitos y estimulación de la secreción de insulina. Al mismo tiempo, la hipoglucemia puede ser consecuencia de la hiperinsulinemia que se desarrolla tras la administración de quinina para detener los ataques de malaria por P. falciparum.
Como consecuencia de la persistencia prolongada del parásito (sin terapia adecuada) en la malaria-malaria, puede desarrollarse un síndrome nefrótico como resultado de un mecanismo inmunológico (deposición de complejos inmunes que contienen antígenos del parásito en la membrana basal de los glomérulos renales).
Cabe señalar que las principales manifestaciones clínicas de todas las formas de malaria (intoxicación, hepatomegalia y esplenomegalia, anemia) se asocian con la etapa de esquizogonia eritrocitaria (reproducción asexual repetida de parásitos en los eritrocitos), y cuanto mayor sea el contenido de parásitos en 1 μl de sangre de un paciente, determinado mediante microscopía de gota gruesa, más grave suele ser la malaria. Por lo tanto, en el diagnóstico de laboratorio de la malaria, es importante no solo establecer el tipo de plasmodium palúdico, sino también determinar el nivel de parasitemia. Según el nivel máximo de parasitemia, las formas de malaria se distribuyen en orden descendente: malaria falciparum (hasta 100 mil en μl o más), malaria vivax (hasta 20 mil en μl, con menos frecuencia más), malaria ovale y malariae (hasta 10-15 mil en μl). En la malaria falciparum, que se presenta con un alto nivel de parasitemia (100 mil por μl y más), aumenta significativamente el riesgo de desarrollar complicaciones graves y fatales, lo que determina la táctica de una terapia antipalúdica intensiva (parenteral).
La aparición de paroxismos febriles en la malaria se produce por la hemólisis de los eritrocitos, la liberación de merozoitos al plasma, la destrucción de algunos de ellos (la otra parte de los merozoitos se introduce de nuevo en los eritrocitos), la activación del MFS y el aumento de la síntesis de interleucina-1, -6, factor de necrosis tumoral a y otros pirógenos endógenos (citocinas inflamatorias) que afectan al centro de termorregulación del hipotálamo.
En presencia de una generación de plasmodios en la sangre, se presentan paroxismos que se alternan regularmente desde los primeros días de la enfermedad. Con frecuencia, en la malaria por falciparum y vivax (en regiones hiperendémicas con alta transmisión de malaria), las personas no inmunes experimentan una fiebre inicial asociada al desarrollo simultáneo de varias generaciones de patógenos en los eritrocitos de los pacientes, con diferentes momentos al final del ciclo de desarrollo. Esto provoca la estratificación de los ataques, suavizando el período de apirexia y distorsionando el paroxismo típico.
A medida que la enfermedad se desarrolla, los factores de defensa específicos y no específicos aumentan (al final de la 1ª-2ª semana), algunas de las generaciones mueren y una (dos) generaciones líderes de parásitos permanecen con el desarrollo de paroxismos típicos cada dos días (o todos los días).
El agrandamiento del hígado y del bazo en todas las formas de malaria se asocia con un importante llenado de sangre, edema e hiperplasia de la articulación metastásica.
La malaria, por regla general, siempre conduce a una anemia hemolítica hipocrómica, en cuya patogenia son importantes una serie de factores:
- hemólisis intravascular de eritrocitos infectados;
- fagocitosis de eritrocitos infectados y no infectados por las células reticuloendoteliales del bazo;
- secuestro (acumulación) de eritrocitos que contienen parásitos maduros en la médula ósea, supresión de la hematopoyesis;
- mecanismo inmune (destrucción de eritrocitos no afectados como resultado de la adsorción de complejos inmunes que contienen la fracción C-3 del complemento en la membrana del eritrocito).
La etapa de gametocitogonia es una especie de derivación de la etapa de SE. Algunos merozoítos (un proceso determinado genéticamente), en lugar de repetir el ciclo de desarrollo asexual tras su introducción en el eritrocito, se transforman en formas sexuales: gametocitos (masculinos y femeninos).
Características de la fase gametocitogonial en la malaria por P. falciparum:
- Los gametocitos aparecen en la sangre periférica no antes de 10-12 días de la enfermedad;
- Los gametocitos, que se acumulan durante el curso de la enfermedad, pueden circular en el torrente sanguíneo durante mucho tiempo (hasta 4-6 semanas o más).
En otras formas de malaria (vivax, ovale, malariae) los gametocitos pueden detectarse en la sangre periférica desde los primeros días de la enfermedad y mueren rápidamente (en cuestión de horas o días).
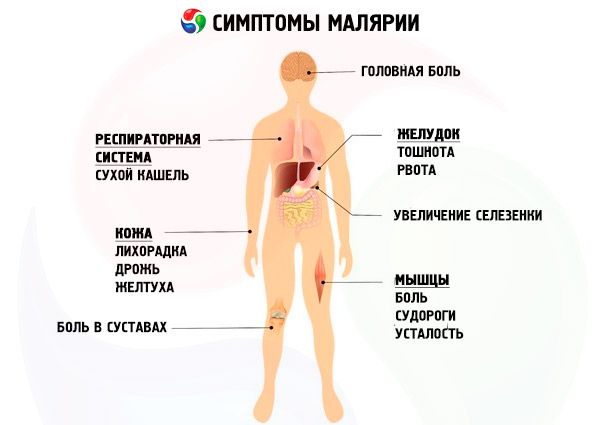
Síntomas malaria
Teniendo en cuenta las características de las especies de parásitos de la malaria y los síntomas correspondientes de la malaria, se distinguen cuatro formas de la enfermedad: malaria de tres días (malaria vivax, malaria tertiana), malaria de cuatro días (malaria quartana), malaria tropical (malaria falciparum, malaria tropica) y malaria ovalada de tres días (malaria ovale).
El curso de la malaria primaria incluye el período inicial de la enfermedad, el período de pico de la enfermedad y la recuperación. Sin tratamiento o con una terapia etiotrópica inadecuada, la malaria entra en un período de recaída. Existen recaídas exoeritrocíticas y eritrocíticas, según el momento de desarrollo: tempranas y tardías. Las recaídas eritrocíticas se observan en la infección por todos los tipos de plasmodios. Las tempranas ocurren dentro de los dos meses posteriores a los ataques primarios; las recaídas que se desarrollan más tarde se consideran tardías. Sin tratamiento o con un tratamiento inadecuado de la malaria de tres días y oval, se produce un período de calma que dura de 6 a 11 meses con la desaparición de los parásitos de la sangre y el bienestar clínico. Luego vienen las recaídas tardías (causadas por la activación de hipnozoítos en el hígado), sustituidas por un período de latencia sin tratamiento, tras el cual la enfermedad reaparece.
P. falciparum vive en el cuerpo humano (sin tratamiento) hasta 1,5 años, P. vivax y P. ovale, hasta 3 años, P. malariae, durante muchos años, a veces de por vida.
¿Qué te molesta?
Formas
Según las recomendaciones de la OMS, la malaria se divide en no complicada, grave y complicada. Las formas malignas de malaria y sus complicaciones son características principalmente de la infección por P. falciparum. La enfermedad causada por P. vivax, P. ovale y P. malariae suele tener un curso benigno.
Malaria de tres días
El período de incubación de la malaria de tres días varía de 10 a 21 días a 6 a 14 meses. Los síntomas prodrómicos de malaria antes del ataque primario son poco frecuentes, pero suelen preceder a las recaídas y se manifiestan con malestar general, debilidad, fatiga, dolor en la región lumbar y las extremidades, un ligero aumento de la temperatura corporal, pérdida de apetito y cefalea. La duración promedio del período prodrómico es de 1 a 5 días.
Al principio, la curva de temperatura es irregular (fiebre inicial), asociada a la liberación asincrónica de varias generaciones de P. vivax en la sangre. Posteriormente, los ataques típicos de malaria comienzan con fiebre intermitente de tres días, lo que indica la formación de la principal generación de parásitos en la sangre. En un ataque febril palúdico, se manifiestan clínicamente tres fases, inmediatamente consecutivas: escalofríos, calor y sudor. Un ataque palúdico comienza con escalofríos, cuya intensidad puede variar desde leves temblores hasta escalofríos intensos. En este momento, el paciente se acuesta, intenta calentarse sin éxito, pero los escalofríos aumentan. La piel se vuelve seca, áspera o con sensación de "piel de gallina" al tacto, fría, y las extremidades y las mucosas visibles están cianóticas. Se observan los siguientes síntomas de malaria: dolor de cabeza intenso, a veces vómitos, dolor en las articulaciones y la región lumbar. La fase de escalofríos dura desde varios minutos hasta una o dos horas, y es sustituida por la fase febril. El paciente se quita la ropa y la ropa interior, pero esto no le produce alivio. La temperatura corporal alcanza los 40-41 °C, la piel se seca y caliente, y la cara se enrojece. El dolor de cabeza, el dolor lumbar y articular se intensifican, y es posible que presente delirio y confusión. La fiebre dura de una a varias horas y es sustituida por un período de sudoración. La temperatura baja drásticamente y la sudoración suele ser profusa, por lo que el paciente debe cambiarse de ropa interior repetidamente. Debilitado por el ataque, se queda dormido rápidamente. La duración del ataque es de 6 a 10 horas. Se considera típico que los ataques comiencen por la mañana y por la tarde. Tras el ataque, comienza un período de apirexia que dura unas 40 horas. Tras 2-3 ataques de fiebre, el hígado y el bazo están claramente aumentados de tamaño. Cambios en la sangre: anemia, que se desarrolla gradualmente a partir de la segunda semana de la enfermedad, leucopenia, neutropenia con desplazamiento de las células en banda hacia la izquierda, linfocitosis relativa, aneosinofilia y aumento de la VSG.
En el curso natural de la enfermedad sin tratamiento etiotrópico, tras 12-14 episodios (4-6 semanas), la intensidad de la fiebre disminuye, los episodios remiten gradualmente y el tamaño del hígado y el bazo disminuye. Sin embargo, tras 2 semanas o 2 meses, se producen recaídas tempranas, caracterizadas por una curva de temperatura sincrónica, un aumento del tamaño del hígado y el bazo, y anemia. Posteriormente, con el desarrollo de la inmunidad, los parásitos desaparecen de la sangre y comienza un período de latencia. Si no se realiza tratamiento con fármacos histoesquizotrópicos en este momento, tras 6-8 meses (y en ocasiones tras 1-3 años), se activan las formas tisulares latentes de los parásitos y se desarrollan recaídas remotas. Estas se caracterizan por un inicio agudo, un curso más leve, un aumento temprano del tamaño del bazo, un número corto de episodios (hasta 7-8), menor intensidad y duración de la parasitemia y la presencia de gametocitos en la sangre.
Paludismo oval
En muchas características clínicas y patogénicas, la malaria ovale es similar a la malaria vivax de tres días. El período de incubación de la malaria ovale es de 11 a 16 días. En esta última, el patógeno tiende a una latencia primaria. El período de incubación puede durar de 2 meses a 2 años o más. Los síntomas de la malaria incluyen fiebre intermitente de tres días, y con menos frecuencia, fiebre diaria. Los ataques febriles suelen ocurrir al anochecer, en lugar de en la primera mitad del día, como es típico en otras formas de malaria. La malaria ovale se caracteriza principalmente por un curso leve con pocos paroxismos que se presentan sin escalofríos pronunciados y con una fiebre más baja en el pico de los ataques. Es característico que los paroxismos durante el ataque primario a menudo cesen espontáneamente. Esto se explica por la rápida formación de una inmunidad estable. Si no se realiza tratamiento con fármacos histoesquizotrópicos, son posibles de 1 a 3 recaídas con un intervalo entre ellas de 17 días a 7 meses.
Cuartana
Generalmente se presenta de forma benigna. El período de incubación es de 3 a 6 semanas. Los síntomas prodrómicos de malaria son poco frecuentes. El inicio de la enfermedad es agudo. Desde el primer ataque, se presenta fiebre intermitente con una periodicidad de ataques cada 2 días. El paroxismo suele comenzar al mediodía y su duración promedio es de unas 13 horas. El período de escalofríos es largo y pronunciado. El período de calor dura hasta 6 horas y se acompaña de cefalea, mialgia, artralgia y, en ocasiones, náuseas y vómitos. En ocasiones, los pacientes presentan inquietud y delirio. En el período interictal, el estado de los pacientes es satisfactorio. La anemia y la hepatoesplenomegalia se desarrollan lentamente, no antes de 2 semanas después del inicio de la enfermedad. Sin tratamiento, se observan de 8 a 14 ataques, pero el proceso de esquizogonia eritrocítica, en un nivel bajo, dura muchos años. Con mayor frecuencia, la infección se presenta como portadora de parásitos sin activación de la esquizogonia eritrocitaria, lo que convierte a estos individuos en donantes potencialmente peligrosos. En focos endémicos, la malaria de cuatro días causa síndrome nefrótico con un pronóstico desfavorable en niños.
Malaria tropical
Es la forma más grave de la infección por malaria. El período de incubación es de 8 a 16 días. Al final de este, algunas personas no inmunes experimentan síntomas prodrómicos de malaria que duran desde varias horas hasta uno o dos días: malestar general, debilidad, fatiga, dolores corporales, mialgia y artralgia, y cefalea. En la mayoría de los pacientes, la malaria tropical comienza de forma aguda, sin período prodrómico, con un aumento de la temperatura corporal de 38 a 39 °C. Si los ciclos de esquizogonia eritrocítica en varias generaciones de P. falciparum en un organismo infectado no terminan simultáneamente, esto suele manifestarse clínicamente por la ausencia de una periodicidad cíclica de ataques febriles. Los ataques, que se presentan con un cambio de fase alternado, comienzan con escalofríos que duran de 30 minutos a una hora. Durante este período, la piel está pálida al examen, fría al tacto, a menudo con una aspereza similar a la piel de gallina. Los escalofríos se acompañan de un aumento de la temperatura corporal de 38 a 39 °C. Con el cese de los escalofríos, comienza la segunda fase del paroxismo: la fiebre. Los pacientes experimentan una ligera sensación de calor, a veces incluso de calor intenso. La piel se vuelve caliente al tacto y el rostro presenta hiperemia. Esta fase dura unas 12 horas y es reemplazada por una sudoración leve. La temperatura corporal desciende a valores normales y subnormales, y al cabo de 1 o 2 horas vuelve a subir. En algunos casos, la malaria tropical se acompaña de náuseas, vómitos y diarrea. En ocasiones, se presentan síntomas catarrales de malaria en las vías respiratorias superiores: tos, rinorrea y dolor de garganta. Posteriormente, se observan erupciones herpéticas en los labios y las alas de la nariz. En la fase aguda, los pacientes notan hiperemia conjuntival; en casos graves, puede acompañarse de petequias o hemorragias subconjuntivales de mayor tamaño.
Durante el pico de la malaria tropical, los escalofríos son menos pronunciados que en los primeros días de la enfermedad, su duración es de 15 a 30 minutos. La fiebre continúa durante días, los períodos de apirexia son raros. En un curso leve de la enfermedad, la temperatura corporal en su pico alcanza los 38,5 °C, la duración de la fiebre es de 3 a 4 días; con un grado de gravedad moderado, 39,5 °C y 6 a 7 días, respectivamente. El curso grave de la enfermedad se caracteriza por un aumento de la temperatura corporal a 40 °C o más, y su duración es de ocho o más días. La duración de los paroxismos individuales (y de hecho la estratificación de varios) en la malaria tropical alcanza las 30 a 40 horas. Predomina el tipo irregular de curva de temperatura, observado con menos frecuencia los tipos remitentes, ocasionalmente intermitentes y constantes.
El agrandamiento del hígado suele determinarse al tercer día de la enfermedad, el agrandamiento del bazo, también a partir del tercer día, pero generalmente se registra solo por percusión; la palpación clara solo es posible al quinto o sexto día. Durante la ecografía de los órganos abdominales, el agrandamiento del hígado y del bazo se determina ya al segundo o tercer día después de que hayan aparecido las manifestaciones clínicas de la malaria tropical. Los trastornos del metabolismo de los pigmentos se observan solo en pacientes con malaria tropical grave y, con menos frecuencia, moderada. Un aumento de más del triple en la actividad de las aminotransferasas séricas se considera un indicador de un pronóstico desfavorable. Los trastornos metabólicos en la malaria tropical incluyen cambios en el sistema de hemostasia e hipoglucemia. Los trastornos cardiovasculares son de naturaleza funcional y se expresan por taquicardia, ruidos cardíacos apagados e hipotensión. Ocasionalmente, se escucha un soplo sistólico transitorio en el ápice del corazón. En las formas graves de la enfermedad, se observan cambios en el ECG en forma de deformación de la parte terminal del complejo ventricular: aplanamiento y configuración inversa de la onda T, y descenso del segmento ST. Simultáneamente, disminuye el voltaje de las ondas R en las derivaciones estándar. En pacientes con la forma cerebral, los cambios en la onda P son de tipo P-pulmonale.
En la malaria tropical se observan a menudo trastornos del SNC asociados a fiebre alta e intoxicación: dolor de cabeza, vómitos, meningismo, convulsiones, somnolencia, a veces síndrome similar al delirio, pero la conciencia del paciente está preservada.
Los signos característicos de la infección por malaria moderada y grave son anemia hemolítica y leucopenia, eosinofilia y neutropenia, y se observa linfocitosis relativa en la fórmula leucocitaria. En las formas graves de la enfermedad, es posible la leucocitosis neutrofílica; la VSG se mantiene constante y significativamente elevada. La trombocitopenia es un signo típico de todos los tipos de malaria. Al igual que con otras enfermedades infecciosas, los pacientes presentan proteinuria transitoria.
La malaria tropical recurrente se debe a un tratamiento etiotrópico inadecuado o a la resistencia de P. falciparum a los agentes quimioterapéuticos utilizados. La evolución natural de la malaria tropical con un pronóstico favorable no dura más de dos semanas. En ausencia de terapia etiotrópica, las recaídas ocurren después de 7 a 10 días.
El embarazo es un factor de riesgo generalmente reconocido para la malaria tropical. Esto se debe a la mayor incidencia del embarazo, la tendencia a formas clínicas graves, el riesgo para la salud y la vida del niño, y un arsenal terapéutico limitado. La malaria tropical en niños menores de cinco años debe considerarse una enfermedad potencialmente mortal. En niños de menor edad (hasta 3-4 años), especialmente en lactantes, la malaria presenta un cuadro clínico único: carece del síntoma clínico más llamativo: el paroxismo palúdico. Al mismo tiempo, se observan síntomas de malaria como convulsiones, vómitos, diarrea y dolor abdominal, con un deterioro progresivo del estado del niño. La aparición de convulsiones y otros síntomas cerebrales no implica necesariamente el desarrollo de malaria cerebral; a menudo, es uno de los síntomas de neurotoxicosis. La parasitemia en niños pequeños suele ser alta: P. falciparum puede afectar hasta el 20% de los glóbulos rojos. La enfermedad puede malignizarse rápidamente y causar la muerte del niño.
Complicaciones y consecuencias
Registrado en todas las etapas de la malaria tropical. Síntomas de malaria con pronóstico desfavorable, que indican la posibilidad de desarrollar una forma maligna: fiebre diaria, ausencia de apirexia entre ataques, cefalea intensa, convulsiones generalizadas recurrentes en más de dos ocasiones en 24 horas, rigidez descerebrada, shock hemodinámico (presión arterial sistólica inferior a 70 mmHg en adultos y inferior a 50 mmHg en niños). Esto también se evidencia por una alta parasitemia (más de 100 mil P. falciparum en 1 μl de sangre), detección de diversos estadios de edad del parásito en sangre periférica, presencia de gametocitos y aumento de la leucocitosis (más de 12,0 x 10⁻¹ /l). También son pronósticos desfavorables la hipoglucemia inferior a 2,2 mmol/L, la acidosis metabólica descompensada, un aumento de más de tres veces de la actividad de las aminotransferasas séricas, así como una disminución del nivel de glucosa en el líquido cefalorraquídeo y un nivel de lactato superior a 6 μmol/L.
Las lesiones graves del SNC en la malaria tropical se agrupan bajo el nombre de "malaria cerebral", y su síntoma principal es el desarrollo de un estado comatoso. El coma palúdico puede ser una complicación de la malaria primaria, recurrente y repetida, pero se observa con mayor frecuencia en la malaria primaria, principalmente en niños, mujeres embarazadas y personas jóvenes y de mediana edad.
La forma cerebral es la complicación más común de la malaria falciparum grave. En las condiciones actuales, se presenta en el 10% de los casos de malaria falciparum en el mundo, y entre el 60% y el 80% de los desenlaces mortales de la enfermedad se asocian con esta complicación. La forma cerebral puede desarrollarse desde los primeros días, pero se registra con mayor frecuencia en la segunda semana de la enfermedad debido a la ausencia de un tratamiento específico o inadecuado. El desenlace mortal puede ocurrir en uno o dos días. En el cuadro clínico de la malaria cerebral se distinguen tres períodos: aturdimiento, estupor y coma verdadero.
La etapa de estupefacción se caracteriza por letargo mental y físico del paciente y agotamiento rápido. Se orienta en el tiempo y el espacio, pero se muestra reticente a establecer contacto, responde preguntas con monosílabos y se cansa rápidamente. Los reflejos tendinosos están conservados.
La fase de sopor se manifiesta por una profunda postración del paciente con raros destellos de consciencia. Es posible que se presente ataxia, amnesia y convulsiones, a veces de naturaleza epileptiforme. Los reflejos corneales están conservados y las pupilas son normales. Los reflejos tendinosos están aumentados y se presentan reflejos patológicos.
En coma, el paciente está inconsciente y no responde a estímulos externos. Se observan trastornos de convergencia, estrabismo divergente, movimientos flotantes de los globos oculares con los párpados abiertos (como si el paciente mirara al techo), nistagmo horizontal y vertical, parálisis del sexto par de nervios craneales; los reflejos tendinosos y abdominales están ausentes, y las funciones vegetativas están gravemente alteradas. Se manifiestan síntomas meníngeos de malaria y reflejos patológicos de Babinski, Rossolimo, etc. Se observa incontinencia urinaria y fecal. Una punción lumbar revela un aumento de la presión intracraneal sin alteraciones pronunciadas en la composición proteica y celular del líquido cefalorraquídeo. Se detecta un alto grado de parasitemia por P. falciparum en diferentes estadios de edad mediante gota gruesa y frotis sanguíneo en pacientes con malaria comatosa. Asimismo, se conocen casos de desenlace fatal por malaria cerebral con niveles muy bajos de parasitemia. La malaria cerebral en niños suele ir acompañada de anemia. La anemia empeora el estado neurológico y somático del niño. Con un tratamiento eficaz, la consciencia suele recuperarse repentinamente.
En la malaria cerebral, las psicosis pueden desarrollarse como consecuencia de cambios distróficos en el parénquima cerebral. En el período agudo, las psicosis se presentan en forma de delirio, amencia, convulsiones epilépticas y estados maníacos. Las psicosis pospalúdicas se caracterizan por depresión, debilidad mental, histeria, síndromes esquizofrénicos y, en niños, retraso temporal del desarrollo mental. En ocasiones, se observan consecuencias remotas de la malaria cerebral: hemiplejía, ataxia, síntomas focales de los nervios craneales, trastornos extrapiramidales, mononeuritis y polineuritis.
Una complicación común de todas las formas de malaria es la anemia hipocrómica. La anemia grave se diagnostica cuando el hematocrito desciende por debajo del 20 % y el nivel de hemoglobina es inferior a 50 g/l. El grado de anemia depende del tipo de parásito, así como de la intensidad y duración de la infección. La gravedad de la malaria en las poblaciones indígenas de países tropicales suele verse agravada por una deficiencia de hierro y ácido fólico en la dieta. Tras los primeros ataques de malaria, puede desarrollarse anemia, que es más pronunciada en la malaria tropical que en otras formas.
El shock tóxico infeccioso (STI) con desarrollo de síndrome de CID es una complicación característica de la malaria falciparum, que se presenta con una parasitemia elevada. El desarrollo de insuficiencia suprarrenal aguda es característico. La evolución del shock tóxico infeccioso en climas cálidos se acompaña de hipovolemia.
El desarrollo de insuficiencia renal aguda suele observarse en casos de malaria maligna y complicada por P. falciparum. Es característico el desarrollo de oliguria y anuria con aumento de creatinina y urea en sangre; el análisis de orina revela proteinuria, cilindruria, piuria y microhematuria pronunciadas.
El síndrome nefrótico es una complicación característica de la malaria, que se caracteriza por un curso lento y de progresión constante, acompañado de edema, hipertensión arterial, proteinuria y desarrollo de insuficiencia renal.
La fiebre hemoglobinúrica es consecuencia de una hemólisis intravascular masiva, tanto con invasión intensa como por el uso de algunos antipalúdicos (quinina, primaquina, sulfonamidas) en personas con deficiencia de la enzima glucosa-6-fosfato deshidrogenasa. En su forma grave, se presenta ictericia intensa, síndrome hemorrágico grave, anemia y anuria, acompañadas de escalofríos, fiebre (40 °C), dolor lumbar, vómitos biliares repetidos y mialgia y artralgia. La orina adquiere un color marrón oscuro debido a la presencia de oxihemoglobina. En casos graves, el número de eritrocitos se reduce a 1 x 10⁻² / l y el nivel de hemoglobina disminuye a 20-30 g/l. En la hemoglobinuria palúdica, la presencia de parásitos en sangre es mínima o nula. Con la retirada rápida del antipalúdico que causó la hemólisis de los eritrocitos, el estado del paciente mejora sin consecuencias graves. En casos graves, debido al desarrollo de insuficiencia renal aguda, el pronóstico puede ser desfavorable. En los últimos años, se ha considerado la naturaleza autoinmune del desarrollo de hemólisis aguda asociada al uso prolongado y frecuente de antipalúdicos (quinina y primaquina). Se observa fiebre alta (con parasitemia leve), orina de color negro, anemia, leucocitosis y aumento de la VSG en el análisis de sangre. La insuficiencia renal progresa rápidamente, lo que puede ser fatal si no se administra el tratamiento adecuado.
La álgida palúdica se caracteriza por manifestaciones clínicas típicas del shock tóxico infeccioso: trastornos hemodinámicos y de la microcirculación, trastornos del sistema de hemostasia, insuficiencia multiorgánica e hipotermia. A diferencia de la malaria cerebral, la consciencia se conserva, aunque posteriormente puede presentarse coma. La álgida puede presentarse en un contexto de edema pulmonar, acidosis metabólica y deshidratación grave. Se observa un alto nivel de parasitemia. El pronóstico depende en gran medida de un tratamiento oportuno y correcto.
El edema pulmonar agudo en pacientes con malaria tropical suele ser mortal. El mecanismo de esta grave complicación no se ha estudiado a fondo. El edema pulmonar puede ser provocado por una rehidratación excesiva, pero también puede desarrollarse en un contexto de presión normal en la circulación pulmonar. Actualmente, la mayoría de los investigadores consideran la insuficiencia respiratoria aguda en la malaria tropical como una manifestación del síndrome de dificultad respiratoria del adulto.
Una complicación rara pero grave de cualquier forma clínica de malaria, con o sin esplenomegalia hiperreactiva, es la rotura esplénica. Esta puede deberse a una torsión del pedículo esplénico con estasis sanguínea aguda y desarrollo de un hematoma subcapsular.
En la malaria tropical son posibles lesiones de la córnea del ojo, iritis, iridociclitis, opacificación del cuerpo vítreo, neuritis óptica, coriorretinitis y hemorragias retinianas; hay reportes de parálisis de los músculos oculares causadas por lesiones de los pares de nervios craneales III, IV y VI, y parálisis de la acomodación.
Recaídas de malaria
El nivel de parasitemia durante una recaída suele ser menor que durante los síntomas primarios de la malaria. Debido al aumento del umbral pirogénico durante el curso de la infección, las manifestaciones clínicas durante una recaída suelen ocurrir con una parasitemia más alta. Las recaídas, por regla general, cursan de forma benigna, con un síndrome tóxico moderadamente expresado y una alternancia regular de paroxismos palúdicos desde el inicio de la recaída; el número de paroxismos es significativamente menor que durante las manifestaciones primarias de la enfermedad. Según el momento de aparición, se distinguen recaídas tempranas (desarrollo de manifestaciones clínicas durante los primeros 2 meses después de las manifestaciones primarias de la malaria) y tardías (después de 2 meses). Según el origen, las recaídas se dividen en eritrocíticas (todas las formas de malaria) y exoeritrocíticas (solo en malaria vivax y ovale).
Diagnostico malaria
El diagnóstico de la malaria se basa en datos epidemiológicos (estancia en un foco de malaria, ausencia o insuficiencia de quimioprofilaxis), en el cuadro clínico de la enfermedad (ataques característicos) y se confirma mediante pruebas de laboratorio.
El diagnóstico de la malaria debe tener en cuenta:
- aparición aguda de la enfermedad, síntomas pronunciados de intoxicación, curso cíclico con ataques alternos de fiebre y períodos de apirexia, agrandamiento del hígado y del bazo, desarrollo de anemia hemolítica progresiva;
- datos de antecedentes epidemiológicos (estancia en zona con alto riesgo de malaria, transfusión sanguínea, drogadicción);
Duración de la malaria, teniendo en cuenta el desarrollo de recaídas con una sola infección y sin terapia etiotrópica adecuada
Forma de malaria |
Duración de la infección |
|
Normal |
Máximo |
|
Malaria-falciparum |
Hasta 1 año |
Hasta 3 años |
Malaria-malariae |
Hasta 2-3 años |
Posible de por vida |
Malaria-vivax y ovale |
Hasta 1,5-2 años |
Hasta 4-5 años |
- resultados de pruebas de laboratorio:
- Resultados del hemograma: disminución de los niveles de hemoglobina, leucopenia, linfomonocitosis, aumento de la VSG;
- Resultados de la microscopía de una gota de sangre gruesa (observación de al menos 100 campos de visión en casos de baja parasitemia): detección de plasmodios y determinación del nivel de parasitemia en 1 µl de sangre (100 campos de visión - 0,2 µl de sangre).
Esto es necesario:
- Para seleccionar el grado de intensidad del tratamiento antipalúdico específico (con un alto nivel de parasitemia en pacientes con malaria tropical, es preferible la administración parenteral de medicamentos).
- Para monitorear la efectividad de una terapia específica.
El nivel de parasitemia también se puede evaluar contando el porcentaje de eritrocitos afectados por cada 100 leucocitos en una gota gruesa de sangre (en este caso, para evaluar el número de parásitos en 1 μl, es necesario conocer el número total de leucocitos y eritrocitos en 1 μl en el paciente);
- Datos microscópicos de un frotis sanguíneo para determinar el tipo de plasmodio. La gota gruesa y el frotis sanguíneo se tiñen mediante el método de Romanovsky-Giemsa.
Como resultado de la acumulación de eritrocitos invadidos que contienen trofozoítos adultos y esquizontes en los vasos de los órganos internos, al examinar una preparación de gota gruesa en casos leves de malaria por P. falciparum, solo se detectan trofozoítos jóvenes (juveniles) en fase anular. La aparición en sangre periférica de eritrocitos invadidos que contienen etapas adultas del desarrollo del parásito (trofozoítos adultos o ameboides, esquizontes) es un signo de laboratorio desfavorable que indica una evolución grave (complicada) de malaria por P. falciparum.
Grados de parasitemia en la malaria
Grados de parasitemia |
Designación convencional |
Número de parásitos en los campos visuales |
El número de parásitos en 1 µl de sangre |
IV |
+ |
1-20 en 100 campos |
5-50 |
III |
+ + |
10-100 en 100 campos |
50-500 |
II |
+ + + |
1-10 en 1 campo |
500-5000 |
I |
+ + + + |
Más de 10 en 1 campo |
Más de 5000 |
En individuos que han tenido un primer contacto (no inmunes) con esta infección, niños pequeños, los primeros ataques pueden ocurrir con una parasitemia muy baja, a veces no detectable al microscopio; esto requiere una nueva prueba de sangre (gota gruesa) después de 6-12 horas, pero no más tarde de 24 horas.
El diagnóstico de laboratorio de la malaria implica el examen microscópico de muestras de sangre (métodos de gota gruesa y frotis fino) teñidas según Romanovsky-Giemsa.
Se realizarán pruebas de malaria a los siguientes pacientes: pacientes febriles con diagnóstico inespecífico durante 3 días durante la temporada epidémica y 5 días durante el resto del año; pacientes con aumentos periódicos y continuos de la temperatura corporal a pesar del tratamiento según el diagnóstico establecido; receptores de sangre con aumento de la temperatura corporal en los últimos 3 meses tras la transfusión; personas que viven en un foco activo, con cualquier aumento de la temperatura corporal. Debe tenerse en cuenta que durante los primeros ataques de malaria, la cantidad de parásitos en la sangre periférica es baja, por lo que es necesario un examen exhaustivo. La malaria con baja parasitemia también se presenta en personas que tomaron antipalúdicos con fines profilácticos (terapia supresora) o fármacos (tetraciclinas, sulfonamidas) con efecto supresor sobre los plasmodios de la malaria antes de la enfermedad. Se recomienda tomar muestras de sangre para análisis tanto durante la fiebre como durante la apirexia. Para detectar parásitos, se examina una gota gruesa, ya que el volumen de sangre que contiene es de 30 a 40 veces mayor que en una gota fina. En caso de alta parasitemia, el patógeno de la malaria se detecta incluso al examinar un frotis fino. Las características morfológicas y las propiedades tintoriales (tinibilidad) de diferentes estadios de edad de las formas asexuales en eritrocitos son claramente distinguibles en un frotis fino. Es necesario determinar el tipo de parásito: esto es especialmente importante para P. falciparum. En la malaria tropical no complicada, P. falciparum se observa en sangre periférica solo en el estadio de trofozoítos jóvenes en forma de anillo. En caso de primoinfección, se detectan estadios más maduros del parásito en sangre periférica cuando la enfermedad tiene un curso maligno grave. La parasitemia aumenta más rápidamente que con la infección por otros tipos de patógenos. Los gametocitos de P. falciparum maduran lentamente, pero viven mucho tiempo (hasta 6 semanas), mientras que los gametocitos de otras especies mueren varias horas después de su maduración. Los gametocitos detectados en la malaria tropical ayudan a determinar la etapa de la enfermedad: en la etapa temprana (con un curso sin complicaciones), solo se detectan trofozoítos anulares; durante la etapa pico, se detectan anillos y gametocitos (con una infección primaria sin tratamiento, esto indica que la malaria dura al menos 10-12 días); en la etapa de recuperación, solo se detectan gametocitos. Durante el tratamiento, el nivel de parasitemia en sangre periférica se determina dinámicamente. Un día después del inicio del tratamiento etiotrópico, debe disminuir en un 25% o más, y al tercer día no debe superar el 25% del valor inicial. La presencia de parásitos en la preparación de sangre al cuarto día después del inicio del tratamiento, siempre que se cumplan todas las condiciones para un tratamiento exitoso, es un signo de la resistencia del patógeno al fármaco utilizado.
En los últimos años, se han utilizado pruebas rápidas (métodos inmunocromatográficos) basadas en la detección de la proteína específica HRP-2a y la enzima pLDH de P. falciparum en focos endémicos para obtener rápidamente una respuesta preliminar. Las pruebas de una de las conocidas pruebas rápidas KAT-PF (KAT MEDICAL, Sudáfrica) han demostrado una alta eficiencia y especificidad con respecto a P. falciparum. La comparación de los resultados de la prueba rápida, la microscopía y la PCR mostró que su eficiencia diagnóstica alcanza el 95-98%. El uso de pruebas rápidas permite conocer el resultado en tan solo 10 minutos. El personal de laboratorio puede dominar la reacción en 1-2 horas. Los métodos rápidos permiten que las personas que viven o viajan a regiones endémicas se autodiagnostiquen; pueden realizarse sobre el terreno. En Rusia, el diagnóstico rápido de la malaria se limita actualmente a estudios clínicos individuales.
En las condiciones modernas, especialmente en estudios masivos, el método de PCR basado en la detección del ADN del parásito de la malaria cobra especial importancia. Este método permite determinar la portación con baja parasitemia y la infección mixta con diferentes tipos de plasmodios, así como diferenciar la recaída de la malaria por P. falciparum resistente a fármacos de la reinfección por P. falciparum. Actualmente, se utiliza principalmente en estudios epidemiológicos.
¿Qué pruebas son necesarias?
Diagnóstico diferencial
El diagnóstico diferencial de la malaria se realiza según la gravedad de las manifestaciones clínicas y su duración. En primer lugar, la malaria se diferencia de las enfermedades que cursan con fiebre prolongada, hepatomegalia y esplenomegalia, y posible desarrollo de anemia: fiebre tifoidea y paratifoidea, brucelosis, leptospirosis, sepsis y linfogranulomatosis. En los primeros 5 días tras el inicio de la enfermedad, un diagnóstico erróneo frecuente de malaria en regiones no endémicas es la gripe (u otras infecciones virales respiratorias agudas).
En los países tropicales de América del Sur, África, Sudeste Asiático e India se realiza el diagnóstico diferencial de la malaria con las fiebres virales hemorrágicas (fiebre amarilla, dengue, etc.).
En la forma cerebral de malaria-falciparum, el diagnóstico diferencial de la malaria se realiza con la encefalopatía (coma) que se desarrolla con diabetes mellitus descompensada, insuficiencia hepática y renal, así como edema e hinchazón del cerebro con meningitis o meningoencefalitis de etiología bacteriana o viral.
¿A quién contactar?
Tratamiento malaria
El tratamiento de la malaria incluye detener los ataques agudos de la enfermedad, prevenir las recaídas y la portación de gametos y restablecer las funciones corporales deterioradas.
Los medicamentos antipalúdicos se dividen en los siguientes grupos dependiendo de su efecto sobre una etapa particular del desarrollo del parásito: agentes hematoesquizotrópicos, eficaces contra las etapas asexuales de eritrocitos de plasmodios; agentes histoesquizotrópicos, eficaces contra las etapas asexuales de tejidos de plasmodios; medicamentos gamotrópicos, que provocan la muerte de los gametocitos en la sangre del paciente o interrumpen la maduración de los gamemonts y la formación de esporozoitos en el cuerpo del mosquito.
Tratamiento etiotrópico
El tratamiento etiotrópico de la malaria en pacientes con malaria debe prescribirse inmediatamente después de establecer un diagnóstico clínico y epidemiológico y tomar sangre para examen parasitológico.
Los fármacos utilizados actualmente pertenecen a seis grupos de compuestos químicos: 4-aminoquinolinas (cloroquina - delagyl, fosfato de cloroquina, nivaquina), quinolinmetanoles (quinina - diclorhidrato de quinina, sulfato de quinina, quinimax, mefloquina), fenantrenometanoles (halfan, halofantrina), derivados de la artemisinina (artesunato, artemeter, arteéter), antimetabolitos (proguanil), 8-aminoquinolinas (primaquina, tafenoquina). Además, se utilizan fármacos antipalúdicos combinados: savarin (cloroquina + proguanil), malarone (atovaquona + proguanil), coartem o riamet (artemeter + lumefantrina).
Si se detecta P. vivax, P. ovale o P. malariae en el paciente, se utilizan fármacos del grupo de las 4-aminoquinolinas, con mayor frecuencia cloroquina (delagyl). El tratamiento de la malaria es el siguiente: los dos primeros días se utiliza el fármaco en una dosis diaria de 10 mg/kg de la base (cuatro comprimidos de delagyl a la vez), el tercer día - 5 mg/kg (dos comprimidos de delagyl) una vez. Hay informes aislados de resistencia de cepas de P. vivax a la cloroquina en Birmania, Indonesia, Papúa Nueva Guinea y Vanuatu. En tales casos, el tratamiento debe realizarse con mefloquina o quinina según el régimen de tratamiento para la malaria no complicada. Los ataques se detienen después de 24-48 horas, y los parásitos desaparecen de la sangre 48-72 horas después del inicio de la ingesta de cloroquina.
Para la cura radical (prevención de recaídas remotas) de la malaria causada por P. vivax o P. ovale, tras finalizar el tratamiento con cloroquina, se utiliza primaquina, un esquizonticida tisular. Se administra durante 14 días a una dosis de 0,25 mg/kg (base) al día. Las cepas de P. vivax resistentes a la primaquina (las denominadas cepas de tipo Chesson) se encuentran en las islas del Pacífico y en países del Sudeste Asiático. En estos casos, uno de los regímenes recomendados es tomar primaquina a una dosis de 0,25 mg/kg al día durante 21 días.
Si se detecta P. falciparum en la sangre de individuos no inmunes en casos leves, los fármacos de elección, según las recomendaciones de la OMS, son mefloquina y derivados de la artemisinina (artemeter, artesunato, arteether); también se puede utilizar halofantrina. En ausencia de mefloquina y halofantrina y/o en presencia de contraindicaciones para el uso de estos fármacos, se prescribe quinina en combinación con antibióticos (tetraciclina, doxiciclina). La tetraciclina se toma 0,5 g dos veces al día durante 7-10 días; puede ser reemplazada con doxiciclina en una dosis diaria de 0,1 g, la duración de la administración es de 7-10 días. En regiones donde P. falciparum es resistente a la mefloquina y la quinina, se recomienda una combinación de preparaciones de mefloquina y artemisinina (artes}nato, artemeter) para el tratamiento de la malaria tropical no complicada. Una combinación de fansidar y artesunato es eficaz en el tratamiento de la malaria tropical sin complicaciones. Los preparados de artemisinina se utilizan ampliamente para tratar la malaria tropical multirresistente en el Sudeste Asiático, varios países de Sudamérica y África. Actúan muy rápidamente tanto en las fases sanguíneas como en los gametocitos. Sin embargo, estos fármacos se eliminan rápidamente del organismo, razón por la cual se producen recaídas de malaria. Es más adecuado prescribirlos en combinación con mefloquina en las siguientes dosis:
- artesunato: 4 mg/kg dos veces al día durante 3 días; mefloquina: 15 mg/kg una vez el día 2 o 25 mg/kg en dos dosis los días 2 y 3;
- artemeter: 3,2 mg/kg una vez al día durante 3 días; mefloquina: 15 mg/kg una vez el día 2 o 25 mg/kg en dos dosis los días 2 y 3.
Esquemas de tratamiento para la malaria no complicada
Esquemas de aplicación |
|||
Preparación |
Primera dosis, mg/kg |
Dosis posteriores, mg/kg (intervalo, h) |
Duración del curso, días |
Cloroquina |
10 (motivos) |
10- 1-2 días 5- 3 días |
3 |
Fansidar (sulfadoxina + pirimetamina) |
2,50-1,25 |
- |
1 |
Quinina, Kinimax, Kinoform |
10 (motivos) |
7.5 (8) |
7-10 |
Mefloquina |
15 (motivos) |
- |
1 |
Halofantrina |
8 (sal) |
8 (6) |
1 |
Artesunato |
4 |
2 (12) |
7 |
Artemeter |
3.2 |
1.6 (24) |
7.0 |
Quinina-tetraciclina |
10.0-1.5 |
10.0 (8)+5.0 (6) |
10.0+7.0 |
Coartem (artemeter + lumefantrina) |
1.3+8 0 |
1.3-8.0 (8) |
3.0 |
Cuando no se ha determinado el tipo de patógeno, se recomienda el tratamiento según los esquemas de tratamiento para la malaria tropical. Si el paciente vomita antes de 30 minutos después de tomar el medicamento antipalúdico prescrito, debe repetir la misma dosis. Si el vómito se produce entre 30 y 60 minutos después de tomar los comprimidos, se prescribe la mitad de la dosis de este medicamento.
Los pacientes con malaria tropical grave deben ser hospitalizados en una unidad de cuidados intensivos o en un departamento de reanimación. La quinina sigue siendo el fármaco de elección para el tratamiento de la malaria tropical grave. En el tratamiento de formas complicadas (malaria cerebral, álgida), la primera dosis (7 mg/kg) de quinina base se administra por vía intravenosa durante 30 minutos. A continuación, se administran otros 10 mg/kg por vía intravenosa por goteo durante 4 horas. De este modo, el paciente recibe 17 mg/kg de quinina base durante las primeras 4,5 horas tras el inicio del tratamiento. Según otro esquema, la dosis inicial de 20 mg/kg de quinina base se administra durante 4 horas. Ambos esquemas son tolerados satisfactoriamente por los pacientes, sin trastornos cardiovasculares ni de otro tipo. Se administra una dosis de mantenimiento de 10 mg/kg de quinina base a intervalos de 8 horas, con una duración de la administración de 1,5 a 2 horas. Se recomienda combinar la quinina con tetraciclina (250 mg cuatro veces al día durante 7 días) o doxiciclina (0,1 g al día durante 7-10 días). Para el tratamiento en niños, se recomienda administrar una dosis de carga (15 mg/kg) de quinina base por vía intravenosa mediante goteo en una solución de glucosa al 5% durante 4 horas. Se administra una dosis de mantenimiento (10 mg/kg) durante 2 horas a intervalos de 12 horas. La misma dosis se utiliza para la administración intramuscular, pero se recomienda diluir la quinina cinco veces en agua destilada y dividirla en dos inyecciones en diferentes glúteos.
El artemeter se utiliza como fármaco alternativo para el tratamiento de la malaria tropical complicada, a una dosis diaria de 3,2 mg/kg el primer día de tratamiento. Durante los seis días siguientes, se administra a una dosis de 1,6 mg/kg por vía intramuscular, en combinación con una dosis de mefloquina.
A los pacientes con formas graves y complicadas de malaria se les prescribe terapia patogénica intensiva. Al realizar la rehidratación, se debe tener cuidado con el edema pulmonar y cerebral, pero la hipovolemia no es menos peligrosa. Si la rehidratación no es eficaz, estos pacientes pueden experimentar insuficiencia de perfusión tisular, acidosis, hipotensión, shock e insuficiencia renal. El desarrollo de anemia no suele ser mortal, pero si el hematocrito se reduce al 15-20%, se deben transfundir glóbulos rojos o sangre completa. En el síndrome de CID se utiliza la transfusión de sangre completa fresca o concentrados de factores de coagulación y plaquetas. En caso de hipoglucemia, se debe administrar una solución de glucosa al 40% por vía intravenosa.
El tratamiento del edema cerebral se basa en la desintoxicación, la deshidratación y el control de la hipoxia cerebral y los trastornos respiratorios (oxigenoterapia, ventilación artificial). Se administran anticonvulsivos según esté indicado. La experiencia en el tratamiento de la malaria cerebral ha demostrado la ineficacia e incluso el peligro del uso de diuréticos osmóticos: dextranos de bajo peso molecular; adrenalina; prostaciclina; pentoxifilina; ciclosporina; sueros hiperinmunes. Tampoco se recomienda la oxigenación hiperbárica.
En caso de insuficiencia renal aguda o insuficiencia renal-hepática aguda, la dosis diaria de quinina debe reducirse a 10 mg/kg debido a la posible acumulación del fármaco, y las soluciones deben administrarse a una velocidad de 20 gotas por minuto. En el período inicial de la insuficiencia renal aguda, se realiza diuresis forzada y, si no hay efecto y la azoemia aumenta, se utiliza hemodiálisis o diálisis peritoneal, que suele dar buenos resultados. En caso de fiebre hemoglobinúrica, se suspende el fármaco que causó la hemólisis. Si es necesario, se sustituye por otros antipalúdicos y se prescriben simultáneamente glucocorticosteroides (prednisolona 1-2 mg/kg) y terapia de desintoxicación.
En caso de rotura del bazo, que generalmente se desarrolla en casos de agrandamiento rápido y significativo del órgano, está indicada una intervención quirúrgica de emergencia.
Para tratar las recaídas de malaria tropical, se selecciona un fármaco no utilizado previamente o se utiliza el anterior, pero en combinación con otros antipalúdicos. La portación de gametos se elimina con primaquina durante 1 a 3 días en dosis terapéuticas normales.
La eficacia del tratamiento contra la malaria se controla mediante el análisis de una gota gruesa de sangre con un recuento de parasitemias en 1 μl. Estos estudios se realizan diariamente del 1.º al 7.º día tras el inicio del tratamiento etiotrópico. Si los parásitos desaparecen durante este periodo, se realizan análisis adicionales de preparaciones de sangre los días 14, 21 y 28 tras el inicio del tratamiento.
Evaluación de la eficacia
La efectividad del tratamiento etiotrópico de la malaria en pacientes con malaria se evalúa mediante tres parámetros: fracaso temprano (FE), fracaso tardío (FL) y tratamiento efectivo.
Tras tomar un medicamento antipalúdico, el paciente puede vomitar (especialmente en niños). Es importante recordar que si el vómito ocurre menos de 30 minutos después de tomar el medicamento, se debe repetir la misma dosis y, después de 30 a 60 minutos, la mitad de la dosis del medicamento utilizado.
Evaluación de la eficacia del tratamiento de la malaria (OMS, 1996)
Falla temprana (FE) |
Empeoramiento o persistencia de los signos clínicos de malaria en presencia de parasitemia durante los primeros 3 días desde el inicio de la terapia específica |
Fallo tardío (LF) |
Reaparición de signos clínicos característicos de la malaria (incluido el desarrollo de un cuadro grave) en presencia de parasitemia desde el 4º al 14º día desde el inicio de la terapia específica |
Eficacia del tratamiento |
Ausencia de parasitemia a los 14 días del inicio de la terapia específica en ausencia de criterios RN y PN |
Tratamiento radical de la malaria
El tratamiento radical de la malaria se realiza simultáneamente con el tratamiento de detención o inmediatamente después del mismo.
- Para la prevención de las recaídas exoeritrocíticas de la malaria vivax y la malaria ovale, con el fin de afectar a los hipozoitos, se prescribe primaquina en dosis de 45 mg (27 mg de base) al día (3 comprimidos) durante 14 días o 6 comprimidos una vez por semana durante 6-8 semanas (en caso de deficiencia de glucosa-6-fosfato deshidrogenasa). El fármaco tafenoquina, un análogo de la primaquina, se encuentra en fase de ensayos clínicos, pero con mayor eficacia clínica y menor frecuencia de efectos secundarios.
- Para prevenir la transmisión de la malaria por P. falciparum (al afectar a los gametocitos), se utiliza primaquina en dosis de 45 mg (27 mg de base) al día (3 comprimidos) durante 3 días. El tratamiento se realiza en regiones endémicas de malaria tropical. Al utilizar Fansidar para el tratamiento de pacientes con malaria por P. falciparum, no se prescribe primaquina debido al efecto eficaz de la pirimetamina, que forma parte de Fansidar, sobre los gametocitos de P. falciparum.
El tratamiento de la malaria falciparum grave o complicada se realiza en unidades de cuidados intensivos. Si no es posible la administración oral de medicamentos, se administra terapia parenteral con uno de los siguientes medicamentos:
- dihidrocloruro de quinina - 10-20 mg/kg (hasta 2,0 g por día) por vía intravenosa en 500 ml de solución de glucosa al 5%, lentamente, 2-3 veces al día hasta que el paciente se recupere de una condición grave, luego uno de los medicamentos orales de acuerdo con el régimen de tratamiento para la malaria falciparum no complicada;
- En las condiciones modernas, en algunos países se utilizan nuevas preparaciones a base de hierbas para tratar las formas graves de malaria falciparum (estas preparaciones no están certificadas en Rusia): Artemeter (Artenam): 160 mg por vía intramuscular el primer día, luego 80 mg durante 6 días; Artesunato: 50 mg por vía intramuscular (por vía intravenosa) 2 veces al día durante 7 días; Artemisinina: 1200 mg por vía intramuscular durante 7 días.
El tratamiento patogénico de la malaria depende de su gravedad y del desarrollo de complicaciones. Se prescriben terapia de desintoxicación, corrección de la acidosis metabólica, hipoglucemia, diuréticos, antihistamínicos, glucocorticosteroides (según indicación), vitaminas, fármacos cardiovasculares y otros. En caso de anuria, se puede realizar diálisis peritoneal. En el tratamiento de la fiebre hemoglobinúrica, en primer lugar, se suspenden los fármacos que causaron la hemólisis y se realiza una transfusión de masa de glóbulos rojos.
Los convalecientes reciben el alta tras completar un ciclo completo de tratamiento parasitológico etiotrópico (interrumpiendo el tratamiento) si presentan 2 o 3 resultados negativos en los análisis de sangre (gota gruesa). Los pacientes con malaria vivax y malaria ovale pueden someterse a un ciclo posterior de tratamiento con primaquina de forma ambulatoria. Los pacientes con malaria son monitoreados durante 1 a 1,5 meses con análisis parasitológicos repetidos de gota gruesa cada 7 a 10 días. Los pacientes con malaria vivax, malaria ovale y malariae son monitoreados durante dos años, con análisis parasitológicos obligatorios de gota gruesa ante cualquier aumento de temperatura.
Prevención
La OMS combate la malaria en todo el mundo en el marco del Programa para Hacer Retroceder la Malaria, adoptado en 1998. Actualmente, la OMS ha establecido un nuevo objetivo para la Región Europea: eliminar la malaria de tres días (P. vivax) para 2010, y la malaria tropical para 2015. El eslabón más importante en el complejo de medidas es la detección y el tratamiento oportunos de las fuentes de infección.
Las medidas preventivas durante el brote se centran en la detección y el tratamiento oportunos de la malaria, así como de los portadores de parásitos (fuentes de infección), y en combatir a los portadores de malaria. Actualmente no existen vacunas eficaces para la inmunización activa contra la malaria.
La profilaxis individual contra la malaria durante la estancia en un foco endémico tiene como objetivo prevenir la infección y prevenir un ataque de malaria. La prevención consiste en tomar medidas de protección contra las picaduras de mosquitos (uso de repelentes, mosquiteros en ventanas y puertas, cortinas de cama y ropa que cubra brazos y piernas al permanecer al aire libre por la tarde y la noche). De acuerdo con las recomendaciones de la OMS, la prevención de un ataque de malaria consiste en tomar medicamentos antipalúdicos. Se recomienda solo para personas no inmunes que viajen a focos con alto riesgo de infección por malaria y falta de acceso a atención médica (distancia de las instituciones médicas, imposibilidad de realizar pruebas rápidas de sangre para la malaria).
La necesidad, duración y frecuencia de uso de los medicamentos se determina únicamente tras consultar con un especialista en enfermedades infecciosas. Es importante identificar las contraindicaciones para el uso de quimioterapia y la presencia de enfermedades concomitantes graves. Las mujeres embarazadas no inmunizadas y los niños pequeños no deben visitar regiones endémicas de malaria.
Dada la alta resistencia de Plasmodium falciparum a la cloroquina, la norma para la prevención de la malaria por Plasmodium falciparum, según lo recomendado por la OMS, es actualmente la mefloquina (250 mg una vez a la semana, 2 semanas antes de partir hacia una región endémica y durante 4 semanas después del regreso). El uso de otros fármacos (doxiciclina, cloroquina en combinación con proguanil, atovaquina en combinación con proguanil, primaquina y otros) lo determinará un especialista en enfermedades infecciosas, teniendo en cuenta la situación epidemiológica de la región de estancia y otros factores mencionados.
Pronóstico
En la mayoría de los casos, la mortalidad se debe a la malaria tropical, o más precisamente, a su forma cerebral, que se presenta en el 10% de los casos graves de malaria falciparum. Los desenlaces mortales por otros tipos de malaria son muy poco frecuentes. Sin embargo, la malaria tropical, con un diagnóstico oportuno y un tratamiento adecuado, culmina en una recuperación completa.
En el caso de pacientes con malaria tropical, se recomienda la observación en el dispensario durante 1 a 1,5 meses y la realización de análisis parasitológicos de sangre con intervalos de 1 a 2 semanas. La observación en el dispensario de pacientes con malaria causada por P. vivax, P. ovale o P. malariae debe realizarse durante dos años. Cualquier aumento de la temperatura corporal requiere análisis de sangre para la identificación temprana de plasmodios palúdicos.

