Médico experto del artículo.
Nuevos artículos
Enfermedad trofoblástica
Último revisado: 07.07.2025

Todo el contenido de iLive se revisa médicamente o se verifica para asegurar la mayor precisión posible.
Tenemos pautas de abastecimiento estrictas y solo estamos vinculados a sitios de medios acreditados, instituciones de investigación académica y, siempre que sea posible, estudios con revisión médica. Tenga en cuenta que los números entre paréntesis ([1], [2], etc.) son enlaces a estos estudios en los que se puede hacer clic.
Si considera que alguno de nuestros contenidos es incorrecto, está desactualizado o es cuestionable, selecciónelo y presione Ctrl + Intro.
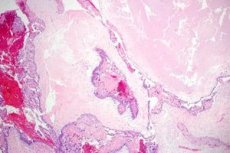
La enfermedad trofoblástica (gestacional) es un término general que designa un espectro de anomalías proliferativas relacionadas con el embarazo derivadas del trofoblasto. Una característica importante de la enfermedad trofoblástica es la formación de quistes lúteos ováricos, que se observa en el 50 % de los casos. La mayoría de las pacientes presentan quistes lúteos bilaterales, que pueden alcanzar grandes tamaños y ocupar toda la cavidad abdominal.
Epidemiología
La incidencia de la enfermedad trofoblástica presenta un patrón geográfico definido, que varía del 0,36 % en países asiáticos al 0,008 % en países europeos (en relación con el número de embarazos). Esta epidemiología se asocia con un deterioro del estado inmunitario de las mujeres con un gran número de embarazos y un intervalo corto entre ellos. Sin embargo, aún no se ha encontrado una explicación exacta para este hecho.
Síntomas enfermedad trofoblástica
El síntoma principal de la enfermedad trofoblástica es que después de la amenorrea se produce un sangrado uterino, a veces acompañado de la liberación de múltiples burbujas con contenido transparente.
Otros síntomas de la enfermedad trofoblástica:
- gestosis temprana grave (náuseas, vómitos), preeclampsia;
- el tamaño del útero excede la edad gestacional esperada;
- durante el examen vaginal - el útero es de consistencia dura y elástica, más largo que el período de embarazo esperado;
- palpación del útero (si es grande, no hay signos del feto);
- ausencia de latidos y movimientos cardíacos fetales;
- ausencia de signos de feto en la cavidad uterina (según datos ecográficos);
- Detección cualitativa y cuantitativa de gonadotropina coriónica humana en orina y sangre (en caso de mola hidatiforme, el nivel de gonadotropina coriónica humana supera su nivel en el embarazo normal entre 50 y 100 veces).
- dolor en el abdomen inferior con desarrollo de coriocarcinoma;
- síntomas causados por la localización predominante de las metástasis tumorales (hemoptisis, síntomas neurológicos, etc.).
Etapa
Clasificación clínica del coriocarcinoma (FIGO, 1992):
- Estadio I: la lesión está limitada al útero, no hay metástasis.
- Estadio II: la lesión se extiende más allá del útero, pero todavía está limitada a los genitales.
- Estadio III: metástasis en los pulmones.
- Estadio IV: lesiones metastásicas de otros órganos.
Formas
La enfermedad trofoblástica incluye:
- mola hidatiforme,
- lunar invasivo (maligno),
- coriocarcinoma,
- tumor trofoblástico del sitio placentario.
 [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
[ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
Mola hidatiforme
La mola hidatiforme se caracteriza por edema y agrandamiento de las vellosidades placentarias con hiperplasia de ambas capas del trofoblasto. Se presenta en dos variantes: completa y parcial; esta última se distingue por la presencia del feto o de sus partes junto con las vellosidades intactas.
La mola invasiva es una mola hidatiforme con invasión miometrial, hiperplasia del trofoblasto y preservación de la estructura de las vellosidades placentarias.
En caso de mola hidatiforme, pueden aparecer quistes lúteos durante las dos primeras semanas. Su presencia constituye un signo de pronóstico desfavorable. La regresión de los quistes lúteos se observa dentro de los tres meses posteriores a la extirpación de la mola hidatiforme.
Tumor trofoblástico del sitio placentario
El tumor trofoblástico placentario surge del trofoblasto del lecho placentario y está constituido principalmente por células citotrofoblasto; puede ser de grado de malignidad bajo o alto.
 [ 16 ]
[ 16 ]
Carcinoma coriónico
El coriocarcinoma asociado al embarazo se origina en el citotrofoblasto y el sinciciotrofoblasto (es decir, en ambas capas del trofoblasto). Se localiza con mayor frecuencia en el útero y puede presentarse tanto durante como después de un embarazo normal o patológico (aborto, aborto espontáneo, parto, mola hidatiforme, embarazo ectópico). En caso de embarazo ectópico, se localiza en la trompa o el ovario, lo cual es extremadamente raro. El coriocarcinoma ovárico puede desarrollarse a partir de células germinales, no está asociado al embarazo y se clasifica como un tumor de células germinales (es decir, no es trofoblástico).
Macroscópicamente, el coriocarcinoma puede ser un tumor nodular localizado en la superficie interna de la cavidad uterina, intermuscularmente, bajo la cubierta serosa o en forma de crecimientos difusos. El tumor es de color púrpura oscuro, de consistencia blanda, no contiene vasos y mide entre 0,5 y 12 centímetros o más. En la mayoría de los casos, se localiza submucosamente.
Microscópicamente, el coriocarcinoma presenta tres histotipos: sincitial, citotrofoblástico y mixto. Sus características incluyen invasión del epitelio coriónico, extensas áreas de necrosis y hemorragia, y grupos aislados de células de Langhans.
Diagnostico enfermedad trofoblástica
El diagnóstico de la enfermedad trofoblástica se basa en los siguientes datos:
- anamnesia;
- examen clínico;
- métodos de investigación radiológica, histológica y hormonal.
Clínicamente importante: anamnesis detallada, examen ginecológico con detección de cianosis de las membranas mucosas de la vagina y del cuello uterino, agrandamiento y dolor del útero, posibles metástasis.
El diagnóstico radiológico incluye la ecografía, la ecografía Doppler, la angiografía, la resonancia magnética (IRM) y la tomografía computarizada (TC).
La ecografía y la dopplerografía son informativas, sencillas, fiables y permiten diagnosticar mola hidatiforme e invasiva, coriocarcinoma, así como metástasis hepáticas, renales y ováricas. Al ser no invasivas e inocuas, son indispensables para monitorizar la eficacia de la quimioterapia. La angiografía con contraste permite un diagnóstico más preciso del coriocarcinoma, especialmente con resultados histológicos negativos del raspado endometrial y de las hormonas trofoblásticas.
Cómo examinar?
¿A quién contactar?
Tratamiento enfermedad trofoblástica
La enfermedad trofoblástica es una de las raras formas de enfermedades malignas, caracterizada por una alta tasa de curación con quimioterapia incluso en presencia de metástasis a distancia.
El principal tratamiento de la enfermedad trofoblástica es la quimioterapia, que se utiliza tanto de forma independiente como en terapias complejas. En el tratamiento complejo de ciertas formas de enfermedad trofoblástica, se emplean la cirugía y la radioterapia.
Principios del tratamiento de la mola hidatiforme
- Aspiración al vacío o extracción de una mola hidatiforme mediante legrado del útero con administración de agentes de contracción uterina (oxitocina intravenosa, etc.).
- Histerectomía por molas hidatiformes grandes, sangrado abundante, falta de condiciones para vaciar el útero; renuencia de la mujer a tener más embarazos. No se extirpan los ovarios con quistes tecalúteos.
- Después de la eliminación del lunar, se realiza una observación durante dos años (controlando el contenido de gonadotropina coriónica humana en la orina una vez al mes).
- La quimioterapia preventiva (metotrexato) después de la evacuación de la mola hidatiforme mediante aspiración al vacío se realiza en los siguientes casos: edad mayor de 40 años, discrepancia entre el tamaño del útero y el período de embarazo esperado, presencia de quistes lúteos durante el período de mola hidatiforme, niveles elevados de gonadotropina coriónica humana superiores a 20.000 UI/ml después de 2-3 evacuaciones o después del tratamiento quirúrgico de la mola invasiva, falta de monitorización dinámica de los niveles de gonadotropina coriónica humana.
Principios del tratamiento del coriocarcinoma
- Quimioterapia de primera línea (metotrexato, actinomicina D, clorambucilo, 6-mercaptopurina, adriamicina, fármacos con platino y alcaloides).
- Tratamiento quirúrgico. Indicaciones: sangrado uterino profuso, tendencia tumoral a la perforación, útero grande, resistencia tumoral a la quimioterapia. Volumen de la cirugía: en mujeres jóvenes con un tumor sin metástasis: extirpación del útero sin apéndices; después de los 40 años: extirpación del útero con apéndices.
- El alta se realiza después de 3 pruebas negativas de gonadotropina coriónica humana, realizadas con intervalos de 1 semana.
- Observación. Determinación del título de gonadotropina coriónica humana (cada 2 semanas) durante 3 meses, y posteriormente cada 6 meses durante 2 años. Radiografía de tórax cada 3 meses (durante un año). Se recomienda el uso de anticonceptivos orales combinados (AOC) durante un año.
La elección del régimen de tratamiento se realiza actualmente teniendo en cuenta el grado de riesgo de desarrollar resistencia tumoral a la quimioterapia según la escala de la OMS.
Según la escala de la OMS, existen 3 grados de riesgo de desarrollo de resistencia: bajo (suma de puntos menor a 5), moderado (5-7 puntos) y alto (8 puntos o más).
En caso de bajo riesgo de resistencia tumoral a la quimioterapia (ausencia de metástasis, tumor uterino pequeño (hasta 3 cm), tamaño reducido de hCG en suero y duración de la enfermedad inferior a 4 meses), se administra monoquimioterapia de primera línea con metotrexato o dactinomicina. La eficacia de la monoquimioterapia oscila entre el 68,7 % y el 100 %.
El primer signo de resistencia tumoral a la quimioterapia es la ausencia de disminución o aumento de la hCG sérica en dos pruebas repetidas con un intervalo de 1 semana.
Escala de la OMS para determinar la resistencia del coriocarcinoma a la quimioterapia
Factor de riesgo |
Número de puntos |
|||
0 |
1 |
2 |
3 |
|
Edad, años |
Hasta 39 |
Más de 39 |
||
Resultado de un embarazo anterior |
Mola hidatiforme |
Aborto provocado |
Parto |
|
Intervalo*, mes |
Menos de 4 |
4-6 |
7-12 |
Más de 12 |
Nivel de HCG, UI/L |
Menos de 10** |
10 3 -01 4 |
10 4 -10 5 |
Más de 10 5 |
Grupo sanguíneo |
0 o A |
B o AB |
||
Tumor más grande, incluido el tumor uterino |
Menos de 3 cm |
3-5 centímetros |
Más de 5 cm |
|
Localización de metástasis |
Bazo, riñón |
Tracto gastrointestinal, hígado |
Cerebro |
|
Número de metástasis |
1-3 |
4-8 |
Más de 8 |
|
Quimioterapia previa |
1 droga |
2 citostáticos o más |
||
- * El intervalo entre el final del embarazo anterior y el inicio de la quimioterapia.
- ** Pueden presentarse niveles bajos de gonadotropina coriónica humana en casos de tumores trofoblásticos en el sitio de la placenta.
Para el tratamiento de pacientes con formas resistentes de tumores, se utilizan diversos regímenes de quimioterapia (2ª línea) con un aumento de la dosis de los medicamentos administrados y de la frecuencia de los cursos.
En caso de riesgo moderado y alto de desarrollo de resistencia tumoral (presencia de metástasis, tamaño del tumor mayor a 3 cm, alto nivel de gonadotropina coriónica humana, duración de los síntomas mayor a 4 meses, inicio de la enfermedad inmediatamente después del parto), se utiliza poliquimioterapia combinada según varios regímenes: MAC (metotrexato, dactinomicina, clorambucina); EMA-CO (etopósido, dactinomicina, metotrexato, vincristina, ciclofosfamida, leucovorina), SNAMOSA (hidroxiurea, dactinomicina, metotrexato, leucovorina, vincristina, ciclofosfamida, doxorrubicina); PVB (cisplatino, vinblastina, bleomicina), EHMMAC (etopósido, hidroxiurea, dactinomicina, metotrexato, vincristina). La combinación más efectiva y menos tóxica de medicamentos de segunda línea es el régimen EMA-CO.
Para el tratamiento de focos tumorales resistentes, es fundamental combinar su extirpación quirúrgica con quimioterapia de segunda línea. En caso de metástasis cerebrales distantes, se realiza poliquimioterapia combinada con radioterapia cerebral completa; la radioterapia es posible en caso de metástasis en el parametrio.
Por lo tanto, la cirugía y la radioterapia son métodos de tratamiento adicionales.
Medicamentos
Prevención
El seguimiento de las pacientes tras una mola hidatiforme se realiza durante 4 años. Su objetivo es el diagnóstico precoz de un posible coriocarcinoma e incluye: monitorización del ciclo menstrual, anticoncepción durante 2 años, exploración general y ginecológica, determinación de la concentración sérica de hCG cada 2 semanas hasta la normalización de los indicadores, y posteriormente cada 6 semanas durante los primeros seis meses y cada 8 semanas durante los 6 meses siguientes.
Una vez cada 4 meses: durante el segundo año y una vez al año durante el tercero y cuarto año; ecografía de los órganos pélvicos y radiografía de tórax 2 semanas después de la evacuación de la mola hidatiforme y posteriormente una vez al año durante los dos primeros años. Se recomiendan los siguientes periodos de observación para pacientes que recibieron quimioterapia preventiva después de una mola hidatiforme: los primeros 3 meses: una vez cada 2 semanas, luego mensualmente durante 3 meses y, posteriormente, según el esquema especificado.
El seguimiento de las pacientes con coriocarcinoma se realiza durante 5 años e incluye un menograma, anticoncepción durante 2 años, una exploración general con examen de las glándulas mamarias, una exploración ginecológica, determinación de la concentración sérica de hCG mensualmente durante el primer año, trimestralmente durante el segundo año, cuatrimestralmente durante el tercer año, dos veces al año durante el cuarto y quinto año, y posteriormente una vez al año. Ecografía de los órganos pélvicos y radiografía o tomografía computarizada pulmonar cada dos meses durante el primer año y posteriormente una vez al año durante el seguimiento.

