Médico experto del artículo.
Nuevos artículos
Meningitis criptocócica
Último revisado: 12.07.2025

Todo el contenido de iLive se revisa médicamente o se verifica para asegurar la mayor precisión posible.
Tenemos pautas de abastecimiento estrictas y solo estamos vinculados a sitios de medios acreditados, instituciones de investigación académica y, siempre que sea posible, estudios con revisión médica. Tenga en cuenta que los números entre paréntesis ([1], [2], etc.) son enlaces a estos estudios en los que se puede hacer clic.
Si considera que alguno de nuestros contenidos es incorrecto, está desactualizado o es cuestionable, selecciónelo y presione Ctrl + Intro.
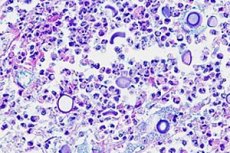
La inflamación de las meninges puede ser causada no solo por bacterias, virus y protistas, sino también por infecciones fúngicas. La meningitis criptocócica es causada por el hongo levaduriforme encapsulado Cryptococcus neoformans, un patógeno oportunista del ser humano. [ 1 ] Se le denominó enfermedad de Busse-Buschke debido a su primera descripción por Otto Busse y Abraham Buschke en 1894. [ 2 ]
Según la CIE-10, el código de la enfermedad es G02.1 (en la sección de enfermedades inflamatorias del sistema nervioso central), y también B45.1 en la sección de micosis (es decir, enfermedades fúngicas).
Epidemiología
Ocho de cada diez casos de meningitis criptocócica ocurren en personas infectadas con VIH/SIDA.
Según datos publicados en The Lancet Infectious Diseases en la primavera de 2017, el hongo causa alrededor de 220.000 casos de meningitis criptocócica al año en personas con VIH o sida, y más de 180.000 fallecen. La mayoría de los casos de meningitis criptocócica se producen en el África subsahariana.
Según las estadísticas de la OMS, en 2017 se registraron 165,8 mil casos de meningitis criptocócica en África, 43,2 mil en países asiáticos, 9,7 mil en América del Norte y del Sur y 4,4 mil casos de la enfermedad en países europeos.
Causas meningitis criptocócica
Las causas de este tipo de meningitis son la infección por el hongo Cryptococcus neoformans (clase Tremellomycetes, género Filobasidiella), que habita en el medio ambiente: en el suelo (incluido el polvo), en madera en descomposición, en los excrementos de aves (palomas) y murciélagos, etc. La infección se produce por vía aérea, al inhalar basidiosporas del hongo en aerosol, aunque en la mayoría de las personas con inmunidad suficiente, C. neoformans no se propaga y permanece como un microorganismo oportunista intracelular facultativo (que no puede infectar a otras personas). Lea también: Criptococos: agentes causantes de la criptococosis [ 3 ].
Por regla general, la meningitis criptocócica se desarrolla en individuos infectados por VIH (estadio IVB), como una infección secundaria, así como en personas con un sistema inmunológico deficiente y en otras enfermedades acompañadas de inmunosupresión a largo plazo. [ 4 ]
La meningitis criptocócica se considera una forma cerebral o extrapulmonar de criptococosis, que se desarrolla después de la diseminación hematógena de C. neoformans desde el tracto respiratorio y los pulmones hasta el cerebro y la médula espinal.[ 5 ]
Factores de riesgo
Los factores que aumentan el riesgo de desarrollar meningitis criptocócica incluyen:
- período neonatal (período del recién nacido) y prematuridad de los bebés;
- debilitamiento del sistema inmunológico en enfermedades oncológicas (incluyendo leucemia, melanoma múltiple, linfosarcoma), en pacientes con infección por VIH y SIDA;
- diabetes;
- hepatitis viral y otras enfermedades causadas por complejos inmunes;
- anemia de células falciformes;
- quimioterapia en presencia de diagnóstico oncológico;
- exceder el nivel permisible de radiación ionizante;
- tratamientos prolongados con antibióticos o esteroides;
- instalación de catéteres y derivaciones intravasculares;
- trasplante de médula ósea o de órganos internos.
Patogenesia
Los criptococos, protegidos de las células inmunes humanas por una cápsula de polisacárido (que inhibe la fagocitosis), secretan proteasas, ureasa, fosfolipasa y nucleasa, enzimas capaces de destruir las células huésped. [ 6 ]
Y la patogénesis de la criptococosis radica en el hecho de que estas enzimas dañan las células lisando las membranas, modificando las moléculas, alterando las funciones de los orgánulos celulares y cambiando el citoesqueleto. [ 7 ]
Las serina proteasas fúngicas destruyen los enlaces peptídicos de las proteínas celulares, escinden inmunoglobulinas y proteínas de las células efectoras inmunes, y la replicación de C. neoformans ocurre dentro de los fagocitos mononucleares (macrófagos), lo que facilita su propagación. [ 8 ]
Además, al atravesar las células endoteliales y ser transportados al interior de los macrófagos infectados, los criptococos alteran la integridad de la barrera hematoencefálica (BHE). El hongo se propaga por el torrente sanguíneo al líquido cefalorraquídeo y luego a las membranas blandas del cerebro, formando colonias de células fúngicas en el tejido cerebral en forma de pseudoquistes gelatinosos. [ 9 ]
Síntomas meningitis criptocócica
Los primeros signos de la meningitis criptocócica son fiebre (la temperatura sube hasta +38,5-39°C) y fuertes dolores de cabeza.
Los síntomas clínicos también incluyen náuseas y vómitos, convulsiones, rigidez del cuello, mayor sensibilidad de los ojos a la luz y alteraciones de la conciencia y el comportamiento. [ 10 ]
Según señalan los expertos, el desarrollo del síndrome meníngeo es más lento que el de la infección bacteriana de las meninges.
Complicaciones y consecuencias
Las complicaciones y consecuencias de la meningitis fúngica causada por criptococo son:
- aumento significativo de la presión intracraneal;
- daño aislado de los nervios craneales con paresia/parálisis del nervio facial y cambios atróficos en el nervio óptico (que conducen a problemas oftalmológicos);
- la propagación del proceso inflamatorio a los tejidos de la subcorteza y los hemisferios del cerebro - meningoencefalitis criptocócica;
- desarrollo de absceso cerebral (criptococoma);
- derrame en el espacio subdural (debajo de la duramadre del cerebro);
- lesión de la médula espinal;
- cambios mentales y disminución de las funciones cognitivas.
Diagnostico meningitis criptocócica
Además de la historia clínica y el examen físico, el diagnóstico de la infección por C. neoformans en la meningitis incluye necesariamente análisis de sangre: clínicos y bioquímicos generales, análisis de suero sanguíneo para anticuerpos contra proteínas de C. neoformans y hemocultivo.
Se realiza una punción lumbar y se realizaun análisis del líquido cefalorraquídeo para antígeno y un análisis bacterioscópico (cultivo bacteriano) del líquido cefalorraquídeo. [ 11 ]
El diagnóstico instrumental se realiza mediante radiografía de tórax y resonancia magnética del cerebro.
Diagnóstico diferencial
El diagnóstico diferencial incluye meningitis y meningoencefalitis de etiología bacteriana y viral, daño cerebral por hongos Histoplasma capsulatum, Coccidioides immitis, Blastomyces dermatidis o amebas (incluida Naegleria fowleri).
Tratamiento meningitis criptocócica
El tratamiento etiológico está dirigido a erradicar los criptococos, para lo cual se utilizan fármacos antifúngicos.
El régimen de tratamiento incluye la administración intravenosa (goteo, a través de un catéter venoso central o por infusión peritoneal) del antibiótico antifúngico poliénico anfotericina B (Amphocyl) en combinación con el fármaco antifúngico flucitosina (5-fluorocitosina) o fluconazol, que posee un efecto fungicida y fungistático. La dosis de estos fármacos se calcula en función del peso corporal del paciente.
Es necesario un control constante del estado del paciente, ya que la anfotericina B tiene un efecto tóxico sobre los riñones y los efectos secundarios de la flucitosina pueden incluir la supresión de la función hematopoyética de la médula ósea, paro respiratorio o cardíaco, desarrollo de lesiones cutáneas en forma de necrólisis epidérmica, etc.
Según las recomendaciones publicadas en la actualización de 2010 de la IDSA (Sociedad Americana de Enfermedades Infecciosas), el tratamiento no ha cambiado en diez años. El tratamiento antifúngico de primera línea se basa en la inducción, consolidación y mantenimiento de los siguientes tres tipos de pacientes: [ 12 ]
Enfermedades relacionadas con el VIH
- Terapia de inducción
- Desoxicolato de anfotericina B (0,7-1,0 mg/kg/día) + flucitosina (100 mg/kg/día por vía oral) durante 2 semanas (Evidencia A1)
- Anfotericina B liposomal (3-4 mg/kg/día) o anfotericina B en complejo lipídico (5 mg/kg/día; monitorizar la función renal) + flucitosina (100 mg/kg/día) durante 2 semanas (Evidencia B2)
- Desoxicolato de anfotericina B (0,7 a 1,0 mg/kg/día) o anfotericina B liposomal (3 a 4 mg/kg/día) o complejo lipídico de anfotericina B (5 mg/kg/día, para pacientes que no toleran la flucitosina) durante 4 a 6 semanas (Evidencia B2)
- Alternativas a la terapia de inducción
- Anfotericina B desoxicolato + fluconazol (Evidencia B1)
- Fluconazol + flucitosina (Evidencia B2)
- Fluconazol (Evidencia B2)
- Itraconazol (Evidencia C2)
- Fluconazol (400 mg/día) durante 8 semanas (Datos A1)
- Fluconazol (200 mg/día) durante 1 o más años (Evidencia A1)
- Itraconazol (400 mg/día) durante 1 o más años (Evidencia C1)
- Desoxicolato de anfotericina B (1 mg/kg/semana) durante 1 año o más (Evidencia C1)
- Terapia de consolidación
- Terapia de apoyo
- Alternativas a la terapia de mantenimiento
Enfermedades relacionadas con el trasplante
- Terapia de inducción
- Anfotericina B liposomal (3-4 mg/kg/día) o complejo lipídico anfotericina B (5 mg/kg/día) + flucitosina (100 mg/kg/día) durante 2 semanas (Evidencia B3)
- Alternativas a la terapia de inducción
- Anfotericina B liposomal (6 mg/kg/día) o anfotericina B en complejo lipídico (5 mg/kg/día) durante 4-6 semanas (Evidencia B3)
- Desoxicolato de anfotericina B (0,7 mg/kg/día) durante 4-6 semanas (Evidencia B3)
- Fluconazol (400 a 800 mg/día) durante 8 semanas (Evidencia B3)
- Fluconazol (200 a 400 mg/día) durante 6 meses a 1 año (Evidencia B3)
- Terapia de consolidación
- Terapia de apoyo
Enfermedad no relacionada con el VIH/trasplante
- Terapia de inducción
- Desoxicolato de anfotericina B (0,7 a 1,0 mg/kg/día) + flucitosina (100 mg/kg/día) durante 4 semanas o más (Evidencia B2)
- Desoxicolato de anfotericina B (0,7–1,0 mg/kg/día) durante 6 semanas (Evidencia B2)
- Anfotericina B liposomal (3-4 mg/kg/día) o anfotericina B en complejo lipídico (5 mg/kg/día) en combinación con flucitosina, 4 semanas (Evidencia B3)
- Desoxicolato de anfotericina B (0,7 mg/kg/día) + flucitosina (100 mg/kg/día) durante 2 semanas (Evidencia B2)
- Terapia de consolidación
- Fluconazol (400 a 800 mg/día) durante 8 semanas (Evidencia B3)
- Fluconazol (200 mg/día) durante 6-12 meses (Evidencia B3)
- Terapia de apoyo
La combinación de anfotericina B y flucitosina ha demostrado ser la más eficaz para eliminar la infección y ha mostrado un mayor beneficio en la supervivencia que la anfotericina sola. Sin embargo, debido a su coste, la flucitosina suele no estar disponible en entornos con recursos limitados donde la carga de la enfermedad es alta. Se han estudiado combinaciones de anfotericina B y fluconazol, que han mostrado resultados superiores a la anfotericina B sola.[ 13 ], [ 14 ], [ 15 ]
Sin tratamiento, el curso clínico progresa a confusión, convulsiones, disminución del nivel de conciencia y coma.
La cefalea refractaria a los analgésicos puede tratarse con descompresión espinal tras una evaluación neuroimagen adecuada con TC o RM. No se conoce con certeza el volumen máximo seguro de LCR que se puede drenar con una sola punción lumbar, pero a menudo se extraen hasta 30 ml controlando la presión después de cada 10 ml extraídos.[ 16 ]
Prevención
La prevención de la infección con el hongo Cryptococcus neoformans es necesaria, en primer lugar, en casos de un sistema inmunológico débil. [ 17 ] Se recomienda evitar lugares polvorientos y trabajar con tierra, y las personas infectadas por el VIH deben recibir terapia antirretroviral continua.
Pronóstico
Sin tratamiento, el pronóstico de cualquier meningitis fúngica es malo.
El pronóstico inicial depende de predictores de mortalidad como los siguientes [ 18 ], [ 19 ]:
- La presión de apertura del líquido cefalorraquídeo es superior a 25 cm H2O.
- Recuento bajo de glóbulos blancos en el líquido cefalorraquídeo
- Discapacidad sensorial
- Diagnóstico tardío
- Títulos elevados de antígenos en el líquido cefalorraquídeo
- Tasa de eliminación de la infección
- La cantidad de levadura en el LCR supera los 10 mm3 ( práctica común en Brasil) [ 20 ]
- Pacientes no relacionados con el VIH y factores pronósticos en estos pacientes, además de los ya mencionados:
- Marcadores de una respuesta inflamatoria débil
- Sin dolores de cabeza
- Neoplasia maligna hematológica primaria
- Enfermedad renal o hepática crónica
La mortalidad varía de un país a otro según los recursos disponibles. Se mantiene alta en Estados Unidos y Francia, con tasas de mortalidad a las 10 semanas que oscilan entre el 15 % y el 26 %, e incluso más altas en pacientes sin VIH debido al diagnóstico tardío y a respuestas inmunitarias disfuncionales. Por otro lado, en países con recursos limitados, la mortalidad aumenta del 30 % al 70 % a las 10 semanas debido a la presentación tardía y la falta de acceso a medicamentos, tensiómetros y una monitorización óptima.

