Médico experto del artículo.
Nuevos artículos
Síndrome de hiperestimulación ovárica
Último revisado: 23.04.2024

Todo el contenido de iLive se revisa médicamente o se verifica para asegurar la mayor precisión posible.
Tenemos pautas de abastecimiento estrictas y solo estamos vinculados a sitios de medios acreditados, instituciones de investigación académica y, siempre que sea posible, estudios con revisión médica. Tenga en cuenta que los números entre paréntesis ([1], [2], etc.) son enlaces a estos estudios en los que se puede hacer clic.
Si considera que alguno de nuestros contenidos es incorrecto, está desactualizado o es cuestionable, selecciónelo y presione Ctrl + Intro.
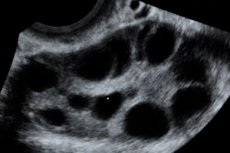
El síndrome de hiperestimulación ovárica (SHO) - complicación iatrogénica en base a la respuesta ovárica hiperérgica no controlada en la administración de gonadotropinas en ciclos y programas de tecnologías de reproducción asistida inducción de la ovulación.
El síndrome puede manifestarse después de la inducción de la ovulación con clomifeno o al inicio del embarazo en un ciclo espontáneo.
 [1],
[1],
Epidemiología
La frecuencia del síndrome de hiperestimulación ovárica varía de 0.5 a 14% con diferentes esquemas de estimulación de la ovulación y no tiende a disminuir. La enfermedad avanza con diversos grados de gravedad y puede causar la muerte en relación con el desarrollo de complicaciones tromboembólicas o SDRA. La letalidad esperada es de 1 para 450-500 mil mujeres. Las formas pesadas del síndrome, que requieren hospitalización en la unidad de cuidados intensivos, se cumplen en 0.2-10%. Según el Registro Nacional Ruso de Métodos de Tecnologías Reproductivas Asistenciales, la frecuencia de hipoxia aguda en 2004 fue del 5,6%.
Causas del síndrome de hiperestimulación ovárica
Factores de riesgo para el desarrollo del síndrome de hiperestimulación ovárica:
- menor de 35 años,
- asténico,
- la presencia de ovarios poliquísticos o multifoliculares,
- maduración de más de diez folículos en el protocolo de estimulación de la ovulación,
- uso de agonistas de la hormona liberadora de gonadotropina y altas dosis de gonadotropinas,
- el inicio del embarazo,
- soporte de fase lútea con drogas HG,
- enfermedades alérgicas
¿Cómo se desarrolla el síndrome de hiperestimulación ovárica?
Síndrome de hiperestimulación ovárica se produce en un contexto de anormalmente alta concentración de las hormonas sexuales en el plasma sanguíneo, que afectan adversamente a las funciones de los diversos sistemas del cuerpo, principalmente en los ovarios, y caracteriza el aumento en el tamaño de los ovarios, a veces hasta 20-25 cm de diámetro, con la formación de ellos y folicular quistes lúteos en el contexto de edema pronunciado del estroma. A partir factor de síndrome de desarrollo - la introducción de dosis ovulatoria de la gonadotropina coriónica humana. El desarrollo síndrome de base es el fenómeno de "aumentar la permeabilidad vascular", lo que conduce a un fluido de salida masiva, rica en proteínas, en el espacio tercero, intersticio y su fideicomiso hipovolemia desarrollo, desequilibrios hemoconcentración, oliguria, hipoproteinemia, electrolitos, aumento de la actividad de las enzimas hepáticas, la formación de ascitis, hidrotórax, hidropericardio con síntomas de shock hipovolémico, o sin ellos. Sin embargo, el "factor X" que conduce a la transudación de fluidos sigue siendo desconocido. En casos severos, ocurren anasarca, artritis, complicaciones tromboembólicas, SDRA.
Actualmente, el síndrome de hiperestimulación ovárica se considera desde el punto de vista de SIRS, contra la cual no es una masiva pacientes daño endotelial con SHO en trasudado peritoneal descubrieron altas concentraciones de interleucinas (IL-1, IL-2, IL-6, IL-8), factor de necrosis tumoral (TNF-a, TNF-(3) el aumento de la síntesis de prostaglandinas ovario, neovascularización de ovario y de la permeabilidad vascular. Bajo la acción de citoquinas proinflamatorias se produce la activación sistémica de la coagulación. Tamaño se correlaciona con la severidad leucocitosis SIRS. Daños en el sistema de órganos debido a fenómenos meteorológicos extremos similares a las lesiones que se producen en la sepsis. El papel de los factores microbianos en oveja y su contribución al desarrollo de SIRS están discutiendo actualmente. Se cree que los microorganismos que colonizan el intestino, tracto urinario, pueden penetrar más allá de los límites de su entorno y tiene un efecto en el cuerpo, similar al de la sepsis.
Síntomas del síndrome de hiperestimulación ovárica
La gravedad del síndrome está directamente relacionada con la gravedad de los trastornos hemodinámicos que determinan el cuadro clínico. La aparición del síndrome puede ser gradual con el aumento de los síntomas, y repentina (aguda), en el que durante varias horas hay una redistribución agudo de fluidos corporales en la acumulación de cavidades serosas. Cuando el síndrome manifestación hay quejas de debilidad, mareo, dolor de cabeza, parpadear "moscas" ante los ojos, dificultad para respirar en reposo y de esfuerzo, tos seca, peor acostado, boca seca, náuseas, vómitos, diarrea, distensión abdominal, sensación tensión, dolor abdominal a menudo sin localización clara, micción rara, fiebre, hinchazón de la vulva y las extremidades inferiores.
Los pacientes con el síndrome de hiperestimulación ovárica pueden desarrollar insuficiencia respiratoria debido a la movilidad limitada debido a la luz ascitis, agrandamiento de los ovarios o la presencia de derrame pleural. Durante SHO grave en fase de demostración podría complicar hidrotórax aguda, síndrome de dificultad respiratoria aguda, embolia pulmonar, OL, atelectasia y hemorragia intraalveolar. El derrame pleural se diagnostica en aproximadamente el 70% de las mujeres con síndrome de hiperestimulación ovárica moderada y grave, con la efusión puede ser unilateral o bilateral en la naturaleza y se produce en un contexto de ascitis. Si SHO describe el desplazamiento y la compresión de los órganos del mediastino como resultado del derrame pleural masivo a mano con el desarrollo de shock y muerte en las mujeres con síndrome de hiperestimulación ovárica y el hidrotórax debido a OB, hemorragia masiva en el lumen de los alvéolos.
Trastornos hemodinámicos. Con HSH de hipotensión arterial de grado medio y grave, taquicardia.
Ascitis El abdomen está hinchado, a menudo tenso, doloroso en todas partes, pero más a menudo en el hipogastrio en la proyección de los ovarios.
Deterioro de la función renal y hepática. Micción diferida observada, oliguria, anuria, hepatomegalia.
El curso de la enfermedad coronaria en el 80% de los pacientes con síndrome severo se acompaña de fiebre. En el 20% de las mujeres, la fiebre ocurre contra la infección del tracto urinario, el 3.8% - debido a la neumonía, el 3.3% - infección del tracto respiratorio superior. La tromboflebitis catéter intravenoso de montaje debido causa fiebre 2%, la inflamación de la grasa subcutánea en el sitio de la punción de la pared abdominal en laparocentesis - 1% de los pacientes. La infección de la herida operativa ocurre en el 1% y los abscesos posteriores a la inyección (inyección intramuscular de progesterona) en 0.5%. La fiebre de génesis no infecciosa en cada segundo paciente con CHD probablemente esté asociada con mecanismos pirogénicos endógenos. Los casos únicos de sepsis se describen en el curso severo de SWS.
En el contexto del desarrollo del síndrome hay una exacerbación de enfermedades somáticas crónicas latentes actuales.
¿Qué te molesta?
Clasificación
No existe una clasificación uniforme del síndrome de hiperestimulación ovárica. Sobre la base de los síntomas clínicos y de laboratorio se distinguen cuatro grados de severidad del síndrome:
- SOH de un grado fácil. Malestar abdominal, ovarios hasta 8 cm de diámetro con quistes o sin parámetros de laboratorio son SHO normales leve conocida como "la hiperestimulación ovárica controlada", ya que es capaz de ver absolutamente todos los ciclos de superovulación y no se considera como un síndrome patológico en el momento, requiriendo tratamiento
- SOH de un grado promedio. El dolor leve en absoluto abdomen, náuseas, vómitos, diarrea y los ovarios son 8-12 cm de diámetro con quistes, ultrasonidos y / o signos clínicos de la ascitis, el hematocrito es menor que 45%, leucocitosis - 10-16h10 9 / l, hipercoagulabilidad (D- dímero - más de 0.5 μg / ml, concentración de fibrinógeno - más de 400 mg / dl, APTT, MNO - dentro de los límites de la norma).
- HHS severo. Hematocrito 45%, leucocitosis - 17-24h10 9 / l, hipercoagulabilidad (D-dímero, 5 ug / ml de fibrinógeno más de 600 mg / dl), los ovarios más de 12 cm de diámetro con quistes, todos los signos clínicos y de laboratorio de SHO moderado y ascitis de tensión, hidrotórax, disfunción hepática, oliguria [diuresis inferior a 0,5 ml / (kg h)].
- OSS de un grado crítico. Hematocrito más de 55%, más leucocitosis 25h109 / l, ascitis a tensión, hidrotórax bilateral, hidropericardio, anasarca, aumento del tamaño de ovario de 20-25 cm, oliguria o anuria, OPN, complicaciones tromboembólicas de SDRA.
Además, el síndrome de hiperestimulación ovárica se divide en temprano y tardío.
Si SHH ocurre en la fase lútea y no ocurre la implantación, el síndrome desaparece brusca y espontáneamente con el inicio de la menstruación, raramente alcanza una forma severa. Si se produce la implantación, con mayor frecuencia se observa el deterioro de la condición del paciente durante las primeras 12 semanas de embarazo. La CGR tardía es causada por un aumento significativo de CG en el plasma sanguíneo y generalmente se asocia con la implantación y el embarazo precoz.
Consecuencias y complicaciones
Las complicaciones del síndrome de hiperestimulación ovárica pueden ocurrir con el desarrollo de complicaciones tromboembólicas. La causa de la trombosis en el síndrome de hiperestimulación ovárica es desconocidos altas concentraciones, sin embargo, el papel principal en la patogénesis de esta condición se retira de las hormonas sexuales, citoquinas inflamatorias, la reducción de la hemoconcentración y CGO. Hospitalización a largo plazo, la restricción de la actividad física, disminución del retorno venoso, debido al aumento de los ovarios, aumento de la actividad de factores de coagulación, la fibrinólisis, y los inhibidores de plaquetas contribuye aún más al alto riesgo de complicaciones trombóticas de síndrome de hiperestimulación ovárica. Demostró que el 84% de los pacientes con complicaciones tromboembólicas, surgidos después de la inducción de la ovulación en las técnicas de reproducción asistida, su desarrollo se llevó a cabo en el contexto del embarazo en el 75% de los casos, hay coágulos de sangre en la línea venosa localizados preferentemente en los vasos sanguíneos de la konechnosey superior, el cuello y la cabeza ( 60%). Un número de pacientes fueron diagnosticados con trombosis arterial espontánea localizada en los vasos cerebrales. Menos comúnmente observado la formación de coágulos en el, poplítea, carótida, subclavia, ilíaca, el codo, la arteria mesentérica femoral y la aorta. En la literatura se presenta con SHO observación de la oclusión de la arteria central de la retina con pérdida de la visión. La incidencia de embolia pulmonar en pacientes con síndrome de hiperestimulación ovárica y trombosis de venas profundas es 29%, mientras que en las mujeres con síndrome de hiperestimulación ovárica, y trombosis venosa profunda de las extremidades superiores y trombosis arterial riesgo de esta complicación es mucho menor, a las 4 y 8%, respectivamente.
El curso severo del síndrome de hiperestimulación ovárica puede ir acompañado de complicaciones que requieren intervención quirúrgica: ruptura del quiste ovárico y hemorragia intraabdominal, torsión de los apéndices del útero, embarazo ectópico.
Diagnóstico del síndrome de hiperestimulación ovárica
El diagnóstico de síndrome de hiperestimulación ovárica se establece en base a los datos de la historia, un laboratorio clínico integrado y un examen decisivo revelaron un aumento con múltiples quistes ováricos expresadas hemoconcentración y paciente hipercoagulabilidad usado en los presentes métodos de ciclo de técnicas de reproducción asistida inducción de la ovulación o controlados para lograr el embarazo.
Investigación de laboratorio
Prueba de sangre clínica
Hematocrito más del 40%, concentración de hemoglobina más de 140 g / l, leucocitosis hasta 50x10 9 / l sin desplazamiento hacia la izquierda, trombocitosis hasta 500-600x10 6 / l. La hemoconcentración (hematocrito superior al 55%) indica una amenaza potencial para la vida.
Análisis bioquímico de sangre
Desequilibrio de electrolitos incluyendo hiperpotasemia (más de 5,3 mmol / l) y la hiponatremia (más de 135 mmol / l), resultando en la reducción osmolaridad del plasma. Hipoproteinemia (proteína total más de 66 g / l), hipoalbuminemia (albúmina de menos de 35 g / l), un alto nivel de proteína C-reactiva, transaminasas hepáticas elevadas y 800 U / l, en algunos casos, el aumento de GGT o fosfatasa alcalina, en algunos pacientes - un aumento en la concentración de creatinina de más de 80 μmol / ly urea en más de 8.3 mmol / l.
Coagulograma
Aumento de los niveles de fibrinógeno de más de 400 mg / dl, factor de von Willebrand más de 140%, concentraciones menores de antitrombina III de menos del 80%, dímero D de más de 0.5 μg / ml. Indicadores normales de APTT, PTI, INR.
 [24]
[24]
Inmunoglobulinas de sangre
Reducción de la concentración en plasma sanguíneo IgG e IgA El análisis de la orina es general. Proteinuria.
Análisis de la composición del líquido ascítico
El alto contenido de proteína (más de 42 g / l) y la albúmina (más de 23 g / L), bajo recuento de glóbulos blancos, un número relativamente alto de células rojas de la sangre, las altas concentraciones de citoquinas pro-inflamatorias, la proteína C reactiva a 135 mg / l (normalmente 0-8 , 2 mg / l), la fracción de globulina de las proteínas.
 [25], [26], [27], [28], [29], [30], [31]
[25], [26], [27], [28], [29], [30], [31]
Oncoproteínas en el plasma sanguíneo
La concentración de CA-125, que refleja la proliferación masiva de tejido ovárico, alcanza sus valores máximos (hasta 5125 U / ml) en la segunda semana de desarrollo de SHO, cuando ambos ovarios están más agrandados. Los niveles elevados de oncomarker persisten hasta 15-23 semanas después de la aparición de los síntomas del síndrome de hiperestimulación ovárica, a pesar del tratamiento en curso.
La procalcitonina en el suero se determina en 50% de los pacientes en el rango de 0.5-2.0 ng / ml, que se considera una reacción inflamatoria sistémica de grado moderado.
Examen microbiológico
En el análisis de orina, secreción de la patógenos atípicos vagina, canal cervical se aísla Pseudomonas, Proteus, Klebsiella, Enterobacter, E coli en una cantidad de más de 10.000 ufc / ml.
La investigación instrumental
Ultrasonido de los órganos pélvicos
Aumento de los ovarios de 6 a 25 cm de diámetro con múltiples quistes, útero de tamaño normal o agrandado, presencia de líquido libre en la cavidad pélvica y embarazo simple progresivo normal o embarazo múltiple.
Ultrasonido de los órganos de la cavidad abdominal
La presencia en la cavidad abdominal de un líquido libre en una cantidad de 1 a 5-6 litros. Tamaño y estructura normales del hígado o hepatomegalia Ecos de discinesia del tracto biliar. Al estudiar los riñones, el complejo de la copa y la pelvis no cambia.
Ultrasonido de las cavidades pleurales
Presencia de ecocardiografía de fluido libre. En el contexto de los trastornos hemodinámicos, una disminución en la FE, una disminución en el volumen diastólico final, una disminución en el retorno venoso, en algunos casos, la presencia de líquido libre en la cavidad pericárdica.
ECG
Violación de un ritmo como arritmia ventricular, taquicardia, cambios difusos de metabólica y la naturaleza del electrolito de miocardio. Radiografía del cofre. Conducido con sospecha de SDRA y tromboembolismo. El hallazgo radiológico característico en el SDRA - la aparición de la pintura "mate" y multifocal infiltrados difusos una densidad bastante alta (consolidación) con un bien redondeado bronquitis aire, las desarrolladas extensa del parénquima pulmonar. Cuando PE en las radiografías muestran cúpula de diafragma alto standing, atelectasia discoide, congestión pulmonar de una de las raíces o el patrón "desmochada" agotamiento raíz pulmonar sobre el área isquémica del pulmón, inflamación periférica sombra triangular.
Indicaciones para la consulta de otros especialistas
Debido a la participación de todos los órganos y sistemas en el proceso patológico, el terapeuta debe ser examinado. Si hay una sospecha de complicaciones trombóticas, consulte a un cirujano vascular. En presencia de hidrotórax pronunciado, consulta al cirujano torácico para resolver el problema de realizar una punción de la cavidad pleural.
¿Qué es necesario examinar?
Cómo examinar?
¿Qué pruebas son necesarias?
Tratamiento del síndrome de hiperestimulación ovárica
La falta de un concepto claro de la fisiopatología del síndrome de hiperestimulación ovárica hace que sea imposible llevar a cabo un tratamiento eficaz, basado pathogenetically disposición de eficacia y prontitud para detener el desarrollo del síndrome y varios trastornos de los órganos que acompañan forma grave de síndrome de hiperestimulación ovárica. Actualmente, la terapia específica de síndrome de hiperestimulación ovárica no es, por lo tanto, las medidas terapéuticas en el respeto de estos pacientes para reducir la terapia patógena para reducir al menos la concentración plasmática de hCG momento del síndrome de regresión espontánea durante 7 días en un ciclo en el que no se ha producido el embarazo, o 10-20 días después del inicio del embarazo. La mayoría de los pacientes hospitalizados en la unidad de cuidados intensivos, ha llegado después de diagnosticado con tratamiento ambulatorio SHO que consiste en la evaluación del peso y diuresis diaria, excesivas limitaciones de la actividad física y la sexualidad, bebida abundante, con la adición de soluciones de electrolitos ricos, los análisis de sangre periódica. La discusión de las estrategias para el tratamiento de este grupo de pacientes implica la realización de un tratamiento sintomático amplia encaminada a prevenir el desarrollo de MODS mediante la restauración de ORC, eliminando hemoconcentración, desequilibrios electrolíticos, la prevención de la insuficiencia renal aguda, síndrome de dificultad respiratoria aguda y complicaciones tromboembólicas.
1 ° etapa: evaluación de la gravedad de la afección
El primer paso para determinar las tácticas de los pacientes con el síndrome de hiperestimulación ovárica - Evaluación de la función hemodinámica y respiratoria, también es necesario llevar a cabo un examen físico completo, con un cuidadoso estudio del estado final, la cabeza y el cuello para descartar la trombosis venosa profunda y la instalación de catéter venoso periférico o un catéter venoso central, con la más conveniente vena subclavia cateterismo ya que el riesgo de trombosis en este caso el más bajo. Para evaluar la diuresis, es necesario un cateterismo de la vejiga. Indicadores clínicos diaria es necesario estudiar los análisis de sangre, electrolitos del plasma, proteínas, actividad de las enzimas hepáticas, creatinina, urea, ultrasonido parámetros de coagulación abdominal llevado a cabo para determinar el grado de aumento en el tamaño de los ovarios y la presencia de ascitis.
Etapa 2 - terapia de infusión
El tratamiento farmacológico para pacientes con SHO debe estar dirigido a mantener la hemodinámica y movilizar el líquido contenido en la cavidad abdominal creando un balance negativo de sodio y agua. La tarea principal es recuperar el volumen de fluido circulante para reducir la hemoconcentración y mantener una filtración renal suficiente. Para la terapia de infusión del síndrome de hiperestimulación ovárica, se usan soluciones coloidales y coloidales.
La elección de la solución cristaloide determina el desequilibrio electrolítico. Al determinar el número de cristaloides de entrada necesario considerar que en condiciones de daño endotelial volumen generalizada de estas soluciones debe ser menor que el volumen de soluciones coloidales en 2-3 veces, como cristaloide predominio exacerbado acumulación de líquido en las cavidades serosas, y en algunos casos conduce al desarrollo de hidropesía.
El fármaco de elección para la restauración y el mantenimiento del volumen intravascular en pacientes con OHSS - hidroxietil almidón 130/0 42 volumen diario - 25-30 ml / kg. También se puede usar hidroxietil almidón 200/0 5 con un volumen de 20 ml / (kilogramo) en la terapia básica de CHD. Sin embargo, es capaz de acumularse en el uso del cuerpo y a largo plazo puede causar disfunción hepática y para aumentar el nivel de transaminasas hepáticas a veces hasta 800 U / L. En este grupo de pacientes es poco práctico para aplicar hidroxietil 450/0 7 debido al alto riesgo de reacciones alérgicas, influencia negativa sobre la función de los riñones, el hígado, el deterioro de los parámetros hemocoagulation (tiempo de coagulación de elongación, el riesgo de complicaciones de sangrado). Las indicaciones para el uso de soluciones de dextrano de alta frecuencia limitada de reacciones alérgicas, influencia negativa sobre el sistema hemostático, la liberación de factor de von Willebrand, la inducción de la cascada proinflamatoria, la falta de efecto sobre las propiedades reológicas de la sangre a las dosificaciones. Dextranos de infusión en condiciones de aumento de la permeabilidad de los capilares pueden conducir al desarrollo de la llamada dextrano síndrome seguido de OL, deterioro de la función hepática, coagulopatía el desarrollo del riñón. Las soluciones de gelatina tampoco están destinadas a la terapia de infusión con CHD.
Cuando la hipoproteinemia es inferior a 25 g / l, se utiliza una solución al 20% de albúmina, volumen diario: 3 ml / kg. Se recomienda el uso de solución de albúmina sólo el 20% como la presión oncótica de una solución al 20% es de aproximadamente 100 mm Hg, y 5% de la presión oncótica de la solución es de aproximadamente 20 mm. Gt; Art. Dada la alta permeabilidad de infusión vascular endotelial de solución de albúmina al 5% en lugar de una solución al 20% conduce a un intercambio más intensivo con piscina extravascular y un fuerte aumento de la presión oncótica en el intersticio, lo que conduce a un aumento en la sobrehidratación de pulmón intersticial.
Los diuréticos están justificados en oliguria, edema periférico, alcanzando valores de hematocrito de 36-38%. La prescripción prematura o excesiva de diuréticos puede provocar agravamiento de la hipovolemia y la hemoconcentración, lo que aumenta el riesgo de complicaciones trombóticas. Aplicar principalmente furosemida - 20-40 mg una vez por vía intramuscular o intravenosa lentamente durante 1-2 minutos.
Principios de la terapia de infusión en el síndrome de hiperestimulación ovárica
Después de la dosis inicial de terapia adicional volumen de infusión de cristaloides y coloides se determina de acuerdo con los siguientes indicadores diuresis - menos de 1 ml / (kghch), el hematocrito de menos de - 40%, la presión arterial media - 70 valor mm RTST, CVP - 8-10 mm. Agua Art. Cuando se alcanzan estos parámetros, la terapia de infusión se detiene. El volumen diario total de soluciones de infusión se debe administrar fraccionalmente dentro de las 24 horas. Si no se siguen estos enfoques, se desarrolla hemodilución, que provoca una acumulación rápida de líquido en las cavidades serosas y un empeoramiento de la condición del paciente. Un error típico en el tratamiento de mujeres con síndrome de hiperestimulación ovárica es una extensión injustificada de la terapia de infusión con la normalización de los parámetros hemodinámicos y de intento de detener completamente el desarrollo del síndrome de hiperestimulación ovárica como una condición iatrogénica.
Etapa 3: prevención de complicaciones
Prevención de trombosis y tromboembolismo
La base para la prevención de complicaciones trombóticas en el síndrome de hiperestimulación ovárica es la eliminación de la hemoconcentración. La terapia antitrombótica está indicada cuando aparecen signos de hipercoagulabilidad en el laboratorio. Para esto, se usa LMWH:
- supraparina cálcica (dosis diaria - 100 anti-Ha IU / kg 2 veces por vía subcutánea),
- dalteparina sódica (100-150 anti-Ha IU / kg 2 veces por vía subcutánea),
- enoxaparina sódica (1 ml de Dkgsut) 1-2 veces por vía subcutánea).
Monitoreo de laboratorio: determinación de la actividad anti-Xa del plasma 3 horas después de la administración de HBPM, que permite mantener una dosis efectiva del fármaco dentro del rango terapéutico seguro y así minimizar la posibilidad de sangrado. El nombramiento de medicamentos antitrombóticos se continúa hasta que los parámetros de coagulación de la sangre se normalicen. La monitorización se lleva a cabo para determinar la concentración de dímero D en plasma mediante un método cuantitativo. La duración de la administración de HBPM se determina individualmente, y en algunos casos puede exceder los 30 días.
Prevención de complicaciones infecciosas
Teniendo en cuenta el efecto positivo de la designación de preparaciones de inmunoglobulina en la prevención de infecciones secundarias en otras enfermedades acompañadas de pérdida de proteínas, se puede contar con la efectividad de esta terapia en pacientes con SHO. Sin embargo, es necesario investigar la actualidad, la indicación de tratamiento antibiótico empírico para la confirmación final o refutación de esta hipótesis desde la perspectiva de la medicina basada en la evidencia - el riesgo de infección secundaria en la hemodinámica críticamente enfermos o inestables. El cambio del fármaco seleccionado empíricamente se realiza de acuerdo con los resultados de un estudio bacteriológico. Cuando se prescribe una terapia antibacteriana empírica, es necesario guiarse por la información sobre la gravedad de la enfermedad, los factores de riesgo para la infección y las características de la resistencia a los antibióticos en esta UCI.
Apoyo nutricional
Conducta por vía oral a todos los pacientes con SHO grave y crítico. Es necesario seguir las recomendaciones:
- el valor de energía es 25-35 kcal / (kilohsut),
- glucosa - menos de 6 g / (kghsut),
- lípidos - 0.5-1 g / (kilohsut),
- Proteínas - 1,2-2 g / (kilohsut),
- un conjunto estándar diario de microelementos y vitaminas.
4 ° etapa - métodos quirúrgicos
Indicaciones para la laparocentesis en mujeres con síndrome de hiperestimulación ovárica:
- ascitis de tensión progresiva,
- oliguria inferior a 0,5 ml de Dkgmmin),
- un aumento en la concentración de creatinina de más de 80 μmol / lo una disminución en su eliminación,
- hemoconcentración con un valor de hematocrito de más del 40%, no susceptible de corrección del fármaco.
Para la laparocentesis, se puede seleccionar el acceso transabdominal o transvaginal. La complejidad técnica es creada por los ovarios agrandados, en relación con los cuales el uso del control por ultrasonido es extremadamente importante. Drenaje abdominal prolongado (paracentesis transabdominal) de 14 a 30 días en porciones eliminación de trasudado catéter peritoneal libre de pirógenos cystoFix® tiene varias ventajas debido a que evita la evacuación simultánea de un gran volumen de trasudado peritoneal y de ese modo eliminar las fluctuaciones bruscas de la causa presión inestabilidad hemodinámica intra-abdominal, estabilizar la condición del paciente, evitar punciones repetidas de la cavidad abdominal para eliminar la ascitis en esta categoría de pacientes. El volumen total de fluido de ascitis evacuado por un período de tratamiento de SHO grave puede ser de entre 30 a 90 litros.
En pacientes con hidrotórax en el fondo del síndrome de hiperestimulación ovárica, el manejo expectante está justificado. Al formar el hidrotórax, la punción de la cavidad pleural se realiza solo en el caso de insuficiencia respiratoria progresiva pronunciada.
Criterios para iniciar el soporte respiratorio en el síndrome de hiperestimulación ovárica grave y crítica:
- falta de respiración independiente y ritmos respiratorios anormales,
- una reducción en el índice respiratorio de menos de 200 mm Hg,
- trastornos del ritmo cardíaco potencialmente mortales,
- taquicardia persistente más de 120,
- hipotensión severa,
- taquipnea más de 40,
- afectación de músculos respiratorios auxiliares.
Con el desarrollo de ARDS y la transferencia al uso de ventilación artificial:
- volúmenes respiratorios pequeños (6 ml / kg),
- presión inspiratoria <30 cm de agua,
- PEEP (> 10 cm de agua),
- aplicar la maniobra de reclutamiento de alvéolos.
El tratamiento quirúrgico en el síndrome de hiperestimulación ovárica se justifica solo en presencia de una patología aguda de torsión del epidídimo, ruptura del quiste ovárico, hemorragia del quiste ovárico. Cuando la torsión ovárica es más efectiva lavosa laparoscópica del ovario. Un error típico en la estrategia de tratamiento para pacientes con OHR no complicada es una cirugía de emergencia y resección de aproximadamente 30-50% de tejido ovárico u ovariectomía bilateral.

