Médico experto del artículo.
Nuevos artículos
Atresia esofágica
Último revisado: 12.07.2025

Todo el contenido de iLive se revisa médicamente o se verifica para asegurar la mayor precisión posible.
Tenemos pautas de abastecimiento estrictas y solo estamos vinculados a sitios de medios acreditados, instituciones de investigación académica y, siempre que sea posible, estudios con revisión médica. Tenga en cuenta que los números entre paréntesis ([1], [2], etc.) son enlaces a estos estudios en los que se puede hacer clic.
Si considera que alguno de nuestros contenidos es incorrecto, está desactualizado o es cuestionable, selecciónelo y presione Ctrl + Intro.
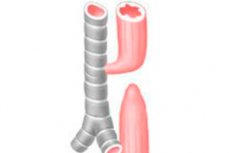
La atresia esofágica (AE) es una malformación congénita en la que el esófago termina ciegamente a una distancia aproximada de 8-12 cm de la entrada a la cavidad oral.
La fístula traqueoesofágica congénita sin atresia es un canal patológico revestido de tejido de granulación o epitelio, que comunica la luz inalterada del esófago con la luz de la tráquea.
La atresia esofágica es el tipo más común de atresia gastrointestinal.
Epidemiología
La atresia esofágica es una malformación congénita del tracto gastrointestinal superior con una prevalencia mundial estimada de 1 de cada 2500 a 1 de cada 4500 nacimientos.[ 1 ] En los Estados Unidos, se estima que la prevalencia es de 2,3 por cada 10 000 nacidos vivos.[ 2 ] La incidencia relativa de la atresia esofágica aumenta con la edad materna.[ 3 ],[ 4 ]
Causas atresia esofágica
La etiología de la atresia esofágica con o sin fístula traqueoesofágica asociada es la falta de separación o el desarrollo incompleto del intestino anterior.[ 5 ] El trayecto de la fístula se origina a partir de una rama del rudimento pulmonar embrionario que no se ramifica debido a interacciones epiteliales-mesenquimales defectuosas.
Varios genes se han asociado con la atresia esofágica, incluyendo Shh, [ 6 ] SOX2, CHD7, MYCN y FANCB. Sin embargo, la etiología no se comprende completamente y probablemente sea multifactorial. Los pacientes pueden ser diagnosticados con AP/TPS aislada o como parte de un síndrome como VACTERL o CHARGE.
Patogenesia
El esófago es un tubo muscular que transporta el bolo alimenticio desde la faringe hasta el estómago. El esófago se origina de la capa germinal del endodermo que forma la faringe, el esófago, el estómago y las líneas epiteliales del tracto aerodigestivo. La tráquea y el esófago surgen de la división de un tubo intestinal anterior común temprano en el desarrollo fetal. [ 7 ] La falta de separación o desarrollo completo de este tubo intestinal anterior común puede resultar en fístula traqueoesofágica (FTE) y atresia esofágica (AE). Prenatalmente, los pacientes con atresia esofágica pueden presentar polihidramnios, predominantemente en el tercer trimestre, que puede ser una pista diagnóstica de atresia esofágica.

Además, aproximadamente el 50% de los pacientes con TPS/EA tendrán anomalías congénitas asociadas, incluyendo VACTERL (defectos vertebrales, atresia anal, defectos cardíacos, fístula traqueoesofágica, anomalías renales y anomalías de las extremidades) o CHARGE ( coloboma, defectos cardíacos, atresia de coanas, retraso del crecimiento, anomalías genitales y anomalías del oído). Después del nacimiento del neonato, los síntomas más comunes de atresia esofágica son salivación excesiva, atragantamiento e incapacidad para pasar una sonda nasogástrica. Además, si hay TPS asociado, se producirá distensión gástrica a medida que el aire pasa desde la tráquea a través de la fístula esofágica distal y luego al estómago.
Los pacientes con este complejo de síntomas deben someterse a una evaluación acelerada para atresia esofágica y fístula traqueoesofágica y ser remitidos rápidamente a un nivel superior de atención para que los evalúe un cirujano pediátrico.
Fisiopatología
La fístula traqueoesofágica y la atresia esofágica son resultado de una división lateral defectuosa del intestino anterior en esófago y tráquea. El trayecto fistuloso entre el esófago y la tráquea puede formarse secundariamente debido a interacciones epiteliales-mesenquimales defectuosas. [6] La fístula traqueoesofágica y la atresia esofágica se presentan juntas en aproximadamente el 90% de los casos. La atresia esofágica y la fístula traqueoesofágica se clasifican en cinco categorías según su configuración anatómica. [ 8 ]
- El tipo A es una atresia esofágica aislada sin fístula traqueoesofágica asociada, cuya prevalencia es del 8%.
El esófago proximal y distal terminan ciegamente y no están conectados a la tráquea. El esófago proximal está dilatado, tiene paredes gruesas y suele terminar más arriba en el mediastino posterior, cerca de la segunda vértebra torácica. El esófago distal es corto y termina a distancias variables del diafragma. La distancia entre ambos extremos determinará si es posible la reparación primaria (poco frecuente) o si se debe realizar una anastomosis primaria diferida o un reemplazo esofágico. En estos casos, es importante descartar una fístula traqueoesofágica proximal.
- El tipo B es la atresia esofágica con fístula traqueoesofágica proximal. Es el tipo más raro, con una prevalencia del 1%.
Esta rara anomalía debe distinguirse de la variante aislada. La fístula no se localiza en el extremo distal del saco superior, sino 1-2 cm por encima de su extremo en la pared anterior del esófago.
- La atresia esofágica tipo C es la más común (84-86%) e implica atresia esofágica proximal con fístula traqueoesofágica distal.
Se trata de una atresia en la que el esófago proximal se dilata y la pared muscular se engrosa, terminando ciegamente en el mediastino superior, aproximadamente a la altura de la tercera o cuarta vértebra torácica. El esófago distal, más delgado y estrecho, desemboca en la pared posterior de la tráquea por la carina o, más comúnmente, uno o dos centímetros proximal a la tráquea. La distancia entre el esófago proximal ciego y la fístula traqueoesofágica distal varía desde segmentos superpuestos hasta una hendidura amplia. En muy raras ocasiones, la fístula distal puede ocluirse u obliterarse, lo que lleva a un diagnóstico erróneo de atresia aislada antes de la cirugía.
- Tipo D: atresia esofágica con fístula traqueoesofágica proximal y distal, rara (alrededor del 3%).
En muchos de estos lactantes, la anomalía se diagnosticó erróneamente y se trató como atresia proximal y fístula distal. Como resultado de infecciones respiratorias recurrentes, se identificó durante la exploración una fístula traqueoesofágica, previamente confundida con una fístula recurrente. Con el creciente uso de la endoscopia preoperatoria (broncoscopia y/o esofagoscopia), la fístula "doble" puede reconocerse precozmente y repararse por completo durante el procedimiento inicial. Si no se identifica una fístula proximal preoperatoriamente, el diagnóstico debe sospecharse por una fuga de gas importante que se origina en el reservorio superior durante la anastomosis.
- La atresia esofágica tipo E es una fístula traqueoesofágica aislada sin atresia esofágica asociada. Se conoce como tipo "H" y tiene una prevalencia de aproximadamente el 4%.
Existe una conexión fistulosa entre el esófago anatómicamente intacto y la tráquea. El trayecto fistuloso puede ser muy estrecho, de 3 a 5 mm de diámetro, y suele localizarse en la región cervical inferior. Suelen ser únicas, pero se han descrito dos o incluso tres fístulas.

Tipos anatómicos comunes de atresia esofágica: a) Atresia esofágica con fístula traqueoesofágica distal (86%). b) Atresia esofágica aislada sin fístula traqueoesofágica (7%). c) Fístula traqueoesofágica tipo H (4%).
Síntomas atresia esofágica
En aproximadamente un tercio de los fetos, la atresia esofágica y la fístula traqueoesofágica se diagnostican prenatalmente. El signo ecográfico más común de atresia esofágica es el polihidramnios, que se presenta en aproximadamente el 60 % de los embarazos. [ 9 ] Si se diagnostica prenatalmente, se puede asesorar a la familia sobre las expectativas posnatales.
Sin embargo, en muchos casos, el diagnóstico no se realiza hasta el nacimiento. Los bebés con atresia esofágica presentan síntomas poco después del nacimiento, con aumento de secreciones que provoca asfixia, dificultad respiratoria o episodios de cianosis durante la alimentación. En la atresia esofágica, una fístula entre la tráquea y el esófago distal hace que el estómago se llene de gas en la radiografía de tórax. Los bebés con atresia esofágica de tipo A y B no presentarán distensión abdominal porque no existe una fístula desde la tráquea hasta el esófago distal. Los bebés con una fístula traqueoesofágica pueden refluir el contenido del estómago a través de la fístula hacia la tráquea, lo que provoca neumonía por aspiración y dificultad respiratoria. En pacientes con atresia esofágica de tipo E, el diagnóstico puede retrasarse si la fístula es pequeña.[ 10 ]
¿Donde duele?
¿Qué te molesta?
Formas
Existen alrededor de 100 variantes conocidas de este defecto, pero tres de las más comunes son:
- atresia esofágica y fístula entre el esófago distal y la tráquea (86-90%),
- atresia esofágica aislada sin fístula (4-8%),
- fístula traqueoesofágica tipo H (4%).
En el 50-70% de los casos de atresia esofágica hay defectos de desarrollo combinados:
- defectos cardíacos congénitos (20-37%),
- defectos del tracto gastrointestinal (20-21%),
- defectos del sistema genitourinario (10%),
- defectos musculoesqueléticos (30%),
- defectos craneofaciales (4%).
En el 5-7% de los casos, la atresia esofágica se acompaña de anomalías cromosómicas (trisomías 18, 13 y 21). Una combinación peculiar de anomalías del desarrollo en la atresia esofágica se denomina "VATER" por las iniciales en latín de los siguientes defectos del desarrollo (5-10%):
- defectos espinales (V),
- defectos anales (A),
- fístula traqueoesofágica (T),
- atresia esofágica (E),
- defectos del hueso del radio (R).
Entre el 30 y el 40% de los niños con atresia esofágica son prematuros o presentan retraso del crecimiento intrauterino. [ 11 ], [ 12 ]
Complicaciones y consecuencias
Pueden presentarse complicaciones quirúrgicas tras la reparación de la atresia esofágica. La complicación más temida es la fuga anastomótica esofágica.[ 13 ] Las fugas pequeñas pueden tratarse con drenaje torácico y ayunas prolongadas hasta su corrección. Si se detecta una fuga importante o una fuga anastomótica, puede ser necesaria una reintervención y una resección esofágica con interposición de un injerto gástrico, colónico o yeyunal.
Otra posible complicación es la estenosis de la anastomosis esofágica. Estas suelen tratarse con dilataciones esofágicas endoscópicas seriadas.[ 14 ] Finalmente, aunque es poco frecuente, se ha reportado fistulización recurrente del esófago y la tráquea. Estos problemas se tratan con reintervención.
Las complicaciones no quirúrgicas de la atresia esofágica y la fístula traqueoesofágica son frecuentes. Se recomienda el uso de inhibidores de la bomba de protones durante al menos un año tras la reparación de la atresia esofágica debido a la dismotilidad esofágica, que conlleva un aumento del reflujo gastroesofágico (RGE) y riesgo de aspiración.[ 15 ] La traqueomalacia es frecuente después de la cirugía. Los neonatos con atresia esofágica y fístula traqueoesofágica suelen presentar una mayor incidencia de disfagia, infecciones de las vías respiratorias y esofagitis.[ 16 ]
Debido al elevado RGE en la infancia y la adultez, estos niños tienen una mayor incidencia de esófago de Barrett y un mayor riesgo de cáncer de esófago en comparación con la población general.[ 17 ] Se recomiendan protocolos de detecciónde cáncer de esófago en estos pacientes, aunque esto es controvertido.
Diagnostico atresia esofágica
La atresia esofágica suele diagnosticarse cuando no se puede introducir una sonda orogástrica. La sonda no llega hasta el estómago y puede observarse enrollada por encima del nivel de la atresia esofágica en la radiografía de tórax. El diagnóstico definitivo se puede realizar inyectando una pequeña cantidad de medio de contraste hidrosoluble en la sonda orogástrica bajo guía fluoroscópica. Se debe evitar el bario, ya que puede causar neumonitis química si se aspira a los pulmones. Para confirmar el diagnóstico, se puede realizaruna esofagoscopia o una broncoscopia para detectar una fístula traqueal.[ 18 ]
Un recién nacido con atresia esofágica y fístula traqueoesofágica requiere evaluación para anomalías de VACTERL y CHARGE, ya que pueden ocurrir en hasta el 50% de los recién nacidos. Específicamente, una evaluación completa requiere un ecocardiograma cardíaco, radiografías de las extremidades y la columna vertebral, ecografía renal y un examen físico minucioso del ano y los genitales para detectar cualquier anomalía. Un gran estudio de un solo centro en los Estados Unidos examinó las anomalías congénitas más comunes asociadas con atresia esofágica y fístula traqueoesofágica. Entre casi 3000 pacientes, los diagnósticos de VACTERL asociados incluyeron anomalías espinales en el 25,5%, malformaciones anorrectales en el 11,6%, defectos cardíacos congénitos en el 59,1%, enfermedad renal en el 21,8% y defectos en las extremidades en el 7,1%. [ 19 ] Casi un tercio tenía 3 o más anomalías y cumplía los criterios para un diagnóstico de VACTERL.
¿Qué es necesario examinar?
Cómo examinar?
Diagnóstico diferencial
Los diagnósticos diferenciales incluyen hendiduras laríngeas, traqueales y esofágicas, tabiques o anillos esofágicos, estenosis esofágicas, duplicaciones tubulares esofágicas, esófago corto congénito y agenesia traqueal. Estos diagnósticos pueden investigarse con mayor profundidad mediante diversas técnicas de imagen, desde radiografías y tomografías computarizadas hasta endoscopia y cirugía.
¿A quién contactar?
Tratamiento atresia esofágica
Una vez diagnosticado el diagnóstico de atresia esofágica, se debe intubar al lactante para controlar la vía aérea y evitar una mayor aspiración. Si aún no se ha hecho, se debe insertar suavemente un catéter para succionar las secreciones orofaríngeas. Se le deben administrar antibióticos, líquidos intravenosos y nada por vía oral. Se debe considerar la nutrición parenteral total (NPT). Una vez que el lactante esté hemodinámicamente estable y la vía aérea se haya estabilizado, se debe consultar a un cirujano pediátrico.
El momento del tratamiento quirúrgico definitivo de la atresia esofágica depende del tamaño del lactante. Si el lactante pesa más de 2 kilogramos, generalmente se ofrece cirugía tras la corrección de las anomalías cardíacas, si las hay. Los lactantes con muy bajo peso al nacer (<1500 gramos) suelen tratarse por etapas, con la ligadura inicial de la fístula seguida de la reparación de la atresia esofágica a medida que el lactante crece.[ 20 ]
Las opciones quirúrgicas para la reparación de la atresia esofágica incluyen toracotomía abierta o cirugía toracoscópica asistida por video.[ 21 ] Los pasos son los mismos en ambas cirugías. Se identifica y divide la fístula entre el esófago y la tráquea. Se puede utilizar un broncoscopio para visualizar el origen de la fístula en la tráquea. Una vez ligada la fístula, se repara la atresia esofágica. Típicamente, se coloca una pequeña sonda nasogástrica para cruzar los dos extremos, y los extremos se suturan con sutura absorbible si se pueden alcanzar los extremos sin demasiada tensión. Si los extremos del esófago están bajo demasiada tensión o no se pueden alcanzar, se puede utilizar la técnica de Foker.[ 22 ] Esta técnica utiliza suturas de tracción en los extremos del esófago y los junta lentamente. Una vez que los extremos se juntan sin tensión, se puede realizar la reparación primaria.
Si hay un desgarro esofágico extra largo que impide la anastomosis primaria, se puede utilizar la inserción de otro órgano como el estómago, el colon o el yeyuno.[ 23 ] Los pacientes con atresia esofágica tipo E "tipo H" pueden tratarse con una incisión cervical alta y evitar la toracotomía para la ligadura de la fístula.[ 24 ] La gastrostomía generalmente no está indicada a menos que la anastomosis primaria haya fallado.
Tras la cirugía, el lactante regresa a la unidad de cuidados intensivos neonatales para observación minuciosa. Se deja una sonda pleural en el lado por donde se accedió al tórax. El lactante continúa recibiendo nutrición parenteral total mediante sonda nasogástrica con aspiración intermitente. Se realiza una esofagografía entre 5 y 7 días para comprobar si hay fugas esofágicas. Si no se detecta ninguna fuga, se suele iniciar la alimentación oral. Si hay una fuga, la sonda pleural recogerá el líquido. La sonda pleural se deja colocada hasta que la fuga se cierre o el lactante tolere la alimentación oral.
Pronóstico
El pronóstico para los neonatos con atresia esofágica y fístula traqueoesofágica es relativamente bueno y depende principalmente de las anomalías cardíacas y cromosómicas más que de la atresia esofágica en sí. Generalmente, la supervivencia global es de alrededor del 85-90%.[ 25 ] Se observa una mayor mortalidad cuando existen anomalías cardíacas concomitantes además de la atresia esofágica. Las muertes tempranas se asocian con anomalías cardíacas, mientras que las muertes tardías se asocian con complicaciones respiratorias. La distancia entre las dos bolsas esofágicas, especialmente si es grande, puede determinar el pronóstico.[ 26 ] Todos los neonatos sometidos a reparación de atresia esofágica tendrán problemas gastrointestinales y respiratorios esperados, que generalmente mejoran con la edad.
Fuentes
- Nasr T, Mancini P, Rankin SA, Edwards NA, Agricola ZN, Kenny AP, Kinney JL, Daniels K, Vardanyan J, Han L, Trisno SL, Cha SW, Wells JM, Kofron MJ, Zorn AM. La remodelación epitelial mediada por endosomas aguas abajo de Hedgehog-Gli es necesaria para la separación traqueoesofágica. Dev Cell. 16 de diciembre de 2019;51(6):665-674.e6.
- Pretorius DH, Drose JA, Dennis MA, Manchester DK, Manco-Johnson ML. Fístula traqueoesofágica intrauterina. Veintidós casos. J Ultrasound Med. Septiembre de 1987;6(9):509-13.
- Cassina M, Ruol M, Pertile R, Midrio P, Piffer S, Vicenzi V, Saugo M, Stocco CF, Gamba P, Clementi M. Prevalencia, características y supervivencia de niños con atresia esofágica: Un estudio poblacional de 32 años que incluyó 1.417.724 recién nacidos consecutivos. Birth Defects Res A Clin Mol Teratol. Julio de 2016;106(7):542-8.
- Karnak I, Senocak ME, Hiçsönmez A, Büyükpamukçu N. Diagnóstico y tratamiento de la fístula traqueoesofágica tipo H. J Pediatr Surg. Diciembre de 1997;32(12):1670-4.
- Scott DA, Atresia Esofágica/Fístula Traqueoesofágica: Resumen – CAPÍTULO RETIRO, SOLO PARA REFERENCIA HISTÓRICA. En: Adam MP, Feldman J, Mirzaa GM, Pagon RA, Wallace SE, Bean LJH, Gripp KW, Amemiya A, editores. GeneReviews® [Internet]. Universidad de Washington, Seattle; Seattle (WA): 12 de marzo de 2009.
- Crisera CA, Grau JB, Maldonado TS, Kadison AS, Longaker MT, Gittes GK. Las interacciones epiteliales-mesenquimales defectuosas determinan la organogénesis de la fístula traqueoesofágica. Pediatr Surg Int. 2000;16(4):256-61.
- Spitz L. Atresia esofágica. Orphanet J Rare Dis. 11 de mayo de 2007;2:24.
- Lupo PJ, Isenburg JL, Salemi JL, Mai CT, Liberman RF, Canfield MA, Copeland G, Haight S, Harpavat S, Hoyt AT, Moore CA, Nembhard WN, Nguyen HN, Rutkowski RE, Steele A, Alverson CJ, Stallings EB, Kirby RS. y la Red Nacional de Prevención de Defectos Congénitos. Datos poblacionales sobre defectos congénitos en Estados Unidos, 2010-2014: Enfoque en los defectos gastrointestinales. Birth Defects Res. 1 de noviembre de 2017;109(18):1504-1514.
- Clark DC. Atresia esofágica y fístula traqueoesofágica. Am Fam Physician. 15 de febrero de 1999;59(4):910-6, 919-20.
- Lautz TB, Mandelia A, Radhakrishnan J. Asociaciones VACTERL en niños sometidos a cirugía por atresia esofágica y malformaciones anorrectales: Implicaciones para cirujanos pediátricos. J Pediatr Surg. Agosto de 2015;50(8):1245-50.
- Petrosyan M, Estrada J, Hunter C, Woo R, Stein J, Ford HR, Anselmo DM. Atresia esofágica/fístula traqueoesofágica en neonatos de muy bajo peso al nacer: mejores resultados con la reparación por etapas. J Pediatr Surg. Diciembre de 2009;44(12):2278-81.
- Patkowsk D, Rysiakiewicz K, Jaworski W, Zielinska M, Siejka G, Konsur K, Czernik J. Reparación toracoscópica de fístula traqueoesofágica y atresia esofágica. J Laparoendosc Adv Surg Tech A. 2009 Abr;19 Suppl 1:S19-22.
- Foker JE, Linden BC, Boyle EM, Marquardt C. Desarrollo de una verdadera reparación primaria para todo el espectro de la atresia esofágica. Ann Surg. 1997 Oct;226(4):533-41; discusión 541-3.
- Bairdain S, Foker JE, Smithers CJ, Hamilton TE, Labow BI, Baird CW, Taghinia AH, Feins N, Manfredi M, Jennings RW. Interposición yeyunal tras reparación fallida de atresia esofágica. J Am Coll Surg. Junio de 2016;222(6):1001-8.
- Ko BA, Frederic R, DiTirro PA, Glatleider PA, Applebaum H. Acceso simplificado para la división de la fístula traqueoesofágica tipo H cervical baja/torácica alta. J Pediatr Surg. Noviembre de 2000;35(11):1621-2. [PubMed]
- dieciséis.
- Choudhury SR, Ashcraft KW, Sharp RJ, Murphy JP, Snyder CL, Sigalet DL. Supervivencia de pacientes con atresia esofágica: influencia del peso al nacer, anomalías cardíacas y complicaciones respiratorias tardías. J Pediatr Surg. Enero de 1999;34(1):70-3; discusión 74.
- Upadhyaya VD, Gangopadhyaya AN, Gupta DK, Sharma SP, Kumar V, Pandey A, Upadhyaya AD. Pronóstico de la fístula traqueoesofágica congénita con atresia esofágica en función de la longitud del espacio. Pediatr Surg Int. 23(8):767-71, agosto de 2007.
- Engum SA, Grosfeld JL, West KW, Rescorla FJ, Scherer LR. Análisis de la morbilidad y la mortalidad en 227 casos de atresia esofágica y/o fístula traqueoesofágica a lo largo de dos décadas. Arch Surg. Mayo de 1995; 130(5):502-8; discusión 508-9.
- Antoniou D, Soutis M, Christopoulos-Geroulanos G. Estenosis anastomóticas tras la reparación de atresia esofágica: experiencia de 20 años con dilatación endoscópica con balón. J Pediatr Gastroenterol Nutr. Octubre de 2010;51(4):464-7.
- Krishnan U, Mousa H, Dall'Oglio L, Homaira N, Rosen R, Faure C, Gottrand F. Pautas ESPGHAN-NASPGHAN para la evaluación y el tratamiento de complicaciones gastrointestinales y nutricionales en niños con atresia esofágica-fístula traqueoesofágica. J Pediatr Gastroenterol Nutr. Noviembre de 2016;63(5):550-570.
- Connor MJ, Springford LR, Kapetanakis VV, Giuliani S. Atresia esofágica y cuidados transicionales: paso 1: una revisión sistemática y un metaanálisis de la literatura para determinar la prevalencia de problemas crónicos a largo plazo. Am J Surg. Abril de 2015;209(4):747-59.
- Jayasekera CS, Desmond PV, Holmes JA, Kitson M, Taylor AC. Grupo de 4 casos de cáncer de células escamosas de esófago en desarrollo en adultos con atresia esofágica corregida quirúrgicamente: ¿es hora de iniciar el cribado? J Pediatr Surg. Abr. 2012;47(4):646-51.
Использованная литература

